Что означает кальциноз аорты и его последствия
В настоящее время аортальный стеноз вследствие возникшего сужения аортального клапана является основным показанием для его протезирования во развитых странах, в том числе и в Красноярске. Несмотря на то, что происходит снижение количества случаев ревматической болезни сердца, из-за старения населения и возникновения атеросклероза у этой группы пациентов, кальциноз клапана стал самой частой проблемой сердечных клапанов в западных странах. Он выявляется приблизительно у 25% взрослых старше 65 лет, из которых 2-3% имеют клинически значимый аортальный стеноз. Даже кальциноз клапана легкой степени ассоциируется с неблагоприятными исходами, и соотноситься с 50% увеличением риска заболеваний сердечно-сосудистой системы. Не существует известных методов лечения, которые замедляют прогрессирование заболевания, и хирургическая замена клапана является единственным эффективным методом лечения аортального стеноза. Более 85000 замена аортального клапана операции делаются в Соединенных Штатах, и более 275000 выполняются по всему миру. Это число, как ожидается, утроится к 2050 году. Указанные выше статистические данные подчеркивают тяжесть заболевания аортального клапана и необходимости понимания ее механизмов, раннее выявление как клинически, так и с использованием неинвазивной эхокардиографии.
Кальциноз аортального клапана является прогрессирующим заболеванием, которое начинается с начальными изменениями в клеточной биологии створки клапана, которые развиваются подобно атеросклеротическому поражению аорты, как и склероз, и в конце концов приводит к кальцификации клапана, вызывая обструкцию оттока крови из выходного тракта левого желудочка. Хотя кальциноз аортального клапана по данных эхокардиографии прогрессирует с возрастом, он не всегда является неизбежным следствием старения. Дело в том, что кальциноз аортального клапана традиционно считался дегенеративным явлением, за длительные годы жизни человека происходят многочисленные механические воздействия на изначально нормальный клапан. Это вызывает оседание кальция на поверхности створки аортального клапана. Однако эволюционирующая концепция, что кальциноз аортального клапана активно регулируется, а значит процесс нельзя охарактеризовать просто как «старение» или «дегенерация». Прогрессивный процесс кальцификации включает в себя накопление липидов, увеличивая количество ангиотензин-превращающего фермента, активность воспаления, неоваскуляризацию и деградацию внеклеточного матрикса.
Надо учесть, что факторы риска кальциноза аортального клапана аналогичны таковым, которые относятся к появлению атеросклероза: возраст, пол, гиперхолестеринемия, сахарный диабет, курение, почечная недостаточность, гипертония. Более того, в патоморфологических исследованиях из извлеченных при протезировании стенотических аортальных клапанов человека были выявлены поражения, похожими на те, что и в атеросклеротических бляшках, которые содержат воспалительные клетки и при отложениях холестерина. Большое значение повышенного уровня холестерина подтверждается исследованиями на ЭхоКГ, демонстрирующих, что у больных с семейной гиперхолестеринемией развиваются поражения аортального клапана в виде кальцификации, которые усиливаются с возрастом. Кроме того, доклинические исследования показали атеросклеротические поражения створок аортального клапана как при атеросклерозе у кроликов и мышей с высоким уровнем холестерина. Из того, что кальциноз створок аортального клапана и атеросклероз может возникать подобным механизмом, то некоторые кардиологи считают, что статины могут включаться в потенциальную терапия для лечения кальциноза аортального клапана. Действительно, ретроспективные исследования с использованием эхокардиографии продемонстрировали уменьшение в прогрессировании заболевания, когда пациенты принимали статины. Кроме того, исследования на животных подтвердили, что лечение статинами сдерживает кальцификацию клапана. Большие проспективные клинические испытания, однако четко не показало, замедление прогрессирования кальциноза аортального клапана у пациентов, получавших высокие дозы статинов. Это может быть из-за позднего внедрения статинов в терапию, после того, ка кальцификация аортального клапана прогрессирует в необратимую стадию.
Аортальный клапан состоит из эндотелиальных клеток и интерстициальных клеток, которые поддерживают здоровье клапаном и их изменения важны в развитии порока сердца. Клапанные интерстициальные клетки, вероятно, опосредуют развитие кальциноза клапана. Какие биологические сигналы аортального клапана запускают активацию, дифференцировку, или патологические изменения пока неясны. Однако, мы знаем, что при кальцинозе аортального клапана, его интерстициальные клетки дифференцируются в миофибробласты и остеобласто-подобные клетки, которые в конечном итоге отвечает за отложение кальция. Патологические триггеры включают гемодинамические напряжения сдвига соединительной ткани, напряжение активных форм кислорода (АТФ), воспалительные цитокины и факторы роста, и физиологический дисбаланс, такие как метаболический синдром, сахарный диабет, терминальная стадия почечной недостаточности, и дисбаланс кальция или фосфата. Клеточные и молекулярные факторы, участвующие в развитии стеноза аортального клапана, однако, остаются в значительной степени неясными. Неблагоприятный прогноз и повышение смертности после появления симптомов дают обоснование для будущих исследований в достижении лучшего понимания процесса заболевания, которые могут привести к эффективным терапевтическим стратегиям для предотвращения кальциноза аортального клапана. В этой статье мы обсуждали современное понимание патофизиологии, факторы риска, клеточные механизмы, диагностики и клинического ведения кальциноза аортального клапана, и описывает направления дальнейших исследований жизненно важное значение для диагностики, лечения, что потенциально предотвращало бы это заболевание.
Причины и лечение кальцификации
Кальций – макроэлемент, участвующий в обменных процессах, является строительным материалом для крепких костей и зубов. Избыточное поступление минерала на фоне нарушения усвоения приводит к его отложению в мягких тканях, внутренних органах и кровеносных сосудах. Такой патологический процесс получил название кальциноз. Кальцификация продолжительное время может протекать бессимптомно и привести к необратимым последствиям в организме.
Классификация кальцификации
Кальцификация – патологический процесс, для которого характерно отложение кальция. В зависимости от локализации макроэлемент может накапливаться и поражать:
В зависимости от этиологии кальцификация бывает 3 типов:
Также кальциноз может быть системным, поражая все органы человека или местным, с локализацией в одном органе или системе.
Причины кальцификации
Отложение кальция в мягких тканях, внутренних органах происходит в результате нарушения метаболизма, что приводит к нарушению усвоения важного макроэлемента для человеческого организма. Чаще всего, сбои в обменных процессах вызваны эндокринными патологиями, болезнями почек инфекционного и аутоиммунного характера, нарушением выработки ферментов при печеночных патологиях и заболеваний поджелудочной железы.
К нарушению обмена кальция может привести недостаточное поступление магния и избыток витамина Д, которые принимают непосредственное участие в усвоении организмом макроэлемента.
Кальцификация отдельного органа может развиваться при образовании кист, опухолей доброкачественного и злокачественного характера, дистрофии тканей.
Процесс образования кальциевых конгломератов также затрагивает соединительную и хрящевую ткань, атеросклеротические бляшки, погибшие паразитирующие микроорганизмы, импланты.
Признаки кальцификации
На начальных этапах распознать патологию крайне сложно в связи с ее бессимптомным течением. Однако некоторые виды имеют достаточно выраженную клиническую картину.
При системном виде кальциноза или при поражении кожных покровов, суставов, эпидермис покрывается небольшими пузырьками, изменения структуры и окраса не наблюдается. По мере прогрессирования патологии кальциевые конгломераты разрастаются и становятся более плотными на ощупь, изменяют свой окрас. Возможно образование свищей.
Известковые отложения в ходе плановых осмотров специалистами или при инструментальном исследовании могут обнаруживаться на зубах, костях, сосудах, мышечных и нервных волокнах. Скопление макроэлемента на тканях органов приводит к нарушению их функционирования.
При поражении сердечной мышцы и сосудистой системы, у больного появляется болевой синдром в грудине, руке, шее, спине, который сохраняется продолжительное время. Также происходит нарушение кровотока, что приводит к скачкам артериального давления, появлению чувства холода в конечностях.
При поражении почек нарастают симптомы интоксикации, нарушается диурез, кожные покровы становятся сухими, вялыми. При кальцификации органов пищеварительного тракта, нарушается их работа, что приводит к возникновению тошноты, рвоты, чувства тяжести в абдоминальной области, запоров.
При поражении и скоплении большого количества кальция в головном мозге больной испытывает частые приступы головной боли и головокружения, скачки внутричерепного давления, нарушение координации движения, ухудшение памяти, проблемы со зрением и слухом. По мере прогрессирования болезни возможны обмороки.
Вместе с этим кальциноз приводит к снижению работоспособности, постоянной вялости и усталости, слабости, снижению массы тела.
Диагностика
Для подтверждения диагноза используется рентгенологическая диагностика. Данный метод позволяет определить характер и размер отложений, а также степень поражения органа, в котором локализуется кальциевый конгломерат. В качестве дополнительных методов исследования назначается:
Для выявления причины кальцификации тканей назначаются дополнительные исследования, в виде общеклинического и биохимического анализа крови. Последний способ позволяет определить уровень кальция, фосфора и магния в крови. При нарушении функций почек назначается общеклинический и бактериологический анализ мочи для оценки работоспособности почек.
Для исключения злокачественного характера новообразований в пораженном органе назначается биопсия тканей. Данный метод предполагает забор биологического материала и его исследования под микроскопом в лабораторных условиях. Биопсия помогает также дифференцировать доброкачественное и злокачественное новообразование.
Лечение
Для лечения кальциноза назначается терапевтический курс, который поможет справиться с заболеванием-первопричиной. Так, если к избыточному отложению кальция привело воспаление инфекционной природы, назначаются антибактериальные препараты.
При нарушении усвоения кальция назначаются медикаменты, содержащие магний, который является антагонистом кальция. Достаточное поступление магния с продуктами питания и медикаментозными препаратами позволяет растворить конгломераты и вывести избыток кальция из организма. В ходе лечения важно принимать диуретики, которые помогут ускорить процесс выведения макроэлемента.
В процессе усвоения кальция принимает участие витамин Д, избыточное поступление которого также отрицательно сказывается на состоянии организма. Поэтому в ходе лечения необходимо соблюдать специальную диету, которая исключает употребление в большом количестве продуктов питания, богатых кальцием и витамином Д. К таким относят рыбу жирных сортов, листовую зелень, молочные продукты, яичный желток, орехи.
При неэффективности консервативных методов лечения, а также образовании конгломератов больших размеров назначается их оперативное удаление. Выбор метода хирургического вмешательства проводится в зависимости от размеров скоплений кальция, а также их локализации.
Кальциноз в период беременности
Отложение кальция во время вынашивания ребенка чаще всего диагностируется в конце третьего триместра гестационного периода. С медицинской точки зрения такой процесс допустим и связан с видоизменением плаценты.
Если кальцификация диагностируется на более ранних сроках, это может привести к преждевременному созреванию плаценты. Как правило, кальциноз у беременных связан с употреблением большого количества продуктов, богатых кальцием, инфекционными процессами и метаболическими нарушениями.
Избыток макроэлемента в организме беременной женщины также опасен, как и его недостаток. Может стать причиной травм ребенка и матери в период родоразрешения.
Профилактика
Чтобы предупредить кальцификацию мягких тканей и внутренних органов следует особое внимание уделить правильному питанию. Важно обеспечить достаточное поступление всех минералов и витаминов в организм, чтобы предупредить развитие патологий различной этиологии.
Также людям с врожденными и приобретенными заболеваниями сердечно-сосудистой системы, почек, эндокринными патологиями важно регулярно проходить плановые осмотры у специалистов, что поможет своевременно предупредить развитие осложнений.
Лечение различных заболеваний стоит проводить только под контролем специалиста и в соответствии с его рекомендациями. Некоторые группы лекарственных препаратов, в том числе для снижения уровня холестерина в крови, артериального давления, а также антибактериальные и гормональные средства могут привести к повышению уровня кальция в организме и нарушению его обмена.
Для предупреждения кальциноза следует вести активный образ жизни, который помогает восстановить нормальный метаболизм, отказаться от употребления алкогольных напитков и табакокурения.
Кальцификация тканей – патологический процесс, связанный с высокой концентрацией кальция в организме. Поражает сердечно-сосудистую, нервную, опорно-двигательную, пищеварительную и мочевыделительную системы. Для предупреждения болезни необходимо правильно питаться и вести здоровый образ жизни. В качестве терапии назначается курс медикаментозных препаратов для устранения причины патологического процесса и нормализации уровня кальция и магния в крови.
Эксперт статьи:
Татаринов Олег Петрович
Врач высшей категории, врач невролог, физиотерапевт, специалист УВТ, ведущий специалист сети «Здоровье Плюс»
Медицинский опыт более 40 лет
Кальциноз: что это такое, как лечить?
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Что значит кальциноз? Это образование скоплений нерастворимых кальциевых солей там, где их наличие не предусмотрено ни с анатомической точки зрения, ни с физиологической, то есть вне костей.
Среди всех биогенных макроэлементов человеческого организма доля кальция – в форме кристаллов гидроксилапатита костной ткани – самая значительная, хотя кровь, клеточные мембраны и внеклеточная жидкость тоже содержат кальций.
И если уровень данного химического элемента значительно повышен, то развивается кальциноз – нарушение минерального обмена (код Е83 по МКБ-10).

Код по МКБ-10
Причины кальциноза
Метаболизм кальция – многоступенчатый биохимический процесс, и на сегодняшний день ключевые причины кальциноза, как одной из разновидностей нарушения минерального обмена, определены и систематизированы. Но, с учетом тесной взаимосвязи всех протекающих в организме обменных процессов, в клинической эндокринологии принято одновременно рассматривать и патогенез отложения кальцинатов (или кальцификатов).
Первостепенной причиной известковой дистрофии признана перенасыщенность крови кальцием – гиперкальциемия, этиологию которой связывают с повышенным остеолизом (разрушением костной ткани) и высвобождением кальция из костного матрикса.
Из-за гиперкальциемии, а также гипертиреоза или патологий паращитовидных желез сокращается выработка щитовидной железой кальцитонина, который регулирует содержание кальция, угнетая его выведение из костей. Предполагается, что именно наличие скрытых проблем со щитовидной железой у женщин в период постменопаузы – в совокупности со снижением уровня эстрогенов, удерживающих кальций в костях – появляются внекостные кальциевые отложения, то есть развивается кальциноз при остеопорозе.
Есть и другие патологические состояния, которые заставляют кальциевые соли концентрироваться в неположенных местах. Так, у пациентов с первичным гиперпаратиреозом, гиперплазией паращитовидных желез или их гормонально активной опухолью синтез паратиреоидного гормона (паратгормона или ПТГ) возрастает, в результате чего подавляется действие кальцитонина, а уровень кальция в плазме крови, как и деминерализация костей, повышается.
Необходимо учитывать важность фосфора в метаболизме кальция, потому что нарушение пропорций содержания этих макроэлементов в организме ведет к гиперфосфатемии, которая усиливает образование «залежей кальция» и в кости, и в мягких тканях, и в кровеносных сосудах. А перенасыщение кальциевыми солями паренхимы почек приводит к почечной недостаточности и развитию нефрокальциноза.
Механизм повышенного остеолиза с выходом фосфата и карбоната кальция из костных депо при наличии раковых опухолей любой локализации объясняют так называемым паранеопластическим синдромом: рост злокачественных неоплазий сопровождается гиперкальциемией, так как мутировавшие клетки способны продуцировать полипептид, по действию подобный паратгормону.
Общеизвестно, что патогенез образования кальциевых солей может быть обусловлен избытком витамина D, с которым в эндокринологии связывают увеличение синтеза 1,25-дигидрокси-витамина D3 – кальцитриола, активно участвующего процессе метаболизма кальция и фосфора. Причастны к развитию известковой дистрофии гипервитаминоз витамина А, приводящий к остеопорозу, а также дефицит поступающего с пищей витамина K1 и эндогенного витамина K2.
При отсутствии эндокринных патологий содержание в плазме крови общего кальция не выходит за пределы физиологической нормы, и тогда причины кальциноза иные, обусловленные местными факторами. В их числе осаждение фосфата кальция на мембранах органоидов поврежденных, атрофированных, ишемизированных или погибших клеток, а также повышение уровня рН жидкости межклеточного пространства из-за активизации щелочных гидролитических ферментов.
Например, процесс обызвествления в случае атеросклероза сосудов представляется так. Когда осевший на стенке сосуда холестерин покрывается оболочкой, формирующейся из гликопротеиновых соединений эндотелия, образуется холестериновая бляшка. И это классический атеросклероз. Когда же ткани оболочки атероматозной бляшки начинают «пропитываться» солями кальция и затвердевают, это уже атерокальциноз.
Далеко не последнее место в этиологии нарушения кальциевого обмена отводится сдвигу водородного показателя кислотности крови (pH) в щелочную сторону при частичной дисфункции физико-химической буферной системы крови (бикарбонатной и фосфатной), поддерживающей кислотно-щелочное равновесие. Одной из причин его нарушения, приводящего к алкалозу, признан синдром Бернетта, который развивается у тех, кто употребляет много содержащих кальций продуктов, принимая от изжоги или гастрита пищевую соду или нейтрализующие кислоту желудочного сока антациды, адсорбирующиеся в ЖКТ.
Считается, что любое из названных выше эндокринных нарушений усугубляет чрезмерное поступление кальция с пищевыми продуктами. Однако, как утверждают исследователи Harvard University, до сих пор нет веских подтверждений того, что кальций пищи повышает вероятность кальцификации тканей, поскольку не вызывает стойкого повышения уровня Са в крови.

«Старческий» порок сердца: истина и мифы
Что скрывается за диагнозом «атеросклеротический стеноз устья аорты»? Каков механизм развития аортального стеноза? Есть ли разница в лечебной тактике в России и за рубежом? Рисунок 1 Многим терапевтам и кардиологам
Что скрывается за диагнозом «атеросклеротический стеноз устья аорты»?
Каков механизм развития аортального стеноза?
Есть ли разница в лечебной тактике в России и за рубежом?
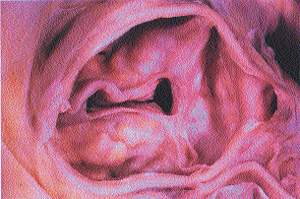 |
| Рисунок 1 |
Многим терапевтам и кардиологам хорошо известен такой нередко встречающийся клинический феномен: у пожилого человека без ревматического анамнеза при выслушивании сердца определяется грубый систолический шум над аортальными точками. Зачастую его практически никак не трактуют и в диагнозе не отражают. Но иногда в попытке объяснить подобную аускультативную картину врач все же выносит примерно такой вердикт: «атеросклеротический стеноз устья аорты». Но нельзя забывать, что диагноз — это формула для лечения, и от того, насколько правильно он будет сформулирован, во многом зависит дальнейшая тактика. Это касается любого диагноза, и данного — в частности. Именно поэтому следует серьезно разобраться не только и не столько в правомочности термина «атеросклеротический стеноз», сколько в том, что же в действительности скрывает за собой «неревматический» систолический шум на основании сердца.
В СССР традиционно рассматривались три основные причины приобретенного аортального стеноза: 1) ревматизм, 2) инфекционный эндокардит и 3) атеросклероз. Именно эта триада, и, как правило, именно в таком порядке перекочевывала из руководства в руководство, из одного учебника в другой до середины настоящего десятилетия, тогда как другим предпосылкам отводилось место в графе «и прочие». Большинство авторов после описания ревматического и «септического» эндокардитов в той или иной форме упоминают атеросклероз, который обычно в преклонном возрасте может привести к формированию кальцинированного стеноза аортального клапана [1].
Между тем за рубежом уже более 30 лет придерживаются иной точки зрения. Она последовательно рассматривается в англоязычных источниках, вышедших в свет в 60-е, 70-е и 80-е годы, и последнее десятилетие исключением не является. Согласно мнению западных исследователей, аортальный стеноз у взрослых может быть результатом: 1) кальцификации и дистрофических изменений нормального клапана, 2) кальцификации и фиброза врожденного двустворчатого аортального клапана или 3) ревматического поражения клапана, причем первая ситуация является наиболее частой причиной аортального стеноза [2].
Итак, налицо очевидная разница в подходах к этой проблеме в России и за рубежом. «Точкой пересечения» был и остается лишь ревматизм, тогда как отечественная и зарубежная школы «дополняют» его каждая двумя разными этиологическими формами: первая — инфекционным эндокардитом и атеросклерозом, вторая — идиопатическим кальцинозом и кальцификацией врожденного порока (чаще двустворчатого клапана). Но следует учитывать, что существуют две оговорки. Во-первых, изолированный кальциноз как трикуспидального, так и бикуспидального аортального клапана — по сути есть один и тот же процесс, наблюдающийся лишь в разных временных диапазонах. Во-вторых, инфекционный эндокардит работами современных авторов фактически исключен из списка существенных причин аортального стеноза. Таким образом, по большому счету остаются два состояния, определяющие диагностические, лечебные и методологические разночтения: атеросклероз и идиопатический кальциноз. Принципиальная разница между этими двумя патологическими состояниями станет понятна после более детального рассмотрения сенильного кальциноза устья аорты как самостоятельной нозологической формы.
В 1904 году в журнале «Архив патологической анатомии» 28-летний немецкий врач Иоганн Георг Менкеберг описал два случая стеноза устья аорты со значительным обызвествлением клапанов [3]. Он предложил рассматривать изменения в створках как дегенеративные, как результат изнашивания тканей с последующим их «склерозом» и обызвествлением. Обнаружив, по-видимому, что-то подобное тому, что изображено на рис. 1, он изобразил в своей статье деформированный клапан, в котором на фоне жировой дегенерации расположено множество известковых депозитов (рис. 2). Его правота будет подтверждена спустя много лет, что найдет отражение в самом термине «дегенеративный кальцинированный аортальный стеноз». Но в начале века статья И. Г. Менкеберга существенного резонанса не вызвала. И лишь через полтора десятка лет она станет объектом внимания и ляжет в основу жарких дискуссий, ведущихся на протяжении долгого времени. Морфогенез порока также вызвал много споров.
 |
| Рисунок 2 |
С менкеберговской гипотезой конкурировали в основном две теории: атеросклеротического поражения и поствоспалительного кальцинирования.
В нашей стране основное значение приобрела атеросклеротическая гипотеза. Считается, что детальное изучение «атеросклероза аортального клапана» в динамике развития «атеросклеротического порока» было выполнено профессором А. В. Вальтером в конце 40-х годов. Он описывал интенсивную липоидную инфильтрацию фиброзного пласта клапана на уровне замыкательной линии и на дне синусов Вальсальвы, причем отложение липоидов он наблюдал также на синусовой поверхности створок в небольших утолщениях субэндотелиального слоя. Далее имела место петрификация липоматозных очагов. Известковые массы раскалываются, что исследователь объяснял подвижностью створок, а образовавшиеся трещины заполняются плазменными белками и новыми порциями липоидов, в которых снова откладывается кальций. Раскалывание петрификатов продолжается, а вслед за этим продолжается и кальцинирование клапана. Фиброзное кольцо становится ригидным, створки твердыми и малоподвижными. Развивается аортальный стеноз [4].
Думается, в 1948 году опубликования этих данных было достаточно для обоснования атеросклеротической гипотезы, хотя критического осмысления требует даже сама идея «раскалывания» петрифицированных масс: если бы оно имело место, вероятно, в значительной степени возросла бы частота микроэмболических осложнений. Сегодня же, когда знания об атерогенезе куда более обширны, представляется возможным выдвинуть минимум два контраргумента теории А. В. Вальтера.
Черту под этими рассуждениями можно подвести выдержкой из статьи об атеросклерозе профессора Вашингтонского университета Э. Бирмана: «С атеросклерозом не следует путать локальное кальцифицирующее поражение клапана аорты, когда с возрастом происходит постепенное накопление кальция на аортальной поверхности клапана» [8].
Поствоспалительная гипотеза, распространенная в основном на Западе, предлагала искать связь кальцинирования с перенесенным когда-то инфекционным эндокардитом, или, что еще более вероятно, латентным ревмокардитом. Так, одни исследователи указывают на наличие в кальциевых конгломератах микробных агентов [9]. Другие публикуют сообщение о результатах гистологического исследования 200 обызвествленных аортальных клапанов, в 196 из которых обнаружены признаки ревматического поражения [10]. Сейчас сложно дать объективную оценку таким данным, но, вероятно, это были секционные находки у людей не столь пожилых и без выраженных известковых отложений. Именно к таким выводам приходишь, изучая мнение современных патологов, утверждающих, что у старых пациентов массивность петрификации всегда маскирует признаки, быть может, когда-то перенесенного ревматического эндокардита.
Однако наметившийся в первой половине века подход привел к формированию двух бытующих теперь за рубежом взглядов. Один из них предполагает, что ревматический вальвулит, даже не оставив стойких гранулематозных повреждений, делает клапан более ранимым в будущем, в значительной степени повышая риск структурной дегенерации [11] и позволяя рассматривать сенильный аортальный стеноз действительно как «дегенеративный», тогда как имеет место поствоспалительная дистрофия, постревматическая дегенерация; при этом перенесенное воспаление как бы детерминирует соединительнотканную деструктуризацию створок в пожилом и старческом возрасте, оказываясь своего рода предиктором кальцинирования клапанного аппарата аорты. Согласно другому взгляду, старческий кальцинированный стеноз является не столько результатом инфекционного эндокардита, сколько сам по себе может вызываться персистирующим в аортальных створках инфекционным возбудителем [12], то есть речь вообще идет о совершенно самостоятельной нозологической форме.
О своеобразности разбираемой патологии свидетельствует также и то, что все чаще появляются публикации об обнаружении в обызвествленных створках аортального клапана различных клеток костной ткани и даже элементов красного костного мозга [13].
Напоминание хорошо известных признаков аортального стеноза врачебной аудитории в данном случае не случайно. Дело в том, что у пожилых и старых пациентов доктора зачастую склонны объяснять наличие тех или иных жалоб скорее ишемической болезнью или общими инволютивными процессами в организме, нежели сформировавшимся «старческим» пороком сердца. Поэтому — коротко об основных особенностях этого заболевания.
 |
| Рисунок 3 |
Аортальный стеноз — один из самых длительно компенсируемых пороков из-за гипертрофии миокарда, столь сильно выраженной, как можно встретить при других заболеваниях сердца (рис. 3). В связи с этим значительно возрастает конечное диастолическое давление в левом желудочке, его наполнение (особенно при физической нагрузке и в условиях тахикардии) затрудняется, что постепенно приводит к повышению давления заклинивания легочной артерии. Развивающаяся при этом одышка, таким образом, на первых порах оказывается следствием первичной диастолической дисфункции левого желудочка, а в период декомпенсации — и систолической дисфункции. С повышенным тонусом миокарда в диастолу связано и нарушение его оксигенации. В то время как увеличение массы левого желудочка усиливает потребность миокарда в кислороде, сдавленные коронарные артерии удовлетворить ее не могут. Отсюда столь типичные для этой категории больных стенокардические боли. При этом, хотя стенокардия возникает у 70% больных с аортальным стенозом, лишь у половины из них имеется коронарный атеросклероз [2]. Третья частая жалоба — обмороки — является следствием снижения сердечного выброса, развивающегося в результате, с одной стороны, уменьшения диастолического наполнения желудочка, с другой — возрастающего градиента давления на уровне аортального клапана [14]. Эквивалентами синкопального состояния могут служить головокружения.
Среди осложнений сенильного стеноза следует отметить эмболии крошащимися известковыми массами (чаще всего коронарных, почечных и церебральных артерий), плохо переносимые и прогностически неблагоприятные аритмии (связанные как с ишемической миокардиопатией, так и с увеличением и дисфункцией левого предсердия) и изредка развивающиеся желудочно-кишечные кровотечения, связанные с ангиодисплазией правых отделов толстой кишки. При этом риск инфекционного эндокардита кальцинированных клапанов снижается в сравнении с изолированными аортальными стенозами ревматической этиологии.
При осмотре редко можно обнаружить что-то специфическое для дегенеративного стеноза у пожилых больных. В отличие от молодых пациентов, имеющих нередко «медленный и малый» пульс, у них даже при тяжелом стенозе в силу снижения эластичности артерий пульс может оставаться нормальным. Пальпаторно длительный приподнимающийся верхушечный толчок определяется в V межреберье несколько кнаружи от среднеключичной линии; нередко может пальпироваться систолическое дрожание. При аускультации первый тон может не изменяться, но в силу функционально-гемодинамических изменений нередко наблюдается его
 |
| Рисунок 4 |
ослабление. При этом второй тон, как правило, меняется, что особенно отчетливо фиксируется при длительном наблюдении за пациентом: пока кальциноз клапана не привел к стенозу, второй тон усилен (при этом в точке Боткина вслед за первым тоном иногда выслушивается систолический тон изгнания), затем из-за уменьшения подвижности створок ослаблен. Для аортального стеноза характерен грубый веретенообразный систолический шум, максимально выслушивающийся у левого края грудины и проводящийся на сонные артерии. При сенильном поражении этот шум имеет некоторые патогенетические особенности (рис. 4). Как видно из схемы, ревматический кальцинированный порок создает при систолическом изгнании гемодинамический эффект «струи», рождающий одни аускультативные феномены, а изолированный кальцинированный стеноз — эффект «спрея» с несколько другими гемодинамикой и нюансами выслушиваемой картины [15]. Так, при выраженной петрификации возникает симптом Галлавардена: высокочастотные компоненты шума проводятся в подмышечную область, имитируя шум митральной регургитации.
В диагностике клиницисту помогут рутинные инструментальные методики: ЭКГ (признаки гипертрофии и нарушения кровоснабжения миокарда левого желудочка, аритмии), рентгенография (кальциноз аортального клапана, изменение конфигурации сердца, признаки застоя в легких) и, конечно, ЭхоКГ (характер изменений в створках клапана, точная оценка степени стеноза и гипертрофии миокарда, измерение показаний внутрисердечной гемодинамики, нарушение локальной сократимости, фракция выброса, градиент давления между аортой и левым желудочком).
Лабораторные показатели, как правило, малоспецифичны и отражают экстракардиальную патологию.
Прогноз при изолированном дегенеративном аортальном стенозе определяется степенью сужения отверстия аортального клапана (см. табл.), но в целом, как правило, благоприятен. Это определяется длительной компенсацией с бессимптомным течением и медленной прогрессией из-за отсутствия комиссуральных сращений, как при ревматическом пороке. При этом следует помнить, что при появлении симптомов летальность и риск осложнений резко возрастает, а 15-20% больных умирают внезапно.
В России изучения этой нозологии как таковой не проводилось, а значит, практикующий врач не ориентирован на соответствующий диагностический поиск. При этом довольно редкое установление диагноза «атеросклеротический стеноз устья аорты» из-за непонимания истинной природы порока приводит к тому, что больному чаще назначают диету и холестеролснижающие средства, нежели направляют на консультацию к кардиохирургу. Но подобное «патогенетическое лечение» приводит лишь к прогрессированию петрифицированного стеноза. Консервативная же симптоматическая тактика вообще у больных аортальным стенозом малоэффективна, а кальцинированным — тем более. Вазодилатирующая и инотропная терапия требует большой осторожности, а назначения нитратов и диуретиков следует избегать.
Скорость прогрессирования стеноза устья аорты
Другими словами, отказ от трактовки сенильного кальцинированного стеноза устья аорты как «атеросклеротического» подведет российских кардиологов и терапевтов к формированию совершенно определенного взгляда на лечебные перспективы у таких пациентов. Единственно эффективным во всем мире признано хирургическое лечение либо путем протезирования аортального клапана (метод с наилучшими показателями отдаленной выживаемости), либо путем баллонной вальвулопластики. Второй метод имеет целый ряд существенных недостатков: большой риск осложнений и вероятность повторной обструкции, высокая интраоперационная летальность (>6%) и смертность в течение года (25%). Между тем именно этот вариант вмешательства остается основным у пожилых пациентов за рубежом; и вообще дегенеративный кальциноз стал основной причиной хирургического лечения при изолированном аортальном стенозе (51% случаев чрескожной баллонной вальвулопластики, тогда как кальциноз бикуспидального клапана и постревматическое поражение — соответственно 40 и 8% случаев). Причем возраст прооперированных больных нередко превышает 80 лет [16].
При написании последнего параграфа автор, разумеется, отдавал себе отчет в том, что проецировать зарубежную ситуацию на российскую действительность невозможно. Нередкая соматическая «запущенность» наших пациентов и стоимость кардиохирургической операции в ближайшее время не позволяют надеяться на какие-то кардинальные изменения в этом вопросе. Настоящая статья лишь подняла геронтологическую проблему, к обсуждению которой в нашей стране не обращались уже многие годы. И дело не столько в том, что 1999 год объявлен «годом пожилого человека» — отечественные медики должны располагать современной информацией и отказаться от устаревших формулировок и несуществующих диагнозов.