Что такое параэзофагеальный лимфатический узел
Поражение легких при лимфоме
Лимфома (лимфоролиферативный процесс) — это группа онкологических процессов с поражением лимфоцитов (клеток иммунной системы), которые сопровождаются изменениями в лимфатических узлах и сосудах. При этом может происходить метастазирование — миграция злокачественных клеток в соседние органы и ткани с образованием вторичных очагов рака. Увеличенные узлы при лимфоме (> 1 см в поперечнике) — плотные и абсолютно безболезненные, поэтому выявляемость заболевания на ранней стадии сравнительно низкая. В этой статье мы расскажем, какие бывают лимфомы, о симптомах, которые должны насторожить, о визуализации патологических изменений на КТ.
Лимфома легких — что это?
Лимфатическая система легких напоминает ветвистое дерево — ее сосуды пронизывают грудную клетку по всей длине и отвечают за лимфоток. Здесь расположено 13 разновидностей лимфотических узлов, классифицируемых по 5 группам:
1.Надключичные лимфатические узлы;
2.Верхние медиальные лимфатические узлы (паратрахеальные, преваскулярные, превертебральные);
3.Аортальные лимфатические узлы;
4.Нижние медиастинальные лимфатические узлы;
5.Корневые, долевые, (суб)сегментарные лимфатические узлы.
В узлах фильтруется лимфа и происходит созревание лимфоцитов. Лимфомы возникают в лимфатических узлах.
Пораженные лимфатические узлы зачастую не видны и не пальпируются. Патологические изменения — увеличенные лимфоузлы, уплотнение ткани — хорошо видны на мультисрезовом КТ-сканировании в высоком разрешении или на МРТ. Для определения специфики новообразования (нормальный или злокачественный процесс) лечащий врач может направить пациента на гистологическое исследование. В одних ситуациях увеличение узлов является относительной нормой (после перенесенных инфекционно-воспалительных заболеваний, травм, аллергических реакций), в других указывает на онкологический процесс. В последнем случае речь может идти о лимфоме.
Поскольку лимфатическая система представляет собой обширную сеть сосудов, капилляров и полостей, то злокачественные клетки могут распространиться по всему телу, образовав множественные диссеминированные метастазы.
Диагностика лимфомы легких
Обычно медицинские специалисты отдают предпочтение МРТ, поскольку отсутствует лучевая нагрузка однако в случае с обследованием воздушной ткани легочной паренхимы, которая в норме практически не содержит жидкость, наиболее подробные результаты обследования и детализированное изображение можно получить с помощью КТ легких. Если лимфома выявлена на МРТ, и у врача есть подозрение, что раковые клетки мигрировали в костную ткань, то пациенту будет рекомендовано дополнительное обследование костей. В ходе компьютерной томографии исследуют ткани разной морфологии, попадающие в зону интереса: кости, внутренние органы, сосуды. Для диагностики последних необходимо дополнительное контрастирование.
Симптомы лимфомы лёгких
Основным симптомом, по которому проще всего заподозрить лимфому легких, является увеличение лимфоузлов, локализованных в области ключиц, шеи, средостения, между ребрами. Некоторые узлы спрятаны в самой грудной клетки и не пальпируются. В таком случае лимфома дает о себе знать только тогда, когда увеличивается в размере и начинает давить на соседние органы, что вызывает дискомфорт.
Важно понимать, что увеличение лимфоузлов не является специфическим признаком злокачественной лимфомы. Оно наблюдается после антибактериальной терапии и при любом инфекционно-воспалительном заболевании — педикулезе, ОРВИ, инфекциях ротоглотки и гортани (включая заболевания стоматологического характера), при болезни кошачьих царапин (лимфоузлы увеличиваются в ответ на повреждение кожи или укус, но не сразу, а в течение последующих 3-20 дней).
Обычно лимфоузлы, увеличенные из-за воспалений, при пальпации болят и вызывают дискомфорт. При лимфоме узлы безболезненные.
Некоторые вирусы способны менять нормальную структуру ДНК лимфоцитов таким образом, что клетки превращаются в злокачественные. Так вирус Эпштейна–Барр (ВЭБ) или ВИЧ-инфекции в анамнезе существенно повышает риск развитие лимфом.
К ранним симптомам лимфомы легких относится:
В течение первых четырех недель проявляются и другие симптомы лимфомы лёгких:
У некоторых пациентов наблюдается кожный зуд. Если лимфома сдавливает органы дыхания или происходит их поражение агрессивными раковыми клетками, возможны затрудненное дыхание, кашель, одышка.
Диагностировать лимфому самостоятельно невозможно, необходимо медицинское исследование внутренних органов и тканей лимфатической системы методом КТ или МРТ.
Лимфома легких — это рак?
Не всегда. Однако к лимфомам относятся преимущественно злокачественные новообразования лимфатической системы, которые формируются из-за бесконтрольного накопления патологически измененных лимфоцитов. Исключением могут быть индолентные лимфомы. Они не требуют лечения, однако наблюдать их тоже важно. Если при этом у пациента проявляется вышеописанная симптоматика (температура, лихорадка, боль в грудной клетке), то обследование и лечение таких лимфом должно проводиться обязательно.
Злокачественные клетки-лимфоциты обладают формой, отличной от «правильных» клеток, и представляют собой фатальный «сбой» в работе организма. У таких клеток возникают совсем другие функции – они производят огромное количество белков и токсинов, при этом не уничтожаются клетками иммунной системы как враждебные.
Лимфомы не всегда являются первичным очагом онкологии. Патологически увеличенный узел или их группа (диссеминированная или локализованная в одном месте) часто бывает следствием метастатических процессов. Это происходит в связи с тем, что лимфатический узел выполняет функцию фильтра и накапливает в себе злокачественные клетки, отделившиеся от первично пораженного органа. В таком случае важно не только выявить лимфому, но и первичный очаг. Увеличение лимфоузлов легких может указывать на рак легких, молочной железы, средостения, желудка, то есть органов, расположенных в непосредственной близости.
Уточнить диагноз относительно доброкачественного или злокачественного новообразования можно по результатам биопсии (гистологического исследования образца ткани). Также пациент сдает клинический и биохимический анализы крови.На КТ легких врачи выявляют новообразование, могут оценить его размер, распространенность увеличенных лимфоузлов, однако сделать точный вывод о разновидности опухоли без анализов не представляется возможным.
Какие бывают лимфомы?
Первично лимфомы принято делить на две большие группы:
По данным НМИЦ онкологии им. Н.Н. Блохина, в России заболеваемость неходжкинскими лимфомами в 1,5-3 раза превышает заболеваемость лимфогранулематозом.
Разница между этими лимфомами становится ясна после морфологического исследования образца ткани (биопсии). При болезни Ходжкина в пораженных лимфоузлах обнаруживаются крупные мутировавшие клетки Березовского — Штернберга — Рида. Ходжкинские лимфомы отличаются более агрессивным течением с ярко выраженной симптоматикой, но они легко поддаются лечению.
Пораженные Ходжкинской болезнью лимфоузлы чаще всего расположены над ключицами, в области шеи, подмышечных впадин, средостения.
Неходжкинские лимфомы помимо B-лимфоцитов, поражают еще и T-лимфоциты. Заболевание обычно протекает без выраженной симптоматики и тяжело лечится. Но сначала необходимо правильно определить разновидность неходжкинской лимфомы — актуальная классификация состоит из 30 наименований, включая:
4 стадии лимфомы легких
Стадии течения заболевания определяют по распространенности лимфом и объему пораженной ткани:
При этом симптомы лимфомы могут быть выраженными уже на первой стадии, а могут не ощущаться пациентом практически до четвертой.
Лимфома легких на КТ
Признаки лимфомы легких особенно выражены на четвертой стадии заболевания, когда болезнь поражает дыхательный орган. На КТ при этом будут видны увеличенные лимфоузлы, формирующие цепочки, конгломераты. При этом у пациента может также наблюдаться отек легких. Однако высокая разрешающая способность КТ позволяет выявить лимфому на ранней, первой стадии.
На КТ лимфомы, как и любые уплотнения, визуализируются сравнительно более светлым цветом. В норме воздушная легочная паренхима практически однородного темного цвета. Иногда таких уплотнений несколько и они диссеминированны. Контуры лимфомы четкие и ровные. Вокруг патологических очагов обнаруживаются участки «матового стекла».
Текст подготовил
Котов Максим Анатольевич, главный врач центра КТ «Ами», кандидат медицинских наук, доцент. Стаж 19 лет
Если вы оставили ее с 8:00 до 22:00, мы перезвоним вам для уточнения деталей в течение 15 минут.
Если вы оставили заявку после 22:00, мы перезвоним вам после 8:00.
КАРТИРОВАНИЕ ЛИМФОУЗЛОВ ПРИ РАКЕ ЛЕГКОГО
Номенклатура лимфоузлов
В литературе опубликовано большое число работ, посвященных особенностям топографии лимфоузлов средостения и путей лимфооттока [2; 12]. В 1960 г. опубликована работа W G. Cahan [3], в которой авторы привели описание радикальной лобэктомии с удалением лимфоузлов ворот легкого и средостения. Однако четкого определения групп лимфоузлов, которое могло бы способствовать клинической регистрации метастазов, в этих работах предложено не было. Позднее вышла в свет японская версия номенклатуры лимфоузлов [9; 10], разработанная с учетом строения бронхиального дерева, данных торакоскопии и гистологического исследования лимфоузлов, удаленных при резекции легкого, и которая в 1976 г. получила одобрение Американского объединенного комитета стадирования рака и оценки результатов лечения [7]. Более того, номенклатура была включена Международным противораковым союзом (ШСС) в систему классификации злокачественных опухолей ТNМ и в 1980 г. утверждена Комитетом по исследованию хирургической номенклатуры Японского общества исследований рака легкого.
В 1983 г. опубликована карта Американского торакального общества (AТS). В ее основу положено строение главных анатомических структур и ориентиров во время выполнения медиастиноскопии [1], и позднее, в 1997 г. предложена карта C. F. Mountain [8], разработанная на основе исследования медиастинальной плевры и данных медиастиноскопии.
В 1996 г. при поддержке Международной ассоциации изучения рака легкого (IASLC) начал работу Международный комитет по стадированию рака [6]. На первом заседании комитета в Лондоне обсуждалось стадирование внутригрудных лимфатических узлов, рекомендации для последующего пересмотра системы стадирования и определение радикальной резекции.
После этого заседания во всем мире был начат сбор информации для формирования базы данных рака легкого, которую систематизировали в соответствии с рекомендациями Проекта стадирования рака легкого IASLC и на основании которой была разработана оригинальная карта; эту карту стали применять как карту лимфоузлов.
№1. Лимфоузлы верхнего средостения/ наивысшие медиастинальные лимфоузлы локализуются в области верхней трети вну-тригрудного отдела трахеи, от верхнего края подключичной артерии или верхушки легкого до точки пересечения верхнего края левой плечеголовной вены и средней линии трахеи.
№3р. Ретротрахеальные медиастинальные лимфоузлы / лимфоузлы заднего средостения локализуются кзади от трахеи.
№4. Трахеобронхиальные лимфоузлы располагаются выше карины. С правой стороны они локализуются медиально по отношению к непарной вене, слева лимфоузлы располагаются в области, окруженной медиальной стенкой дуги аорты.
№5. Субаортальные лимфоузлы / лимфоузлы боталловой связки располагаются в области, прилегающей к ligamentum arte-riosum (боталлова связка). Границами являются дуга аорты и левая главная легочная артерия.
№6. Парааортальные лимфоузлы располагаются вдоль восходящей части аорты и в области боковой стенки дуги аорты, сзади отграничены блуждающим нервом.
№8. Параэзофагеальные лимфоузлы располагаются ниже бифуркационных лимфоузлов, вдоль пищевода.
№9. Лимфоузлы легочной связки локализуются в области заднего и нижнего края нижней легочной вены.
№10. Лимфоузлы ворот легкого локализуются вокруг правого и левого главных бронхов.
№11. Междолевые лимфоузлы располагаются между долевыми бронхами легких. Междолевые лимфоузлы правого легкого разделяются на две группы.
№11s. Верхние междолевые лимфоузлы располагаются в области бифуркации бронхов верхней и средней долей легкого.
№11i. Нижние междолевые лимфоузлы локализуются в области бифуркации бронхов средней и нижней долей легкого.
№12. Долевые лимфоузлы располагаются вокруг ветвей долевых бронхов и разделяются на три группы.
№12u. Верхнедолевые лимфоузлы.
№12m. Среднедолевые лимфоузлы.
№12l. Нижнедолевые лимфоузлы.
№13. Сегментарные лимфоузлы локализуются вдоль сегментарных бронхов.
№14. Субсегментарные лимфоузлы располагаются вдоль субсегментарных бронхов.
По данной классификации каждая позиция регионарных лимфоузлов обозначается соответствующим номером. Лестничные и надключичные лимфоузлы при стадировании считают экстраторакальными.
Номенклатура лимфоузлов по данным КТ
Впервые номенклатура по данным КТ разработана в 1991 г., опубликована в 1995 г. и пересмотрена в 1999 г.
В целях более точного и правильного анализа лимфоузлов средостения на КТ их локализация и группировка анатомически определяются номером группы регионарных лимфоузлов. При отграничении групп лимфоузлов от прилегающих структур и органов на срезе используют прямую линию.
Границы групп медиастинальных лимфоузлов
Группы лимфоузлов средостения
№1. Верхние (наивысшие) лимфоузлы верхнего средостения. Лимфоузлы, локализующиеся в области от верхушки легкого до уровня пересечения левой плечеголовной вены и средней линии трахеи, включая срез, содержащий уровень пересечения.
№2. Паратрахеальные лимфоузлы. Лимфоузлы, расположенные каудальнее группы №1, краниально к дуге непарной вены; центр узла локализуется между претрахеальной и ретротра-хельной линиями, исключая срез, содержащий пересечение левой плечеголовной вены, средней трахеальной линии и дуги непарной вены.
№3а. Передние медиастинальные лимфоузлы. Лимфоузлы, расположенные каудальнее группы №1, с центром, находящимся кпереди от линии, проходящей от верхней полой вены до передней стенки восходящей части аорты.
№3. Претрахеальные лимфоузлы. Лимфоузлы, расположенные каудальнее группы №1, проксимально к правой главной легочной артерии, центр узла локализуется кпереди от пара-трахеальной линии или кзади от линии передней стенки верхней полой вены и справа от левой границы аорты. Лимфоузлы, локализующиеся выше дуги аорты и слева от левой подключичной артерии и левой общей сонной артерии, классифицируют как №6, если эти узлы прилегают к группе №6.
№3р. Ретротрахеальныелимфоузлы. Лимфоузлы, расположенные каудальнее группы №1, проксимально к килю трахеи; центр узла локализуется кзади от ретротрахеальной линии, исключая узлы на срезе, содержащем главные бронхи с двух сторон.
№4. Трахеобронхиальные лимфоузлы. Лимфоузлы, расположенные каудальнее непарной вены, включая уровень, содержащий непарную вену. Центр узла локализуется между паратрахе-альной и ретротрахеальной линиями. Лимфоузлы локализуются справа от левой границы аорты и соприкасаются с трахеей слева от дуги непарной вены. (Центр узла локализуется слева от группы №4, однако узлы, четко отграниченные от трахеи, классифицируют как №5.)
№5. Субаортальные лимфоузлы. Лимфоузлы между дугой аорты и левой легочной артерией. Центр узла локализуется слева от левой границы аорты и кзади от задней стенки восходящей части аорты.
№6. Парааортальные лимфоузлы. Лимфоузлы, локализующиеся слева от восходящей части аорты и дуги аорты. Центр группы располагается кзади от передней стенки восходящей части аорты. В области, где видна задняя стенка восходящей аорты, лимфоузлы локализуются кпереди от задней стенки восходящей аорты.
№7. Бифуркационные лимфоузлы. Лимфоузлы, локализующиеся под килем трахеи. Центр узла располагается кзади от передней стенки линии главных бронхов. Лимфоузлы, прилегающие к медиастинальной поверхности главных бронхов с двух сторон или промежуточному бронху, и узлы, не локализующиеся под килем, классифицируют как №10.
№8. Параэзофагеальные лимфоузлы. Лимфоузлы, локализующиеся каудально по отношению к килю (на срезах, содержащих главные бронхи с двух сторон по отдельности), прилегающие к пищеводу, но не прилегающие к бронхам.
№9. Лимфоузлы легочной связки. Лимфоузлы, расположенные каудальнее нижних легочных вен.
В качестве стандартной хирургической операции выполняют лимфодиссекцию в объеме ND2а ^В1а-2а), в случае запущенного рака выполняют лимфодиссекцию ND2b (ND^-2b) (табл. 1-2).
Ц. Наруке
Центральный госпиталь Сайсейкай, Токио, Япония
ЛИТЕРАТУРА / REFERENCES
Материалы конгрессов и конференций
IV РОССИЙСКАЯ ОНКОЛОГИЧЕСКАЯ КОНФЕРЕНЦИЯ
РАСШИРЕННЫЕ И КОМБИНИРОВАННЫЕ ОПЕРАЦИИ ПРИ НЕМЕЛКОКЛЕТОЧНОМ РАКЕ ЛЕГКОГО
М.И. Давыдов, Б.Е. Полоцкий, А. К. Аллахвердиев, К.К. Лактионов, С.С. Герасимов, Л.А. Никуличев
ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, Москва
Регионарное метастазирование является неотъемлемой характеристикой рака легкого и отражает прогрессирование опухолевого процесса. Его закономерности изучаются в многочисленных клинических работах, однако, неоднозначность результатов во многом связана с неоднородностью сравниваемых групп, подходом к отбору больных для хирургического лечения, различием тактики оперирования и объемов выполняемых вмешательств. Именно поэтому до сих пор дискутируется вопрос о необходимости и достаточном объеме удаления регионарного лимфатического аппарата.
Сформулированная еще в 60-70 годах позиция о широком удалении клетчатки средостения с лимфатическими узлами на стороне операции (то есть выполнении расширенных операций), несмотря, казалось бы, на практическую и теоретическую очевидность, до сих пор не нашла должного места в хирургии рака легкого. В свое время применение операций такого объема ограничивалось более тяжелой их переносимостью.
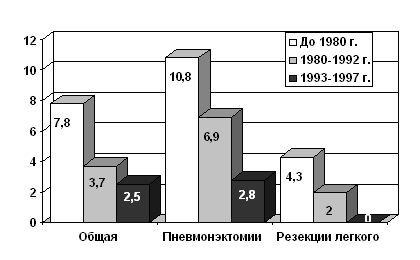
Результаты, отраженные на рис. 1, как в нашей, так и практически во всех крупных онкопульмонологических клиниках, демонстрируют значительное снижение послеопера-ционной летальности в последние годы.
Следует особо подчеркнуть, что эти показатели достигнуты на фоне расширения возрастных границ хирургического метода, и в них реализовано развитие хирургической техники, анестезиологии, реаниматологии, терапии и фармакологии. Такое положение дает основание вновь вернуться к вопросу о выполнении более широких операций, не опасаясь увеличения послеоперационной летальности.
Рис. 1. Динамика послеоперационной летальности (данные ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России)
Согласно Международной анатомической номенклатуре (1980), лимфатические узлы легкого и средостения подразделены на группы, которым соответствуют этапы регионарного метастазирования:
Отражая в целом закономерность и последовательность лимфогенного метастазирования, эта и предыдущая классификации в известном смысле схематичны, поскольку этапность и направление метастазирования нередко более многообразны, так как кроме анатомических вариантов лимфооттока возможно «повреждение» регионарных лимфатических коллекторов при ранее перенесенных или сопутствующих заболеваниях. В этих случаях, минуя первоначальные группы лимфоузлов, метастазы сразу же могут поражать последующие этапы. Все это в каждом конкретном случае представляет трудности при интраоперационной оценке распространенности опухоли.
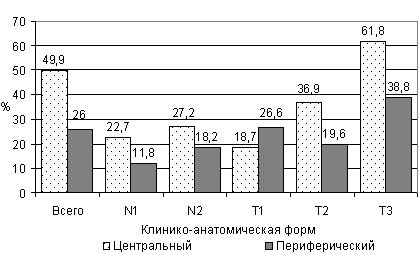
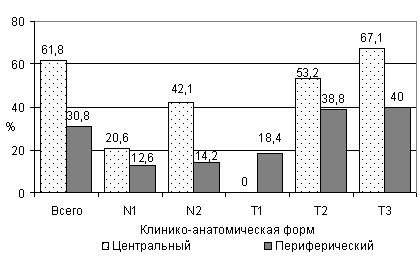
Изучение закономерностей регионарного метастазирования у 1145 больных, оперированных в Онкологическом научном центре, проводилось с учетом клинико-анатомической и гистологической формы опухоли, ее распространенности и локализации (рис. 2, 3.).
Рис.2. Регионарное лимфогенное метастазирование плоскоклеточного рака легкого.
Рис.3 Регионарное лимфогенное метастазирование аденокарциномы легкого.
Прорастание опухоли в окружающие ткани (табл. 1) связано с более частым регионарным метастазированием во всех сравниваемых группах, однако максимально и достоверно чаще оно (метастазирование) проявляется при центральном и периферическом раке с централизацией за счет поражения лимфоузлов уровня N1 и N2
Таблица 1.
Частота регионарного метастазирования рака легкого с врастанием в соседние структуры.
| Регионарное метастази- рование (N) | Централ- ьный рак | Периферич. с центра- лизацией | Периферич. без центра- лизации |
|---|---|---|---|
| абс. (%) | абс. (%) | абс. (%) | |
| N 0 | 42 (24,4) | 21 (48,8) | 48 (60,0) |
| N 1 +N 2 | 130 (75,6) | 22 (51,2) | 32 (40,0) |
Нарушение этапности метастазирования изучено у 175 и отмечено у 61 (34,9%) больных. Чаще, в 36 случаях (59,0%), метастазы отсутствовали в лимфатических узлах I этапа при поражении лимфатических коллекторов последующих, II и III, этапов. У 13 (21,2%) больных встретилось сочетанное отсутствие метастазов в лимфоузлах II этапа при поражении I и III этапов.
Нарушение этапности в зависимости от распада опухоли и обструктивного пневмонита достоверно различается: последнее осложнение чаще сочеталось с таким нарушением.
Оказалось, что ни рентгенологическая, ни интраоперационная пальпаторная оценка лимфоузлов как метастатических не является достоверной. В рентгенологически увеличенных лимфатических узлах метастазы подтверждены морфологически только в 56% случаев при поражении корня легкого и в 48,4% случаев при поражении средостения. В 28,8% случаев в рентгенологически не увеличенных лимфатических узлах при гистологическом исследовании выявлены метастазы рака.
В определяемых интраоперационно лимфатических узлах метастазы были гистологически доказаны только в 50% случаев в корне легкого и в 37% случаев в средостении.
Анализ частоты метастазирования в регионарные лимфатические узлы в зависимости от объема их удаления (табл.2) показал, что при выполнении так называемых типичных операций с удалением бронхопульмональных, корневых, верхних и нижних (бифуркационных) трахеобронхиальных узлов метастазы в них обнаружены при последующем гистологическом исследовании у 26,4% больных. При расширенных операциях, выполненных по принципиальным соображениям, метастазы во внутригрудные лимфоузлы выявлены у 39,2% больных (р A
Рис. 4. 5-летняя выживаемость после радикальных расширенных и стандартных опе-раций при раке легкого (данные ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России).
Разбираемый объем медиастинальной лимфодиссекции традиционно осуществлялся из бокового доступа. Очевидно, что правосторонняя локализация опухоли, в силу анатомических особенностей, позволяет выполнить ее более полноценно. В то же время при таком доступе и правосторонней локализации процесса, не говоря уже о левостороннем расположении опухоли, практически не удается полноценно удалить лимфатические узлы и клетчатку контралатеральной стороны и выше левого плечеголовного венозного ствола. Именно поэтому сегодня нас такой объем вмешательства уже не удовлетворяет, и актуальным является изучение возможностей билатеральной медиастинальной и шейно-надключичной лимфодиссекции с использованием для этого полной продольной стернотомии.
Признанными лидерами в разработке этих операций являются японские хирурги, которые обосновывают свою точку зрения 20-30%-ным поражением метастазами контралатеральных лимфатических узлов, особенно при левосторонней локализации опухоли.
Наш опыт таких операций (14), выполненных у больных центральным раком, производит благоприятное впечатление: удается полноценно удалить клетчатку средостения, надключичных и нижне-шейных областей.
Комбинированные и расширенно-комбинированные операции также выполняются в силу необходимости из-за большой распространенности опухолевого процесса. Анализируя результаты этих операций, следует отчетливо понимать, что значительную их часть выполняют при опухолях, не истинно прорастающих в соседние органы, а интимно к ним предлежащих, так как во время вмешательства оценить достоверно инвазию зачастую трудно. Наиболее типичным примером этого является резекция перикарда в тех случаях, когда обработать сосуды корня легкого экстраперикардиально технически сложно или невозможно, и приходится их перевязывать интраперикардиально. Аналогичная ситуация складывается при резекции париетальной плевры, когда в целях соблюдения радикализма выполняется экстраплевральное выделение предлежащей к ней опухоли и тому подобное. Такого рода операции, являясь, с хирургической точки зрения, комбинированными, принципиально по своему биологическому смыслу отличаются от вмешательств, выполняемых при истинном врастании в соседние органы. Именно поэтому их онкологические результаты следует анализировать раздельно, и основой этого является, прежде всего, полноценное морфологическое исследование.
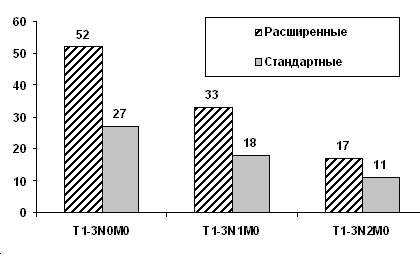
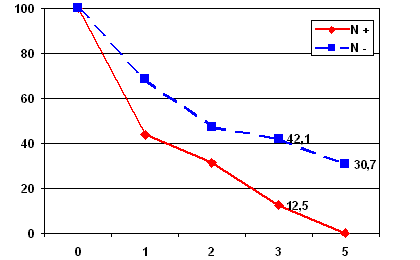
Анализ результатов радикального хирургического лечения больных с истинным прорастанием в соседние органы показал, что в целом они малоудовлетворительны: менее трети (28,3%) больных переживают 3 года, и единичные (8,3%) пациенты живут более 5 лет.
Рис. 5. Выживаемость после расширенно-комбинированных операций в зависимости от метастатического поражения внутригрудных лимфоузлов
Таким образом, мы считаем, что современные знания внутригрудной лимфодинамики и логика радикального хирургического лечения заставляют сегодня пересмотреть терминологию и унифицировать хирургические вмешательства. На наш взгляд, современная операция при раке легкого, независимо от локализации опухоли в органе, должна сопровождаться широким вскрытием средостения (медиастинальной плевры) и полным удалением клетчатки с лимфатическими узлами независимо от визуальной их оценки как интактных. Только такой подход позволяет обеспечить максимально возможный радикализм, объективизировать внутригрудную распространенность опухоли и может считаться базовым для разработки и оценки любых вариантов комбинированного лечения. По сути, такого рода операции сегодня следует расценивать как стандартные.