Ээг при сдвг что показывает у детей
Анализ ЭЭГ ребёнка помогает при диагностике СДВГ
На сегодняшний день с постановкой диагноза при СДВГ ( Синдром дефицита внимания и гиперактивности) существуют определённые сложности. Имеющиеся методики основаны в основном на субъективной оценке специалистов. Среди методик можно упомянуть и структурированный опросник родителей ребёнка, критерии гиперактивности психологов П. Бейкера и М. Алворда и т. д. Однако теперь появилась возможность сделать постановку диагноза более точной — с помощью ЭЭГ ( Электроэнцефалограммы).
В США был одобрен новый тест мозговых волн, измеряемых электроэнцефалограммой ( ЭЭГ) для диагностики синдрома дефицита внимания и гиперактивности ( СДВГ). FDA ( Food and Drug Administration) — агентство Министерства здравоохранения и социальных служб США — дало разрешение на использование системы NEBA. Данная система позволяет более точно поставить диагноз.
Как же работает такая методика? ЭЭГ ведет запись электрических импульсов, которые производят нервные клетки головного мозга. Прибор измеряет частоту импульсов в секунду в течение 20-ти минут, Он рассчитывает соотношение бета и тета ритмов, которые, согласно исследованиям выше у детей и подростков с СДВГ. В качестве доказательства эффективности, NEBA провело клиническое исследование 275 пациентов, в возрасте от 6 до 17 лет. Дети и подростки подверглись диагностике на приборе, а независимая группа экспертов по результатам ряда обследований подтвердило наличие у пациентов СДВГ или другого расстройства.
Однако, новый метод подвергли критике американские неврологи, отметив недостаточное количество исследований ЭЭГ при СДВГ. Неврологи отмечают, что подобные изменения ритмов на энцефалограмме могут появляться вследствие тревоги, депрессии или медикаментозного лечения. Таким образом, ЭЭГ можно пока использовать лишь как вспомогательное средство диагностики синдрома дефицита внимания и гиперактивности.
Анализ ЭЭГ ребёнка помогает при диагностике СДВГ
На сегодняшний день с постановкой диагноза при СДВГ ( Синдром дефицита внимания и гиперактивности) существуют определённые сложности. Имеющиеся методики основаны в основном на субъективной оценке специалистов. Среди методик можно упомянуть и структурированный опросник родителей ребёнка, критерии гиперактивности психологов П. Бейкера и М. Алворда и т. д. Однако теперь появилась возможность сделать постановку диагноза более точной — с помощью ЭЭГ ( Электроэнцефалограммы).
В США был одобрен новый тест мозговых волн, измеряемых электроэнцефалограммой ( ЭЭГ) для диагностики синдрома дефицита внимания и гиперактивности ( СДВГ). FDA ( Food and Drug Administration) — агентство Министерства здравоохранения и социальных служб США — дало разрешение на использование системы NEBA. Данная система позволяет более точно поставить диагноз.
Как же работает такая методика? ЭЭГ ведет запись электрических импульсов, которые производят нервные клетки головного мозга. Прибор измеряет частоту импульсов в секунду в течение 20-ти минут, Он рассчитывает соотношение бета и тета ритмов, которые, согласно исследованиям выше у детей и подростков с СДВГ. В качестве доказательства эффективности, NEBA провело клиническое исследование 275 пациентов, в возрасте от 6 до 17 лет. Дети и подростки подверглись диагностике на приборе, а независимая группа экспертов по результатам ряда обследований подтвердило наличие у пациентов СДВГ или другого расстройства.
Однако, новый метод подвергли критике американские неврологи, отметив недостаточное количество исследований ЭЭГ при СДВГ. Неврологи отмечают, что подобные изменения ритмов на энцефалограмме могут появляться вследствие тревоги, депрессии или медикаментозного лечения. Таким образом, ЭЭГ можно пока использовать лишь как вспомогательное средство диагностики синдрома дефицита внимания и гиперактивности.
Ээг при сдвг что показывает у детей
Однако специальные психологические и инструментальные методы диагностики позволяют уточнить диагноз и оценить выраженность проявлений данного расстройства.
Среди наиболее доступных непсихологических методов исследования головного мозга следует выделить ЭЭГ (электроэнцефалографию), в том числе:
Не электроэнцефалографические методы диагностики:
Клиническая ЭЭГ
Это распространенное исследование головного мозга, при котором изучается его состояние, отраженное в производимой живым мозгом биоэлектрической активности. Изучается, как работает мозг, какую электрическую активность он имеет в обычных, стандартных условиях (в спокойном состоянии с закрытыми глазами).
Обычно у детей с признаками СДВГ не выявляется существенных нарушений в работе головного мозга, что, в частности, и позволило отнести это расстройство к так называемым минимальным мозговым дисфункциям.
ЭЭГ пробы с интеллектуальной нагрузкой
В обычном ЭЭГ исследовании не учитывается то, как мозг реагирует на различного рода интеллектуальную нагрузку, которая встречается, например, при выполнении учебных заданий. Неуспеваемость детей с СДВГ по различным школьным предметам, требующим активного внимания, связана с нарушениями в работе мозга, которые определяются в частности при проведении подобных нагрузочных проб.
Например, при чтении и осмысливании читаемого текста, прослушивании или переписывании текста, письме под диктовку, мозг ребенка с СДВГ может быть недостаточно «настроен» на работу, тем более, если работа рутинная или не интересная. Подобные изменения в работе мозга связаны в основном с выраженностью определенного рода биоэлектрической активности, так называемой медленно-волновой активностью мозга.
Изучая соотношение между медленно-волновой и быстро-волновой активностью (коэффициента дефицита внимания-КДВ) в специально выбранной точке мы сравниваем полученный результат с базой данных, где показаны средние значения этого показателя у детей разного возраста.
Если КДВ превышает среднее значение на определенную статистически значимую величину, мы делаем вывод о высокой вероятности диагноза СДВГ у этого ребенка и о необходимости применения нейротерапевтической коррекции, по методу ЭЭГ-БОС.
ЭЭГ исследования Вызванных Потенциалов головного мозга (ВП)
Кроме обычной электрической активности ЭЭГ, современное оборудование позволяет заметить минимальные изменения в работе мозга, которые связаны с его реакцией на внешние раздражители. Такое исследование называется исследованием Вызванных Потенциалов головного мозга (ВП), то есть особенностей ответа мозга на предъявляемые специальные видимые или слышимые стимулы. По характеру этого ответа также можно сделать вывод о степени выраженности нарушений функций головного мозга, в частности функции активного внимания.
Картирование головного мозга это дополнительная обработка имеющейся записи ЭЭГ, осуществляемая специальными компьютерными программами. Отображается карта распределения различной по степени (от минимума до максимума) выраженности того или иного вида биоэлектрической активности в коре головного мозга.
Подобная обработка ЭЭГ позволяет увидеть, как на карте, области мозга, имеющие функциональный дефицит, что также помогает в диагностировании и в выборе правильной терапевтической стратегии.
TOVA-тест – тест вариабельности внимания
Испытуемому предлагается наблюдать, как на экране, на сером фоне, появляются, сменяя друг друга, зеленые квадратики либо в верхней, либо в нижней части экрана. Задача испытуемого нажимать на кнопку мыши как можно быстрее, когда зеленый квадратик находится в верхней части экрана. С помощью этого теста определяется скорость реакции, количество ошибок по невнимательности (пропуски), ошибки по причине импульсивности (ошибочные нажатия). Полученные данные сравниваются с нормой, и определяется степень отклонения, то есть насколько выражены эти изменения.
Анализ особенностей электроэнцефалограммы у детей с синдромом нарушения внимания и гиперактивностью
М.И. Лохов, Ю.А. Фесенко, Л.П. Рубина, НИИ экспериментальной медицины РАМН
Центр восстановительного лечения «Детская психиатрия», Санкт-Петербург.
Основанием для формирования синдрома нарушения внимания с гиперактивностью (СНВГ) является минимальная дисфункция мозга (МДМ). Понятие МДМ возникло в неврологической детской практике для характеристики перинатальных поражений мозга, не приводящих к выраженным нарушениям моторики и интеллекта, но вызывающих четкие неврологические и психопатологические расстройства [1, 2]. Большинство исследователей к наиболее часто встречающимся при МДМ неврологическим симптомам относят нарушение ассоциативных движений, подергивание различных групп мышц, тремор пальцев рук, нарушения сухожильных рефлексов и координации движений, а к психопатологическим расстройствам — нарушение внимания, гиперактивность, эмоциональную лабильность, повышенную утомляемость, нарушение восприятия и образования понятий. В связи с тем что «нарушение внимания с гиперактивностью» встречаются при МДМ в 80—93%, они были выделены в отдельный синдром, заменяющий (хотя и не совсем справедливо) в настоящее время понятие МДМ.
За последние десятилетия в детской неврологической практике отмечается рост числа детей с СНВГ. В Санкт-Петербурге, по данным эпидемиологических обследований, СНВГ обнаруживается у 17,5% детей в возрасте от 4 до 11 лет [3]. В диагностическом и статистическом руководстве по психическим заболеваниям Американской ассоциации психиатров 1994 г. (DSM-IV) указанный синдром разделен на 3 вида: с преобладанием невнимательности, с преобладанием гиперактивности-импульсивности и смешанный.
С нейрофизиологической точки зрения высказывается предположение, что в основе этиологии СНВГ лежит нарушение взаимодействия хвостатого ядра и фронтальной коры, вызванное, по-видимому, дисбалансом дофамина и норадреналина [4]. Для компенсации этого дисбаланса организм вынужден прибегать к своеобразной стимуляции коры головного мозга через двигательные центры, что и приводит к синдрому гиперактивности. Таким образом, повышенная двигательная активность служит своеобразным защитным механизмом, поддерживающим определенное функциональное взаимодействие между структурами мозга, ответственными за его нормальное развитие.
Использование при СНВГ компьютерного кросскорреляционного анализа электроэнцефалограммы (ЭЭГ) предоставляет принципиально новые возможности для определения взаимодействия структур коры головного мозга, которое может осуществляться не только непосредственно между самими участками коры, но и через подкорковые образования. Вычисление кросскорреляционной функции позволяет раскрыть механизмы и пути формирования функциональных связей между активностью разных отделов мозга.
При анализе кросскорреляции количественно определяются обычно следующие величины:
При этом по величине Ccr можно судить о степени корреляционной связи двух процессов: при значении Ccr до 0,2 — связь очень слабая; от 0,2 до 0,5 — умеренная; от 0,5 и выше — значительная; от 0,7 до 0,9 — тесная или высокая.
При t=0 процесс характеризуется синфазностью колебаний в двух отведениях ЭЭГ. При сравнении 1 и 2-го отведений t со знаком + характеризует опережение процесса в отведении 1 по сравнению с отведением 2, а t со знаком минус характеризует опережение в отведении 2 по сравнению с отведением 1.
В наших многолетних исследованиях кросскорреляционной активности в ЭЭГ у детей в норме и при развитии пограничных расстройств [5—7] использовалась монополярная регистрация с усредненным ушным электродом на компьютерной энцефалографической приставке «Телепат» с записью на жесткий носитель компьютера и последующей обработкой по специальным программам анализа, разработанным в ЛЭТИ им. А. С. Попова. Для представления полученных результатов в наглядной форме использовался известный метод проекции графов [8], отражающий динамику перемещения фокусов максимальной активности и сопряженного угнетения различных областей левого и правого полушарий головного мозга. На языке теории графов такие области обозначаются соответственно как точки истока и стока. Мы изучали наличие истоков и стоков в теменно-затылочную или нижнетеменную зону (цитоархитектонические поля 39 и 40, по Бродману) правого полушария головного мозга. Эта область коры головного мозга, по данным многих исследований [9—11], играет ведущую роль в развитии психики и интеллекта ребенка, а также имеет немаловажное значение при многих психических нарушениях во взрослом возрасте [12, 13]. Достаточно сказать, что характерные профили психотропных фармакологических препаратов строятся именно по отношению к правой теменно-затылочной области коры головного мозга [14].
В нашей практике из 658 детей в большинстве случаев (70%) встречался именно смешанный тип СНВГ, часто (в 30—40%) осложненный другими пограничными психическими расстройствами детского возраста (тики, заикание, энурез) [5, 6].
Рис. 1. Усредненные данные кросскорреляционного анализа ЭЭГ здоровых испытуемых детей 3—11 лет. Тонкие стрелки на графиках обозначают кросскорреляции со значением от 0,3 до 0,5, а более толстые — выше 0,5. Направление стрелок характеризует опережение в работе той структуры, откуда стрелка исходит (так называемый исток).
Рис. 2. Усредненные данные кросскорреляционного анализа ЭЭГ детей 3—11 лет, страдающих тяжелыми формами заикания (пояснения в тексте).
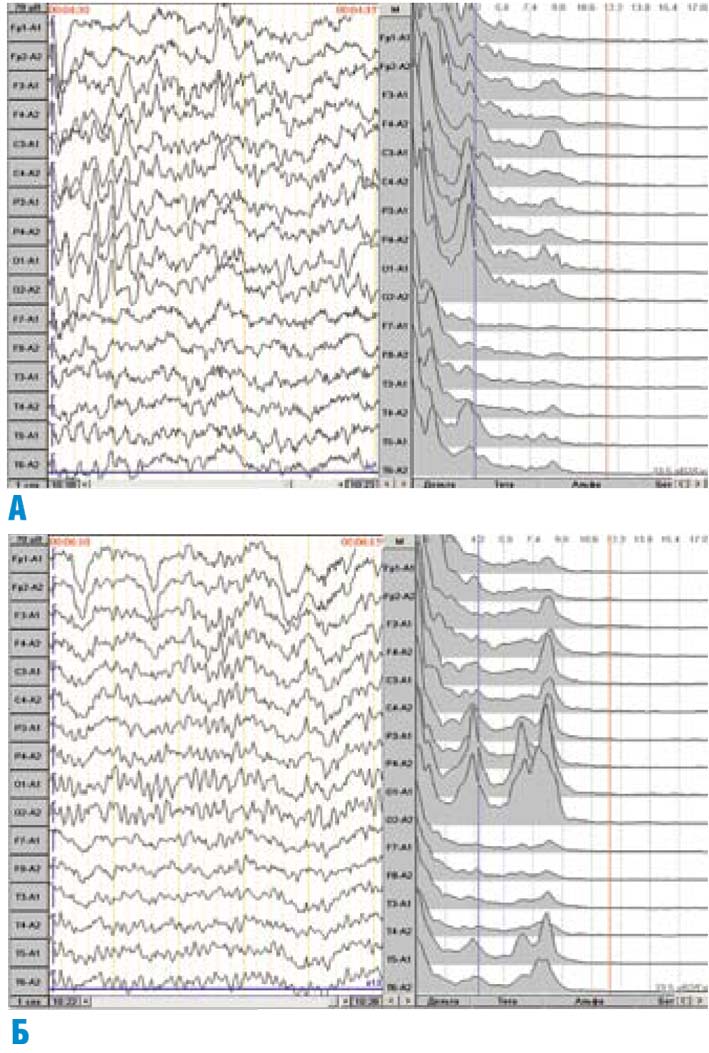
Рис. 3, а. Фрагмент компьютерного кросскорреляционного анализа фоновой записи ЭЭГ больного О., 6 лет, с СНВГ.
Рис. 3, б. Фрагмент компьютерной ЭЭГ того же больного на фоне гипервентиляции.
Предварительный диагноз: заикание, СНВГ.
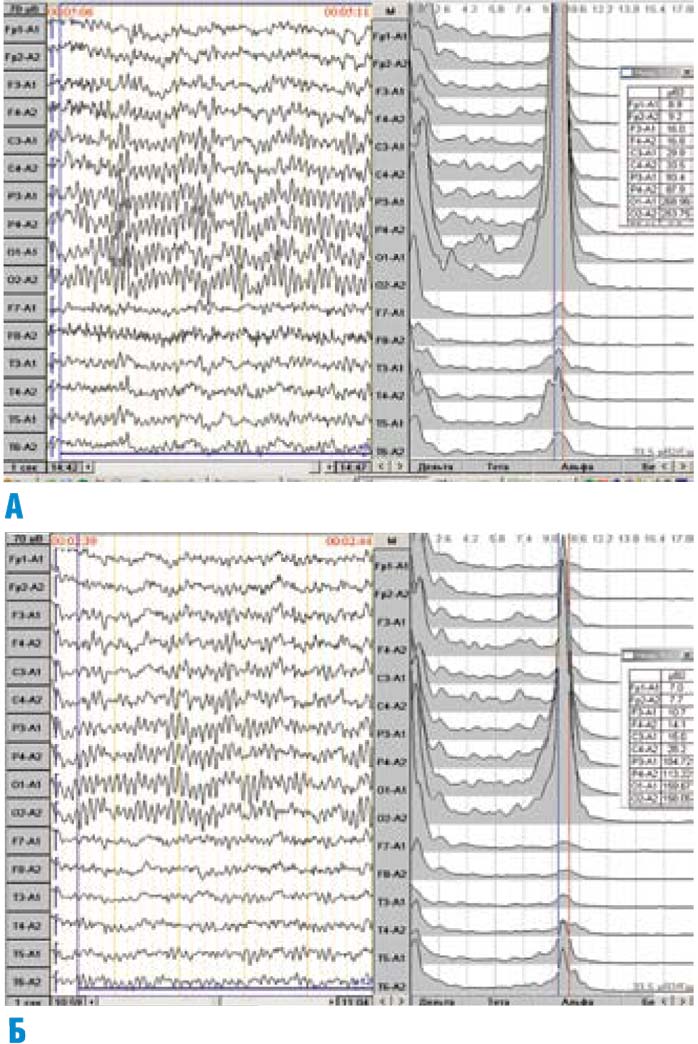
Рис. 3, в. Фрагмент компьютерного кросскорреляционного анализа ЭЭГ на фоне гипервентиляции у того же больного.
В приведенных далее результатах исследований показана динамика изменения характера кросскорреляционной активности, характеризующей взаимоотношения между различными зонами коры головного мозга в норме и при СНВГ у детей 3—11 лет, при жестко выбранной периодичности и эпохи анализа (8 с) фоновой записи ЭЭГ и во время гипервентиляции. Гипервентиляция проводилась в течение 3 мин, с максимальной глубиной вдоха и выдоха, и частотой 20 дыхательных движений в минуту.
Как видно из представленных данных (рис.1), усредненных более чем по 200 здоровым испытуемым (дети 3—11 лет), правая теменно-затылочная область в норме (3-минутная фоновая запись), начиная с 3—4-летнего возраста, являлась областью истоков, что подтверждается результатами других исследований [9—11]. При анализе, как правило, использовался диапазон частот 4—12 Гц. При динамике кросскорреляций в случае последовательного анализа фоновой записи ЭЭГ у одного здорового ребенка оказывалось, что взаимоотношения между структурами не являлись однородными. Они как бы «дышат», конкурируют между собой за лидерство на усредненной записи. В некоторых случаях обнаруживалось, что отрезки ЭЭГ меняли отношения между собой на прямо противоположные тем, которые выявлялись при статистическом усреднении записи в целом. Такой живой динамический рисунок кросскорреляций был характерен для большинства детей 3—11 лет. Стоит также заметить, что в норме большинство связей имело коэффициент корреляции выше 0,5.
Совершенно иная картина наблюдалась при анализе ЭЭГ у больных детей того же возраста с пограничными психическими расстройствами, в частности с СНВГ (рис. 2).
На рис. 3, а приведены результаты компьютерной ЭЭГ больного О., 6 лет, с СНВГ и заиканием. Приведены результаты обработки фоновой записи, т. е. записи ЭЭГ в состоянии спокойного бодрствования с закрытыми глазами. Фоновая запись отличалась от характерной для нормы лишь измененным в некоторых фрагментах направлением взаимодействия между структурами мозга. Однако во время гипервентиляции — усиленной дыхательной активности, которая в обычных условиях эквивалентна усиленному дыханию при энергичной двигательной активности ребенка — отмечалось заметное изменение этих взаимоотношений. В ответ на гипервентиляцию в ЭЭГ по прошествии первой минуты возникали генерализованные вспышки q-ритмической активности в диапазоне частоты 4 Гц (рис. 3, б), что сопровождалось временным восстановлением полноценных кросскорреляционных связей теменно-затылочной зоны правого полушария с другими областями головного мозга (рис. 3, в).
Таким образом, можно предположить, что гиперактивность является своего рода защитным механизмом, временно восстанавливающим нормальные связи в коре головного мозга и тем самым сохраняющим нормальное интеллектуальное развитие ребенка.
Проведенное нами исследование обнаружило, что наблюдаемые изменения не характерны для других моносимптоматических пограничных расстройств детского возраста.
Итак, ЭЭГ у детей с СНВГ имеет ряд особенностей, которые отличают ее от характерной для нормы или детей с другими моносимптоматическими пограничными психическими расстройствами.
Полученные данные позволяют говорить о более слабом контроле со стороны ретикулярной формации ствола мозга за неспецифическими таламическими структурами и о ведущей роли этих структур в синхронизации взаимодействия между различными образованиями головного мозга, участвующих в процессах памяти и обеспечивающих интеллектуальную сохранность больного СНВГ.
Литература:
Журнал «Обозрение психиатрии и медицинской психологии им. В.М. Бехтерева», т. 02, N2, 2005
Терапия тикозных гиперкинезов с коморбидным синдромом гиперактивности с дефицитом внимания у детей
Опубликовано в журнале:
Лечащий врач, октябрь 2013, № 9
Г. М. Джанумова*, кандидат медицинских наук
А. В. Будкевич*, кандидат медицинских наук
Г. С. Пилина**
* МБУЗ ДГКБ № 9 им. Г. Н. Сперанского, Москва
** ГБОУ ВПО Ижевская государственная медицинская академия, Ижевск Ключевые слова: дети, тикозные гиперкинезы, синдром гиперактивности с дефицитом внимания, медикаментозная терапия.
Одной из актуальных проблем детской неврологии на сегодняшний день являются тикозные гиперкинезы. Внимание специалистов к этой группе заболеваний обусловлено не только увеличением частоты встречаемости этого вида патологии, но и возрастанием доли медикаментозно резистентных форм.
В большинстве случаев тики сопровождаются коморбидными проявлениями в виде поведенческих и эмоционально-волевых расстройств, обсессивно-компульсивного синдрома, вторичного энуреза, когнитивных нарушений [1–3].
В 50% случаев тикам у детей сопутствует синдром дефицита внимания и гиперактивности (СДВГ) [1, 3–5]. Это связано с общими механизмами в патогенезе тикозных гиперкинезов и СДВГ [4–9], подтвержденными наличием характерных невротических паттернов электроэнцефалограммы (ЭЭГ) по данным спектрально-когерентного анализа [10–13]. Электроэнцефалографическая картина тикозных расстройств и СДВГ характеризуется многообразными вариантами отклонений от нормы, но общим для них является изменение основного ритма (от умеренной дезорганизации до выраженной дизритмии), что обуславливает использование идентичных методов лечения данных нозологий.
Лечение тиков, а также сопутствующих им коморбидных состояний представляет собой длительный процесс. В терапии тикозных расстройств применяется большой спектр различных методов лечения: режимные мероприятия, психотерапия, физиотерапия, немедикаментозные методы, разнообразная медикаментозная терапия. Предлагается применение метода биологической обратной связи, аудиовизуальная стимуляция, транскраниальная электростимуляция, транскраниальная микрополяризация. За последние годы разработана эффективная медикаментозная терапия тикозных гиперкинезов, но и она имеет определенные недостатки. Использование нейролептиков, антиконвульсанотов и транквилизаторов не решило проблемы лечения тиков. При их назначении очень часто наступают ранние осложнения в виде синдрома паркинсонизма, дистонических и дискинетических нарушений, психомоторного возбуждения, а также усиление симптомов дефицита внимания при наличии сопутствующего СДВГ. У больных с преходящими тиками лучше ограничиться препаратами гамма-аминомасляной кислоты (ГАМК). При лечении тиков и синдрома дефицита внимания используется Пантогам [3], высокая терапевтическая эффективность локальных и распространенных тиков, а также синдрома дефицита внимания была отмечена при применении препарата Тенотен детский, также реализующего свое регулирующее влияние на центральную нервную систему через ГАМК [4, 7, 14].
Фармакотерапия СДВГ отличается большим разнообразием. Отечественными специалистами при лечении СДВГ широко используют препараты ноотропного ряда, применение которых при СДВГ патогенетически обосновано, поскольку ноотропные препараты оказывают стимулирующее действие на недостаточно сформированные у детей этой группы когнитивные функции (внимания, памяти, организации, программирования и контроля психической деятельности, речи, праксиса). Однако часто стимулирующее действие ноотропов может давать побочный эффект в виде усиления гиперактивности, что требует назначения в комплексе с ноотропами седативных препаратов. В связи с разнообразием коморбидных состояний, сопровождающих тики, а также наличием сопутствующего СДВГ в лечении следует предпочитать препараты, оказывающие поливалентное действие с минимальными побочными эффектами, при этом соблюдая правило монотерапии [9]. Таким требованиям соответствует Тенотен детский, который оказывает сбалансированное анксиолитическое и ноотропное действие, а также отличается отсутствием побочных эффектов. Препарат содержит релизактивные антитела к мозгоспецифическому белку S-100, который оказывает регулирующее влияние на базовые функции нервных клеток (проведение нервного импульса, деление и рост нейронов и их энергетический обмен).
Целью настоящего исследования была оценка клинической эффективности применения Тенотена детского в лечении детей с тикозными гиперкинезами (транзиторными тиками, хроническими моторными или вокальными тиками) с сопутствующим синдромом гиперактивности и дефицитом внимания.
Материалы и методы исследования
На базе консультативно-диагностического центра MБУЗ ДГКБ № 9 им. Г. Н. Сперанского (Москва) у 120 детей в возрасте от 3 до 15 лет (31 девочка и 89 мальчиков), страдающих тикозными гиперкинезами и сопутствующим СДВГ, проведено сравнительное исследование результатов терапии в следующих группах:
Группа А — 60 детей с тиками и коморбидным СДВГ, получающие препарат Тенотен детский (схема лечения — по 1 таблетке 3 раза в день), разделенная на две подгруппы по форме течения: А1 — 30 детей с транзиторными и А2 — 30 детей с хроническими моторными и вокальными тиками.
Группа В — 60 детей с тиками и коморбидным СДВГ, получающие Пантогам (схема лечения — по 1 таблетке 3 раза в день), разделенная на две подгруппы по форме течения: В1 — 30 детей с транзиторными и В2 — 30 детей с хроническими тиками.
Продолжительность терапии во всех описанных группах составила 12 недель.
Диагностика клинических проявлений СДВГ и тикозных гиперкинезов проводилась в соответствии с критериями МКБ-10 и DSM-IV (Diagnostic and Statistical Manual of mental disorders — Руководство по диагностике и статистике психических расстройств, США).
Эффективность терапии оценивалась клинически по количественному подсчету тиков за 20 минут до и после лечения с вычислением коэффициента эффективности лечения (КЭ) по методике В. П. Зыкова [4]. Низким считали КЭ в диапазоне 0–33%, умеренным — 34–67%, высоким — 68–100%.
Оценка степени тяжести сопутствующего СДВГ производилась с помощью шкалы SNAP-IV, которая представляет собой опросник для родителей, состоящий из 43 вопросов, позволяющих оценить степень невнимательности, гиперактивности и импульсивности.
Оценка уровня тревожности производилась с помощью шкалы тревожности по методике Г. П. Лаврентьевой и Т. М. Титаренко (в баллах).
Наряду с динамикой клинических проявлений изучали состояние биоэлектрической активности головного мозга методом компьютерной электроэнцефалографии (ЭЭГ) с анализом спектров мощности и когерентности по методикам, разработанным нами ранее [1, 2, 5–7]. ЭЭГ регистрировали до и после курса терапии с использованием компьютерного комплекса «Нейрокартограф» фирмы «МБН» (Москва).
Результаты и их обсуждение
Подгруппы детей с транзиторными тиками
В подгруппе А1 у детей с транзиторным тиками и коморбидным СДВГ после 2‑месячного курса терапии Тенотеном детским КЭ составил 75% и был расценен как высокий, причем у 8 детей отмечалась полная редукция тикозной симптоматики (табл. 1).
Таблица 1
Коэффициент эффективности лечения больных с хроническими тиками и СДВГ
| Коэффициент эффективности | Группа А | Группа В | ||
|---|---|---|---|---|
| А1 | А2 | B1 | B2 | |
| Высокий | * | * | ||
| Средний | * | * | ||
В контрольной подгруппе В1 у пациентов, получавших Пантогам, был также высокий КЭ (73%), и у 9 детей тики полностью нивелировались. Однако в группе детей, получавших Пантогам, в одном случае имела место аллергическая сыпь, у двоих детей нарушился сон.
В подгруппе, получавшей Тенотен детский, отмечалось более выраженное улучшение показателя невнимательности. Динамика остальных показателей СДВГ на фоне лечения в группах А1 и В1 существенно не различалась.
Уровень тревожности у детей с транзиторными тиками и СДВГ в подгруппах А1 и В1 имел следующую динамику: количество детей с низким уровнем тревожности, получавших Тенотен детский, увеличилось в 5 раз, а в подгруппе В1 лишь в 1,8 раза. Количество детей со средним уровнем тревожности в подгруппе пациентов с транзиторными тиками + СДВГ, получавших Тенотен детский, уменьшилось в 2,5 раза, а в подгруппе пациентов с транзиторными тиками + СДВГ, получавших Пантогам, уменьшилось в 1,3 раза. В процессе лечения подгруппы А1 Тенотеном детским количество детей с высоким уровнем тревожности снизилось в 3 раза, а в подгруппе В1 — не изменилось. Полученные данные свидетельствуют о более выраженном анксиолитическом эффекте Тенотена детского.
Подгруппы детей с хроническими тиками
В подгруппах А2 и В2 у больных с хроническими тиками и СДВГ КЭ в обеих группах был расценен как средний. В группе детей с тиками и СДВГ, которые получали Тенотен детский, КЭ был равен 64%, а в группе, получавшей Пантогам, КЭ составил 55% (табл. 1). В обеих группах более быстрым регрессом отличались моторные тики, однако полной редукции тиков не наблюдалось ни у одного пациента.
В подгруппе А2 после терапии Тенотеном детским отмечалось достоверное снижение показателей импульсивности и гиперактивности, а в подгруппе В2 были получены достоверные показатели снижения уровня невнимательности.
Нами было замечено, что более высокий уровень тревожности наблюдался в подгруппах А2 и В2, т. е. это дети с хроническими моторными и вокальными тиками и СДВГ. Динамика уровня тревожности также оказалась более позитивной в группе детей, получавших Тенотен детский (А2).
Также отмечено, что в подгруппе В2, получавшей Пантогам, у 1 ребенка имел место аллергический ринит, у 2 нарушение сна и у 1 ребенка отмечено усиление гиперактивности и тикозной симптоматики (к моторным тикам присоединились вокальные).
Таким образом, результаты исследования показали, что тикозные гиперкинезы, осложненные сопутствующим СДВГ, имеют свои особенности, проявляющиеся прямой зависимостью между тяжестью тикозной симптоматики, выраженностью симптомов СДВГ и уровнем тревожности. Дети с хроническими моторными и вокальными тиками имеют более тяжелое течение симптомов СДВГ и отличаются более высоким уровнем тревожности. При лечении Тенотеном детским отмечалась редукция тикозной симтоматики, уменьшение выраженности симптомов СДВГ и снижение уровня тревожности, особенно в группе детей с транзиторными тикозными гиперкинезами и сопутствующим СДВГ.
Оценка эффективности лечения по показателям электроэнцефалограммы
Анализ ЭЭГ детей с тикозными гиперкинезами и сопутствующим СДВГ показал, что биоэлектрическая активность головного мозга у них изменена с высокой степенью вариабельности. У 38% пациентов преобладали дизритмические проявления. У 8% больных отмечен средний и низкий уровень вольтажа. У 29% нарушения общемозговой ритмики были выражены меньше и выражались в виде дезогранизации основного ритма. В четверти случаев (25%) имело место изменение ритмики в виде пространственного расширения представительства альфа-ритма, включая височные отделы.
Кроме того, на ЭЭГ у 60% детей выявлялись признаки повышения активности глубинных образований в виде билатеральных вспышек тета-, альфа-подобных волн или вспышек низкочастотных бетаколебаний высокой амплитуды. У многих больных регистрировались одиночные или распространенные острые волны, которые по своему генезу не являлись эпилептическими и носили неспецифический характер. Достоверные эпилептиформные знаки с отчетливой полушарной или локальной проекционной зоной встречались в 5% случаев. Довольно часто наблюдалась односторонняя полиритмия по альфа-ритму, что на спектрограммах ЭЭГ проявлялось в виде поли- или двухмодального пика мощностных значений в альфадиапазоне. При вариантах с распространенным альфа-ритмом выделяли специальные клинически значимые варианты его распределения, такие как невротические паттерны ЭЭГ. Такие варианты ЭЭГ у детей с тикозными гиперкинезами встретились у 42% пациентов.
Проведенный спектральный анализ обнаружил значимые изменение мощностных характеристик в 76% случаев. Двухмодальный пик альфа-ритма отмечен в 26% случаях. Повышение мощности основного ритма установлено у 49% пациентов, у 26% отмечено существенное снижение относительно нормы (табл. 2).
Таблица 2
Динамика мощности доминирующего альфа-ритма до и после лечения Тенотеном детским детей с тикозными гиперкинезами и сопутствующим СДВГ (мкВ2)
| Показатели электроэнцефалограммы | Норма* M ± d ± m | До лечения M ± d ± m | После лечения M ± d ± m | Оценка достоверности | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Спектр мощности (альфа-пик) в затылочной области | Исходно сниженная мощность (26%) | 172 ± 47 ± 9,4 | 59 ± 17 ± 4,3 | 112 ± 28 ± 9,3 | p | Исходно повышенная мощность (49%) | 290 ± 56 ± 11,2 | 138 ± 46 ± 11,5 | p | В пределах нормальных значений (25%) | 141 ± 34 ± 11,3 | 159 ± 45 ± 15 | p > 0,5 |
Примечание. * Использовано нормальное значение мгновенной мощности альфа-пика (по данным В. П. Зыкова, 1999). Дополнительно к среднеквадратичному отклонению (), которое использовал автор, нами выполнено вычисление среднеквадратичной ошибки средней (m), поскольку принято именно этот параметр использовать для вычисления достоверности различий.
Состояние внутримозговой интеграции электрических процессов мозга количественно оценивалось по значениям средней когерентности. По межполушарным парам отмечено снижение относительно нормы уровня внутримозговых связей в парах Fp2‑Fp1 и F4‑F3 и повышение в парах С4‑С3 и Р4‑Р3 у половины пациентов (51%) как свидетельство ослабления уровня межлобных отношений и повышение межтеменных. Аномальное состояние внутриполушарных отношений было отмечено у 43% детей в виде снижения значений когерентности в парах Fp1‑T3 и Fp2‑T4 и повышения в парах Т3‑О1 и Т4‑О2 (табл. 3 и 4).
Таблица 3
Результаты изменения внутриполушарных отношений по средней когерентности ЭЭГ до и после лечения Тенотеном детским детей с тикозными гиперкинезами и сопутствующим СДВГ