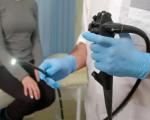
Эзофагит эозинофильный это что
Эозинофильный эзофагит
Эозинофильный эзофагит (англ. eosinophilic esophagitis; EoE) — клиническая форма поражения пищевода, развивающаяся на фоне аутоимунных заболеваний. Характеризуется увеличенным количеством эозинофилов в слизистой оболочке пищевода (эозинофилы — один из видов лейкоцитов крови). Предполагают, что причиной такой формы эзофагита является пищевая или респираторная аллергия и она требует иной тактики лечения, отличной от рефлюкс-эзофагита.
Эозинофильный эзофагит имеет тенденцию к увеличению частоты. В США в настоящее время зафиксировано 150 000 больных эозинофильным эзофагитом, 75 % из которых — взрослые.
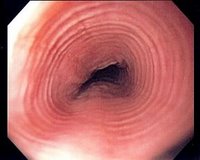
Эозинофильный эзофагит является распространенной причиной рефрактерной терапии к гастроэзофагельной рефлюксной болезни (ГЭРБ). Пациенты с эозинофильным эзофагитом обычно молодые люди, имеющие в анамнезе указания на перемежающуюся дисфагию, появляющуюся после приёма твердой пищи, и часто — на задержку пищи в пищеводе. Довольно частым ошибочным диагнозом при наличии эзофагита у этих больных является ГЭРБ. У многих больных имеется связь с развитием астмы или наличием пищевой аллергии, особенно против молока, яиц, арахиса или дынь. На предполагаемый диагноз эозинофильного эзофагита указывают эндоскопические проявления: множественные кольца в просвете пищевода, продольные бороздки, или экссудат белого цвета (Пасечников В.Д.).

Гистологическое исследование биоптата. Гиперплазия клеток базального слоя многослойного плоского эпителия (а). Эозинофилы в межклеточных пространствах – более 20 в 1 поле высокого разрешения в многослойном плоском эпителии пищевода (б). Окраска гематоксилином и эозином. Увел. а) х120, б) х500 (Валитова Э.Р. и др.).
При биопсии проксимального и дистального отделов пищевода в гистологических препаратах определяются более 15-20 эозинофилов в поле зрения.
Эозинофильный абсцесс в слизистой оболочке пищевода. Furuta G. et al, Gastroenterology, 2007; 133: 1342-1363.
Периферическая эозинофилия не является распространенным патологическим признаком. Патогенез эозинофильного эзофагита не известен. Предполагают, что развитие этого состояния провоцируется приемом пищи и аэроаллергенов, стимулирующих ответ цитокинов, обусловленных активацией Т-хелперов 2 типа, другие исследования предполагают, что у некоторых пациентов имеется атипичный вариант ГЭРБ. Естественное течение эозинофильного эзофагита плохо изучено, но известно, что оно не связано с исходом в рак пищевода. Симптомы этого заболевания и снижение количества эозинофилов в ткани достигается после трёхмесячного назначения ингаляционных стероидов (флутиказона пропионата дважды в день утром и вечером по 440 мкг). Для гарантированного адекватного поступления стероидов в пищевод, а не в легкие, спейсер не должен использоваться вместе с ингалятором. В случае, если ингаляционные стероиды не приводят к разрешению симптомов, используется иная терапия, включающая применение антагониста лейкотриена D4 (монтелюкаста 10-40 мг в день) или пероральных стероидов (преднизон 30 мг в день в течение 2 недель) с постепенным снижением дозы в течение 6 недель. У других пациентов используются ингибиторы протонной помпы с последующим бужированием стриктур (Пасечников В.Д.).
Имеются исследования, доказывающие, что после исключения из рациона больных шести групп наиболее вероятных аллергенов (молочные продукты, соя, пшеница, орехи, морепродукты, яйца) у большинства отмечаются клинические, эндоскопические и гистологические улучшения (Wolf WA et al, Clin Gastroenterol Hepatol. 2014;12:1272-1279).
Лечение эозинофильного эзофагита
Ингибиторы протонной помпы 20–40 мг (в зависимости от выбранного препарата) 1–2 раза в день в течение 8–12 недель или 1 мг/кг на 1 прием дважды в день в течение 8–12 недель у детей значительно облегчают симптомы и приводит к нормализации гистологической картины у значительной группы пациентов.
Системное применение кортикостероидов имеет строгие показания: тяжелая дисфагия как результат осложнений эозинофильного эзофагита (стриктуры и узкий пищевод); связанная с осложнениями госпитализация; потеря массы тела. Из-за значительных побочных эффектов длительное применение системных стероидов при эозинофильном эзофагите не рекомендовано.
Топические стероиды применяют у детей и взрослых для индукции ремиссии и поддерживающей терапии. Они хорошо переносимы и имеют минимальные побочные эффекты, среди которых наиболее частыми являются кандидоз полости рта и пищевода, герпетическая инфекция. Для индукции ремиссии применяют флутиказон в дозе 440–880 мкг дважды в день по схеме впрыск–глоток и будесонид (густая суспензия) 2 мг в день. После приема топических стероидов не рекомендуется принимать пищу и пить в течение 30 минут. После успешной индукции ремиссии необходима длительная поддерживающая терапия.
Раздел «Лечение. » написан на основе статьи Ивашкина В.Т. и др.
Эозинофильный эзофагит
Эозинофильный эзофагит — это хронический иммуноопосредованный воспалительный процесс, который характеризуется резко выраженной эозинофильной инфильтрацией слизистой оболочки пищевода. Патология проявляется затруднениями проглатывания твердой пищи, загрудинными болями, периодически возникающей рвотой. Для диагностики эзофагита используется эндоскопическое обследование с биопсией, гистологический анализ биоптатов. Для уточнения диагноза проводится исследование крови и мочи, иммунограмма. Лечение предполагает комбинацию индивидуально подобранной диеты с назначением топических стероидов и ингибиторов протонной помпы.
МКБ-10
Общие сведения
Эозинофильный эзофагит (ЭоЭ) — вторая по частоте выявления патология пищевода после ГЭРБ. Манифестирует в любом возрасте, но чаще встречается у школьников (средний возраст пациентов — 9 лет) и у людей среднего возраста (около 38-40 лет). В 75-82% ЭоЭ развивается у мужчин. Распространенность эозинофильного эзофагита на 10 тыс. населения у детей составляет 10,5 случаев, у взрослых — около 4,5 случаев. За последние 20 лет ученые отмечают рост заболеваемости в 70 раз, что обуславливает высокую медико-социальную значимость болезни.
Причины
Заболевание относится к иммунным антигенопосредованным поражениям слизистого слоя ЖКТ, но его этиологические факторы до конца не определены. Существует мнение, что патология выступает как проявление общей атопической реакции организма. В современной гастроэнтерологии принята концепция, согласно которой выделяют 3 группы причин эозинофильного эзофагита:
Факторы риска
Вероятность развития эозинофильного эзофагита возрастает при наличии у человека других аллергических заболеваний:
Установлена повышенная заболеваемость среди пациентов с наследственными поражениями соединительной ткани (синдромы Элерса-Данлоса, Марфана). К независимым факторам риска относят потребление ГМО-продуктов, повсеместное и неоправданное использование антибиотиков. Вероятность появления эзофагита увеличивается при проживании в регионах с неблагоприятной экологической ситуацией.
Патогенез
Патофизиологической основой эозинофильного эзофагита является миграция вглубь пищеводной слизистой эозинофилов — клеток лейкоцитарного ряда, которые в норме там отсутствуют. Под действием аллергенов происходит активация Т-лимфоцитов, индукция синтеза специфических провоспалительных интерлейкинов 4, 5 и 13. Эти вещества влияют на эпителий и усиливают выработку эотаксина-3.
Как следствие усиливается хемотаксис эозинофилов из периферической крови в эзофагеальную слизистую, повышается их пролиферация в костном мозге. Эозинофилы выделяют биологически активные вещества — МВР, катионные белки, пероксидазу и нейротоксин. Следующим этапом эозинофильного воспалительного процесса становится выброс гистамина и цитокинов, которые оказывают прямое повреждающее действие на пищевод.
Симптомы эозинофильного эзофагита
У детей дошкольного возраста заболевание проявляется трудностями с кормлением. Периодически по окончании приема пищи появляются срыгивание или рвота. Дети отказываются от еды, становятся нервными и беспокойными. Из-за сложностей с проглатыванием ребенок предпочитает жидкую или полужидкую пищу, длительно пережевывает каждый кусочек. Наблюдается медленный набор веса, отставание в росте и физическом развитии.
Школьники и подростки, страдающие эозинофильным эзофагитом, жалуются на изжогу, умеренные боли за грудиной. Возникает необходимость запивать водой любую твердую пищу, что облегчает глотание. Ребенок ест очень медленно, обычно оставляет половину порции на тарелке. Некоторые подростки сообщают о чувстве «застревания» еды в пищеводе, дискомфорте в верхних отделах живота. При попытке быстрого поглощения пищи начинается рвота.
У взрослых людей клиническая картина схожа, но в связи с длительным течением эозинофильного эзофагита симптомы выражены сильнее. Больные предъявляют жалобы на мучительные давящие или распирающие боли по ходу пищевода, которые беспокоят после еды. Дисфагия наблюдается постоянно, возникают сложности с употреблением даже полужидкой пищи. Неприятные симптомы провоцируют повышенную нервозность и раздражительность.
Осложнения
Опасное последствие эозинофильного эзофагита — острый разрыв пищевода (синдром Бурхаве), обусловленный обтурацией органа большим пищевым комком. Это состояние сопровождается подкожной эмфиземой, болевым шоком. На фоне разрыва иногда начинаются профузные кровотечения в виде кровавой рвоты, которые опасны геморрагическим шоком и без оказания медицинской помощи имеют неблагоприятный исход.
При длительном существовании эозинофильного воспаления в стенке органа образуется соединительная ткань. Фиброз проявляется стриктурами и стенозом пищевода, что усугубляет клиническую картину заболевания. Персистирующие воспалительные процессы являются предпосылкой для метаплазии эпителиальных клеток, поэтому наличие эозинофильного эзофагита сопряжено с риском появления злокачественных опухолей.
Диагностика
При первичной консультации врач-гастроэнтеролог использует несколько опросников для оценки частоты и тяжести симптомов. При физикальном обследовании эозинофильный эзофагит ничем не отличается от ГЭРБ. В пользу первого заболевания говорит отягощенный аллергологический анамнез. Для верификации диагноза обязательно проводится комплекс лабораторно-инструментальных методов, включающий:
Лечение эозинофильного эзофагита
Консервативная терапия
Первый этап лечения — подбор рациона питания. Элементная диета с приемом аминокислотных смесей назначается редко, поскольку зачастую плохо переносится больными. Чаще прибегают к таргетной диете, которая предполагает исключение из рациона индивидуальных пищевых аллергенов. До проведения специфических тестов показана эмпирическая элиминационная диета, предусматривающая ограничение наиболее распространенных аллергизирующих веществ.
Эффективность диетотерапии составляет около 53% у детей и около 40% у взрослых. Если клинические проявления не удается купировать немедикаментозными способами, используют лекарственные препараты. Для лечения эозинофильного эзофагита рекомендована длительная поддерживающая терапия, которая в несколько раз снижает вероятность обострения. Схема включает:
Хирургическое лечение
К эндоскопическим методам прибегают при сужении пищеводного просвета до 13 мм и менее. Хирургические вмешательства в основном рекомендуются взрослым. Для снижения явлений дисфагии показана эндоскопическая баллонная дилатация или бужирование пищевода. Вмешательство выполняется в плановом порядке после стихания активности процесса в результате проведения медикаментозной терапии.
Экспериментальное лечение
На сегодняшний день существует успешный опыт применения моноклональных антител к интерлейкинам для редукции симптоматики и уменьшения эозинофильной инфильтрации. В клинических испытаниях установлена высокая эффективность препаратов для купирования дисфагии. Хорошие результаты наблюдаются при назначении селективных антител к ИЛ-13, эффект которых продолжается дольше 6 месяцев.
Прогноз и профилактика
Благодаря разработке новых методов терапии эозинофильного эзофагита стойкой ремиссии удается добиться у 80-90% больных. Прогноз благоприятный: большинство пациентов, которым правильно подобрано лечение, отмечают улучшение качества жизни и возвращение к привычному ритму активности. Профилактика включает раннее выявление и лечение атопических патологий, устранение пищевых и экологических факторов риска.
Эозинофильный эзофагит
Общая информация
Краткое описание
Клинические рекомендации по диагностике и лечению эозинофильного эзофагита (Москва, 2013)
Этиология и патогенез
В формировании ЭоЭ имеет значение патогенетическое влияние трех групп факторов: воздействие воздушных и пищевых аллергенов, генетическая предрасположенностьи активация Т-хелперов 2 типа (Th2).
Триггерным фактором развития эзофагита являются аллергены внешней среды (пищевые и воздушные), которые, попадая на слизистую оболочку пищевода, инициируют развитие иммуновоспалительного процесса. Роль пищевых аллергенов в развитии заболевания подтверждается высокой эффективностью элиминационных диет у детей с ЭоЭ.
Для заболевания характерно сезонное течение, с обострением клинической картины и увеличением количества эозинофилов в слизистой пищевода в период цветения растений, что свидетельствует о роли воздушных аллергенов в патогенезе ЭоЭ.
ЭоЭ очень часто протекает на фоне других атопических заболеваний. В целом, до 86% взрослых и 93% детей, больных ЭоЭ, имеют аллергические заболевания на момент обращения, около половины больных отмечают наличие таких заболеваний в анамнезе, что свидетельствует об атопическом характере ЭоЭ.
Итак, пищевые и воздушные антигены являются пусковым фактором заболевания, в основе же патогенеза ЭоЭ лежит генетически детерминированная патология иммунного ответа. Зачастую заболевание носит семейный характер: около 8% больных детей имеют кровных родственников, страдающих ЭоЭ.
На сегодняшний день уже известно несколько генетических аномалий, приводящих к развитию эозинофильной инфильтрации слизистой оболочки пищевода. Усилия ученых направлены на расшифровку новых генов, ответственных за развитие атопических заболеваний в целом и эозинофильного эзофагита в частности.
Возникновение эозинофильного эзофагита обусловлено мутацией в гене TSLP (расположен в хромосоме 5q22), кодирующем синтез тимического стромального лимфопоэтина, а также мутацией в гене, кодирующем синтез рецептора к тимическому стромальному лимфопоэтину (TSLPR), расположенному в половых хромосомах Xp22.3 и Yp11, с чем связано преобладание лиц мужского пола среди больных ЭоЭ. Данная мутация приводит к гиперэкспрессии гена TSLP в слизистой оболочке пищевода.
TSLP является цитокином, экспрессируемым клетками тимуса, слизистой оболочки желудочно-кишечного тракта, легких, кожи. TSLP активирует иммунокомпетентные клетки, в частности, дендритные клетки и мастоциты, способствуя детерминации иммунного ответа по Тh2-зависимому пути. Гиперэкспрессия TSLP характерна не только для ЭоЭ, но и для бронхиальной астмы, атопического дерматита, экземы. Более того, в коже при атопическом дерматите и в слизистой пищевода при ЭоЭ имеются схожие морфологические особенности: эозинофильная инфильтрация и гиперплазия базального слоя многослойного эпителия, дегрануляция эозинофилов, что говорит об общности патогенеза ЭоЭ и атопических заболеваний.
Кроме того, у больных ЭоЭ в гене, кодирующем эотаксин- 3 (аллель G SNP (T/G +2496), 3’ UTR гена эотаксина-3) имеется замена тимина на гуанин в положении 2496, что приводит к гиперэкспрессии цитокина эотаксина – 3.
Эотаксин-3 является хемокином эозинофилов, стимулирующим пролиферацию эозинофилов в костном мозге, выход их в периферическое кровеносное русло. Эотаксин-3 удлиняет время жизни эозинофилов и вызывает их хемоаттракцию в слизистую пищевода. Экспрессия эотаксина-3 в слизистой оболочке пищевода больных ЭоЭ в 50 раз превышает таковую у здоровых добровольцев. Причем, чем выше уровень экспрессии эотаксина-3, тем выраженнее степень воспалительной инфильтрации пищевода.
Таким образом, имеющиеся поломки в генетическом аппарате иммунокомпетентных клеток приводят к развитию иммунного ответа по пути активизации Т-хелперов 2 типа, которые продуцируют чрезвычайно активную группу интерлейкинов (ИЛ-4, ИЛ-5, ИЛ-13), обладающих огромным разнообразием эффектов.
В целом, иммунный ответ при ЭоЭ характеризуется гиперпродукцией Тh2-ассоциированных цитокинов в ответ на воздействие пищевых и воздушных антигенов, что, как известно, характерно для большинства атопических заболеваний. На сегодняшний день ЭоЭ признается одним из проявлений общей атопической реакции организма (наряду с атопическим дерматитом, астмой, пищевой аллергией и другими атопическими заболеваниями). В этой связи всем больным с подозрением на ЭоЭ рекомендовано проведение дополнительных исследований (консультация пульмонолога, исследование функции внешнего дыхания, кожные аллергические пробы и др.), направленных на диагностику бронхиальной астмы, пищевой аллергии и других атопических состояний.
Таким образом, с учетом накопленных на сегодняшний день данных, этиопатогенез ЭоЭ представляется следующим образом: при воздействии воздушных и пищевых аллергенов на слизистую оболочку пищевода у лиц с имеющейся генетической предрасположенностью происходит активация антигенпрезентирующих клеток с последующим представлением антигенов Т-лимфоцитам и мастоцитам. Т-лимфоциты в условиях гиперэкспрессии TSLP детерминируются по пути преимущественного образования Т-хелперов 2 типа и совместно с мастоцитами начинают продуцировать интерлейкины ИЛ-4, ИЛ-5, ИЛ-13, которые, воздействуя на эпителий пищевода, фибробласты, гладкомышечные клетки стимулируют экспрессию ими эотаксина-3.
Гиперпродукция эотаксина-3 эпителиоцитами в результате мутации и/или сенсибилизации вызывает хемоаттракцию эозинофилов в слизистую оболочку пищевода. Кроме того, интерлейкины Т-лимфоцитов 2 типа, особенно ИЛ-5, сами обладают свойствами колониестимулирующих факторов для эозинофилов, активируя их пролиферацию в костном мозге и выход в периферическое русло, увеличивают продолжительность жизни и хемоаттракцию эозинофилов в слизистую пищевода.
Воспаление, индуцированное эозинофилами, характеризуется гиперэкспрессией ИЛ-13 и TGF-ß, которые стимулируют клеточную пролиферацию, фиброзо- и ангионеогенез. Кроме того, эозинофилы синтезируют лейкотриены C4, D4, T4, эффект которых реализуется в повышении сосудистой проницаемости, гиперпродукции слизи, стимуляции сокращений гладкомышечных клеток.
Кроме эозинофилов в слизистой оболочке пищевода больных ЭоЭ наблюдается значительное увеличение числа мастоцитов, присутствующих в здоровом пищеводе в единичных количествах. На поверхности мастоцитов при ЭоЭ обнаруживаются синтезированные (системно или локально) IgE, содействующие активизации тучных клеток пищевыми антигенами. Активированные мастоциты способны высвобождать такие медиаторы воспаления, как цитокины, гистамин, протеазы.
В слизистой оболочке больных ЭоЭ обнаруживаются также В-лимфоциты, продуцирующие IgЕ, высок уровень других субпопуляций лимфоцитов (CD3+,CD8+,CD4+). Массивное повреждение слизистой оболочки иммунокомпетентными клетками быстро приводит к вовлечению в процесс фибробластов и эндотелиоцитов, происходит гиперплазия базального слоя эпителия и гладкомышечных клеток, активация фиброзогенеза и ангионеогенеза в подслизистом слое, что в конечном итоге приводит к потере эластичности мышечной ткани и образованию стриктур стенки пищевода.
Существует влияние еще одного фактора, вносящего значительный вклад в развитие и прогрессирование воспаления слизистой пищевода при ЭоЭ. Речь идет о сопутствующей гастроэзофагеальной рефлюксной болезни.
ГЭРБ служит кофактором в патогенезе ЭоЭ, способствуя более глубокому проникновению антигенов через поврежденную кислотно-пептическим рефлюктатом слизистую пищевода. Наличие кислого рефлюкса усиливает степень эозинофильной инфильтрации слизистой пищевода, способствует высвобождению мастоцитами медиаторов воспаления, а расширение межклеточных пространств при ГЭРБ приводит к взаимодействию антигенпрезентирующих клеток с аллергенами. Поэтому значительная доля пациентов с клиническими и гистопатологическими особенностями, характерными для ЭоЭ, отвечает на антисекреторную терапию клиническим улучшением и уменьшением степени эозинофильной инфильтрации слизистой пищевода.
Эзофагит эозинофильный это что
Полный текст статьи:
Эпидемиология
Считается, что эозинофильный эзофагит встречается чаще у мужчин, чем женщин и у детей, чем взрослых. Однако конкретные цифры распространенности данной патологии все еще не ясны [13].
Этиология
Вопросы этиологии данного заболевания дискутабельны. Рассматривается роль пищевых аллергенов и воздушных аллергенов. Так же обсуждается возможность аутоиммунного характера заболевания. Считается, что пищевая аллергия при ЭОЭ носит характер пищевой гиперчувствительности и является аллергической реакцией IV типа. Роль воздушных аллергенов в развитии ЭОЭ кажется вероятной с того момента как в эксперименте продемонстрировал развитие эозинофильного эзофагита у мышей в ответ на действие воздушного аллергена [14]. Косвенным подтверждением такой возможности является и тот факт, что не у 100 % пациентов жесткая ограничительная диета приводит к улучшению. Сами же эозинофилы оказывают свое воздействие через выделяемые ими при дегрануляции медиаторы воспаления как лейкотриены и простагландины, а также путем образования свободных радикалов и пероксидазы.
Клиника и диагностика
Симптомы ЭОЭ подобны таковым при ГЭРБ. Они включают изжогу, регургитацию, рвоту, боль эпигастрии и дисфагию. Клиника у взрослых и детей отличается. У маленьких детей в клинической картине может доминировать отказ от еды, тошнота, рвота у подростков (и взрослых) чаще встречается дисфагия. Симптомы, особенно рвота и дисфагия, чаще носят интермитирующий характер с частотой 1-2 раза в месяц. Изжога и боль в эпигастрии более постоянны. Симптомы могут нарастать с течением времени. У примерно 50 % детей с ЭОЭ присутствуют другие проявления аллергии как бронхоспазм, экзема и аллергический ринит. Около 35-45 % пациентов имеют семейный анамнез пищевой аллергии или астмы. Стриктуры, связанные с ЭОЭ, более склонны к рецидиву, чем пептические стриктуры при ГЭРБ.
На основании обследования 347 пациентов Liacouras [10] сообщал, что у 81 % пациентов с ЭОЭ наблюдались симптомы ГЭРБ, причем рвота и регургитация у 70 % больных. В 69 % случаев беспокоила боль в животе, в 19 % дисфагия (преимущественно наблюдалась у мужчин). Сопутствующий бронхоспазм, экзема или ринит был у 52% больных, а отягощенный семейный аллергологический анамнез у 43 % пациентов.
Диагноз ЭОЭ более вероятен у пациента с:
Успешная диетотерапия (ограничительная) делает это диагноз еще более вероятным.
Эндоскопия
Морфология
Для ЭОЭ характерна «выраженная» изолированная эозинофильная инфильтрация пищевода. Несмотря на то, что однозначного толкования понятия «выраженная» эозинофильная инфильтрация не достигнуто, большинство авторов соглашается с тем, что количество эозинофилов более 20 является диагностическим критерием ЭОЭ. Обнаружение такого числа эозинофилов у пациента, получающего массивную антисекреторную терапию еще более характерно для данной патологии [13].
Наиболее сложной является дифференциальная диагностика ЭОЭ и ГЭРБ. Основные критерии суммированы в таблице.
| Эозинофильный эзофагит | ГЭРБ |
| Симптомы интермитирующие | Симптомы постоянные |
| Нормальные данные рН-метрии | Патологические данные рН-метрии |
| Антисекреторная терапия без эффекта | Секреторная терапия эффективна |
| Более 20 эозинофилов в поле зрения | 1-5 эозинофилов в поле зрения |
Лечение
Основными вопросами терапии ЭОЭ остаются:
Антисекретоная терапия и антирефлюксные операции при ЭОЭ не эффективны!
Элиминационная диета. Наиболее логичным и легким подходом кажется устранение аллергена. Основной проблемой данной тактики является крайняя сложность точного выявления пищевого аллергена ответственного за заболевание. Кроме того, у ряда пациентов наблюдается аллергия не на один, а несколько пищевых продуктов. Кожные пробы с различными аллергенами могут помочь в выявлении агента вызвавшего ЭОЭ, но далеко не всегда. Строгая элиминационная гипоаллергенная аминокислотная диета не очень приятна. Достаточно сказать, что в одном исследовании сообщающем об успешном применении такого подхода только 3 пациента из 51 согласились принимать эту формулу перорально, в остальных случаях использовался назогастральный зонд [12]. Да и положительное действие диеты, как правило, становится заметным только через несколько дней. Кроме того, специальные формулы дороги и не везде доступны. Проблемой остается расширение диеты после достигнутого положительного эффекта т.к. риск рецидива весьма высок.
Наиболее рациональным, при невозможности выявления специфического антигена, нам представляется исключение 7-х аллергогенных групп продуктов как молоко, соя, яйца, пшеница, рыба, моллюски и орехи. Купирование симптоматики в течение 7-10 дней и разрешение эозинофильной инфильтрации при повторной биопсии через 4-6 недель позволяет аккуратно расширять диету по одному виду продуктов 1 раз в неделю (существуют специальные перечни продуктов согласно их потенциальной аллергогенности) под пристальным контролем симптоматики. При возникновении симптомов исключите последний вид введенной пищи. Если после исключения «опасной семерки» симптомы, или эозинофильная инфильтрация сохраняются, то необходимо применить элиминационную, основанную на аминокислотах диету с ее последующим расширением по ранее изложенной схеме.
Противовоспалительное лечение. Системные кортикостероиды. Ряд исследований подтвердили эффективность такой терапии. Например Liacouras применил метилпреднизолон в дозе 1,5 мг/кг в два приема в течение 4 недель. После лечения у 19 из 20 пациентов отмечалось значительное клиническое и гистологическое улучшение. Однако у 9 пациентов симптомы появились вновь при сроках наблюдения до одного года [9]. Однако системные эффекты кортикостероидов весьма не желательны и это привило к использованию местных стероидов [2]. Например, таких как флутиказон, будесонид или беклометазон. Рекомендуется два распыления этих препаратов в рот с последующим проглатыванием два раза в день в течение 6 недель [4]. Положительный ответ наступает в течении недели. Единственным описанным осложнением такой терапии являлся кандидоз пищевода, который наблюдался при применении флyтиказона в дозе 220 мг два раза в день [18]. Кроме того, используются селективные антагонисты лейкотриенов и препараты направленные на снижение продукции цитокинов.