Как поддержать печень при химии
Защита печени после химиотерапии
Печень — наиболее крупный, сложный, выполняющий в организме большое количество функций, орган. Печень после химиотерапии орган, который подвергся максимальным негативным воздействиям. При этом затрагиваются такие функции, как участие в обмене веществ, обезвреживание токсинов и выведение с желчью различных веществ. Это происходит потому, что печень вначале является проводником противоопухолевого лекарственного средства, а затем включает функцию защиты от токсического воздействия этого же препарата.
Перед назначением курса химиотерапии лечащий врач обязательно назначает биохимический анализ крови. У пациентов, которые не работают на вредном производстве, не болели гепатитом и не злоупотребляют алкоголем, результаты такого анализа находятся в пределах нормы. При помощи этого же анализа выявляют и начальную стадию каких-либо нарушений, с этой целью до и после химиотерапевтического курса сдают кровь на ферменты и билирубин. Иногда по окончании химиотерапии эти показатели ухудшаются в 5 раз, но это не причина для волнений, поскольку печень обладает способностью к восстановлению своих поврежденных клеток, что и происходит обычно между курсами лечения.
Печеночная недостаточность
При выраженной печеночной недостаточности отмечаются отклонения в «биохимии» крови, наблюдаются желтушность кожи и слизистых, кровоизлияния на коже, сосудистые «звездочки». Данные симптомы говорят о поражении значительного количества печеночных клеток, что требует полной или частичной отмены химиотерапии. Во избежание таких явлений при назначении особо токсичных химиопрепаратов следует употреблять также и препараты, защищающие печень, лучше всего сделать это до начала лечения.
Гепамин
Благодаря научным поискам в настоящее время появилось эффективное средство нового поколения Гепамин, специально разработанное для лечения печеночных патологий, в том числе и таких опасных, как печеночная энцефалопатия и тяжелые формы циррозов.
Гепамин обладает способностью блокировать не только главные симптомы, но и непосредственную причину заболевания. Под действием данного препарата восстанавливается нарушенный обмен аминокислот, происходит нормализация обменных процессов, усиливается обезвреживающая функция печени. Побочных эффектов от применения данного средства не наблюдается. Поэтому, Гепамин включили в стандарты медпомощи онкологическим больным. В его состав входят натуральные биологически активные компоненты, произведенные во Франции.
Инозие Ф, Сирепар
При токсическом поражении печени продемонстрировал свою эффективность препарат Инозие Ф. Его принимают по две таб. 3 раза в день.
Урсофальк
Наибольших похвал гепатологов, т. е. докторов, специализирующихся на лечении заболеваний печени, добился препарат Урсофальк, прием которого выполняется по одной капсуле 2-3 раза в день. На сегодняшний день он считается лучшим, но применять его следует при действительно серьезных поражениях печени.
Эрбисол
Особым успехом пользуется разработанный на Украине препарат Эрбисол. Он эффективен при острых и хронических гепатитах, в том числе медикаментозных и токсических. Помимо этого, Эрбисол нашел применение в качестве гепато- и иммунопротектора при проведении химиотерапии.
Благодаря своему свойству защищать печеночные клетки от лучевого и химического воздействия, стало возможным использование более интенсивных способов лечения сильнодействующими средствами, а также облучение максимальными дозами без риска развития тяжелых побочных эффектов, проявляющихся в виде вегетативного, болевого и диспепсического синдромов, выпадения волос.
Способность восстанавливать иммунную систему является еще одним ценным качеством Эрбисола. Показанием к назначению Эрбисола служат развившиеся гепатиты печени после химиотерапии.
Фосфоглив
Фосфоглив является отечественным препаратом растительного происхождения, относящимся к новому поколению. Он способен восстановить нарушенную способность печени выводить вредные вещества. Назначают данное средство при гепатитах, жировых и токсических повреждениях печени.
Ропрен
Ропрен представляет собой новый российский препарат, предназначенный для защиты и восстановления пораженных клеток печени после химиотерапии. Он назначается по 3 капли одновременно с приемом пищи.
Преднизолон
Нельзя также обойти вниманием препарат Преднизолон, который, хоть и является гормональным, необходим при повреждениях печени после химиотерапии. Рекомендуется принимать его по 4-6 таблеток в день после еды, содержащей молочные продукты. Дополнительно с этим рекомендуется прием оротата калия, что необходимо для предотвращения потерь калия, которые влечет за собой прием преднизолона.
Если печень нуждается в экстренной помощи, в некоторых случаях назначается дексаметазон внутримышечно по 8 мг 1 или 2 раза в день.
Гепабене
Помогает восстанавливать печеночные клетки и препарат растительного происхождения под названием Гепабене. Он наиболее эффективен при длительных нарушениях биохимических показателей крови.
Гепаркомпозитум
Галстена
Препаратом, восстанавливающим и нормализующим печень после химиотерапии, является также Галстена. Это лекарственное средство способно уменьшать размеры печени, которые под его влиянием могут сокращаться на 4 см.
Применяется Галстена при поражениях желчевыводящих путей и печени. Под ее действием улучшается переносимость жирной пищи, исчезает чувство тяжести справа, уменьшается и пропадает тошнота, вздутие живота, боли в правом подреберье, заметно улучшаются биохимические показатели крови.
Препарат не имеет побочных эффектов, принимается по 15-20 капель трижды в день через час по окончании приема пищи.
Эссенциале
Если биохимические анализы крови пациента еще перед началом лечения указывают на наличие нарушений, к перечисленным ранее лекарственным средствам добавляют препарат Эссенциале-Н. Длительность его приема составляет два-три месяца, при этом эффект от лечения может проявиться только спустя несколько недель от его начала. Принимают это средство по 2 таблетки 3 раза в день во время еды. Для ускорения результата препарат могут вводить внутривенно по 5-10 инъекций ежедневно.
Аналогичным образом действует препарат Эссливер Форте, который тоже защищает печень и уменьшает проявления лекарственной интоксикации.
Гепастерил
В случае тяжелой печеночной недостаточности назначают препарат Гепастерил А. Есть также другая разновидность лекарства — Гепастерил В, который наиболее эффективен при поражениях печени в результате химиотерапии, но он чрезвычайно дефицитен.
Гепастерил назначают по 500 мл путем внутривенно — капельного введения, со скоростью приблизительно 40 капель в минуту. Максимальную эффективность проявляет в сочетании с отечественным лекарственным средством — гемодезом, который применяют также способом внутривенно-капельных вливаний. Назначают гемодез по 400 мл в сутки ежедневно или через день, на курс отводится 5 таких процедур.
Креон
При поражениях печени и поджелудочной железы больным назначают препарат Креон. Данное средство рекомендуется принимать от 1 до трёх капсул во время еды, что значительно облегчает работу печени.
Все перечисленные выше лекарственные средства относятся к современным. Помимо них существуют хорошо знакомые, уже зарекомендовавшие себя в течение многих лет — метионин, кокарбоксила, АТФ, липоевая кислота, которые малотоксичны и менее дорогостоящи.
Для подбора эффективного метода лечения вы можете обратиться за
— методы инновационной терапии;
— возможности участия в экспериментальной терапии;
— как получить квоту на бесплатное лечение в онкоцентр;
— организационные вопросы.
После консультации пациенту назначается день и время прибытия на лечение, отделение терапии, по возможности назначается лечащий доктор.
Восстановление печени после химиотерапии
Содержание:
Самым большим непарным органом в теле человека считается печень. Она отличается не только размерами, но и наиболее важными функциями, которые выполняет. В ней происходят основные обменные процессы и преобразование пищи в необходимые для нормальной жизнедеятельности элементы. В печени вырабатываются белки альбумины, участвующие в метаболизме, и растворимые ß-глобулины – факторы свертывания крови. Накопленный ее клетками (гепатоцидами) гликоген перерабатывается в глюкозу, являющуюся источником энергии всего организма. Но, пожалуй, главной ее особенностью является дезинтоксикация чужеродных веществ и метаболитов. Отравляющие компоненты – яды, аллергены, токсины трансформируются в безвредные соединения и выводятся естественным образом.
Почему печень страдает после химиотерапии
Гепатотоксичность развивается при введении препаратов даже в строгих терапевтических дозах. Всемирной организацией здравоохранения регистрируется более двадцати видов побочных эффектов. Это обусловлено неизбирательностью действия цитостатиков, что сопровождается поражениями и функциональными нарушениями органа.
Симптомы повреждения печени
При развитии осложнений сбивается курс противоопухолевого лечения, дозировки вводимого препарата приходится снижать, что отражается на успешности терапии. Но главная проблема заключается в том, что негативное лекарственное воздействие трудно отличить от симптомов самой онкологии. Традиционные лабораторные пробы информативны только в диагностике заболевания, они не могут отобразить картину экскреторного и метаболического потенциала печени.
Сама она лишена нервных окончаний, вследствие чего болевые сигналы в мозг не поступают. Клинические особенности проявляются лишь на поздних стадиях при увеличении печени. Как только пациент обнаружит у себя следующие признаки, следует срочно обращаться к врачу:
При незначительном воспалении печень способна самостоятельно регенерироваться (восстанавливаться). Деление клеток помогает ей воссоздать первоначальный размер, даже если сохранено 25% здоровой ткани от общего объема. Но при повышенной нагрузке и коротких сроках между сеансами химии развиваются осложнения в виде гепатита или печеночной энцефалопатии, переходящей в кому с летальным исходом.
Препараты, применяемые для восстановления
Восстановление печени после химиотерапии ставит иногда специалистов в тупик и является предметом дискуссий. Выбирая гепатопротектор, положено придерживаться принципов доказательной медицины. Все используемые лекарства делятся на пять типов:
Общие рекомендации по образу жизни
Восстановление печени после химиотерапии включает целый комплекс мероприятий. Помимо лекарств, ухода со стороны медицинского персонала и родственников, важную роль в этом играют режим и диета. Привести в порядок печень помогут:
Следует сократить употребление бобовых. Полностью исключить прием острого, копченого и жареного. Убрать из рациона колбасы, маринады, соленья. Запрещаются спиртные и газированные напитки.
Восполнению витаминов и микроэлементов способствуют БАДы. Некоторые из них содержат бактерии, необходимые для воссоздания микрофлоры кишечника. Полезны отвары и настои из кукурузных рылец, овса, расторопши. Так же наши специалисты рекомендуют принимать капсулы с хлорофиллом ВИАЛАЙФ, которые помогут в кратчайшие сроки минимизировать побочные действия токсичных химиотерапевтических препаратов, благодаря свойствам максимально возможной дозировки хлорофилла в составе. Необходимы регулярные пешие прогулки, соблюдение распорядка дня и крепкий сон, так как печень подвержена суточным ритмам.
Услуги нашей клиники
Нашей клиникой давно используется авторская методика доктора Борисова Избирательная хронофототерапия (ИХФТ) в основе которой лежит фотодинамическая терапия способна активируя каскад биохимических и клеточных реакций регулировать уровень показателей иммунного статуса. В организм вводится специальное вещество – хлорофилл (натуральный фотосенсибилизатор последнего поколения), которое накапливается раковыми клетками. В место скопления направляется лазерный луч, способный синхронизироваться с ритмами больного, что позволяет уменьшить или увеличить интенсивность воздействия. Проникая на нужную глубину, он концентрируется на патологических клетках, уничтожая их, при этом не касаясь здоровых. В течение нескольких месяцев опухоль распадается. Она практикуется как в сочетании с хирургическими способами, а также до и после хирургических вмешательств, так и индивидуально. Широкий спектр возможностей позволяет задействовать ее при неэффективности химио-и лучевой терапии или в связи с тяжелым соматическим состоянием больного.
Для проведения применяется аппаратный лазер с определенной длиной волны. Выбор режимов также дает возможность осуществлять флуоресцентную диагностику в целях обнаружения очага воспаления, если он расположен на внутренних органах. Найти и ликвидировать опухоли помогает предварительно введенный фотосенсибилизатор последнего поколения (хлорофилл). Накапливаясь в пораженных тканях, он начинает под воздействием луча разрушать их. Происходит спазмирование сосудов, питание и рост новообразования прекращается.
ФДТ хорошо переносится людьми любого возраста и пола. В отличие от химиотерапии имеет ряд преимуществ:
Сроки и цены
Если вам предстоит в ближайшее время пройти химиотерапию, но вы не желаете или боитесь ее делать, ФДТ – это то, что вам нужно. Узнайте о ней более подробно, позвонив по телефону, или запишитесь на бесплатную консультацию.
На пути к безопасной химиотерапии
На пути к безопасной химиотерапии
«Доспехи» из чертополоха: новая стратегия защиты печени от побочных эффектов лекарств.
рисунок автора статьи
Автор
Редакторы
Статья на конкурс «Био/Мол/Текст»: На протяжении последних 50 лет химиотерапия, несмотря на серьёзные побочные эффекты, остаётся главным способом лечения рака. Значительный урон при этом наносится клеткам печени — гепатоцитам, в связи с чем понятие «гепатотоксичность» до недавнего времени было практически неотделимо от химиотерапии. Результаты новых исследований указывают на возможность сменить эту парадигму и сделать лечение рака гораздо более безопасным. Рассказываем о новом подходе, предложенном в 2020 году коллективом российских и американских учёных.
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Своя работа» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Лекарства из «чёрного ящика»
Лекарственная гепатотоксичность — это появление структурно-функциональных поражений печени, вызванных приёмом фармацевтических препаратов.
Противораковые средства на основе дакарбазина широко используются в клинической практике для лечения злокачественной меланомы, саркомы мягких тканей, классической лимфомы Ходжкина и неходжкинской лимфомы [8]. Однако, несмотря на высокую терапевтическую эффективность, данные многочисленных исследований свидетельствуют о тяжёлых гепатотоксических побочных эффектах дакарбазина [4], [9–10]. При этом наибольший урон печени наносят активные формы кислорода — свободные радикалы, которые вырабатываются в ответ на приём противоракового лекарства [10].
Новая стратегия защиты печени
На базе Государственного университета Южной Дакоты российско-американский коллектив учёных разработал стратегию по защите печени от негативного влияния противораковых препаратов. Предложенный подход, не нарушая эффективности химиотерапии, позволяет значительно снизить показатели гепатотоксичности, при этом морфология печени остается близкой к нормальной. Успешность разработки была подтверждена в ходе экспериментов на животных. Результаты этого исследования опубликованы в журнале Frontiers in Bioengineering and Biotechnology [11]. Кроме того, новая стратегия по снижению побочных эффектов гепатотоксичных лекарств была защищена патентом.
В чём новизна?
Существующие в настоящее время методы защиты печени от гепатотоксичных лекарств предполагают продолжительный приём таблеток, содержащих молекулы-протекторы. Одним из наиболее часто используемых гепатопротекторов с доказанной клинической эффективностью является силимарин или его активный компонент – силибинин. Это вещество, полученное из семян расторопши (чертополоха), активирует антиоксидантные клеточные механизмы, напрямую нейтрализует свободные радикалы, препятствует провоспалительной активации макрофагов печени, вызванной приёмом лекарств.
Важно отметить, что фармакокинетика лекарств-гепатопротекторов, включая силибинин, далека от идеальной. Вводимые перорально, они очень быстро выводятся из организма, и лишь небольшая их часть достигает печени, что не позволяет в полной мере запустить защитные процессы. К тому же при таком подходе часть протекторных агентов может попадать в опухоль и оказывать нежелательное воздействие на ход противораковой терапии. Стандартный внутривенный способ введения этих молекул в свободном виде практически неосуществим из-за их низкой растворимости в воде.
Фармакокинетика — совокупность процессов, происходящих с лекарством после его попадания в организм: всасывание, распределение, метаболизм и выведение.
Чтобы преодолеть вышеуказанные ограничения, учёные разработали новую стратегию высокоэффективной доставки силибинина в печень путем его внутривенного введения в наноинкапсулированном виде. Препарат предназначен для использования перед началом химиотерапии в качестве превентивного средства. За счёт применения полимерных нанокапсул в качестве носителя гепатопротектор за короткое время и в достаточном количестве накапливается в тканях печени и запускает в них каскад реакций, благодаря которым активируются механизмы антиоксидантной защиты клеток. Таким образом, препарат позволяет эффективно «подготовить» печень к встрече с цитотоксическим противораковым лекарством.
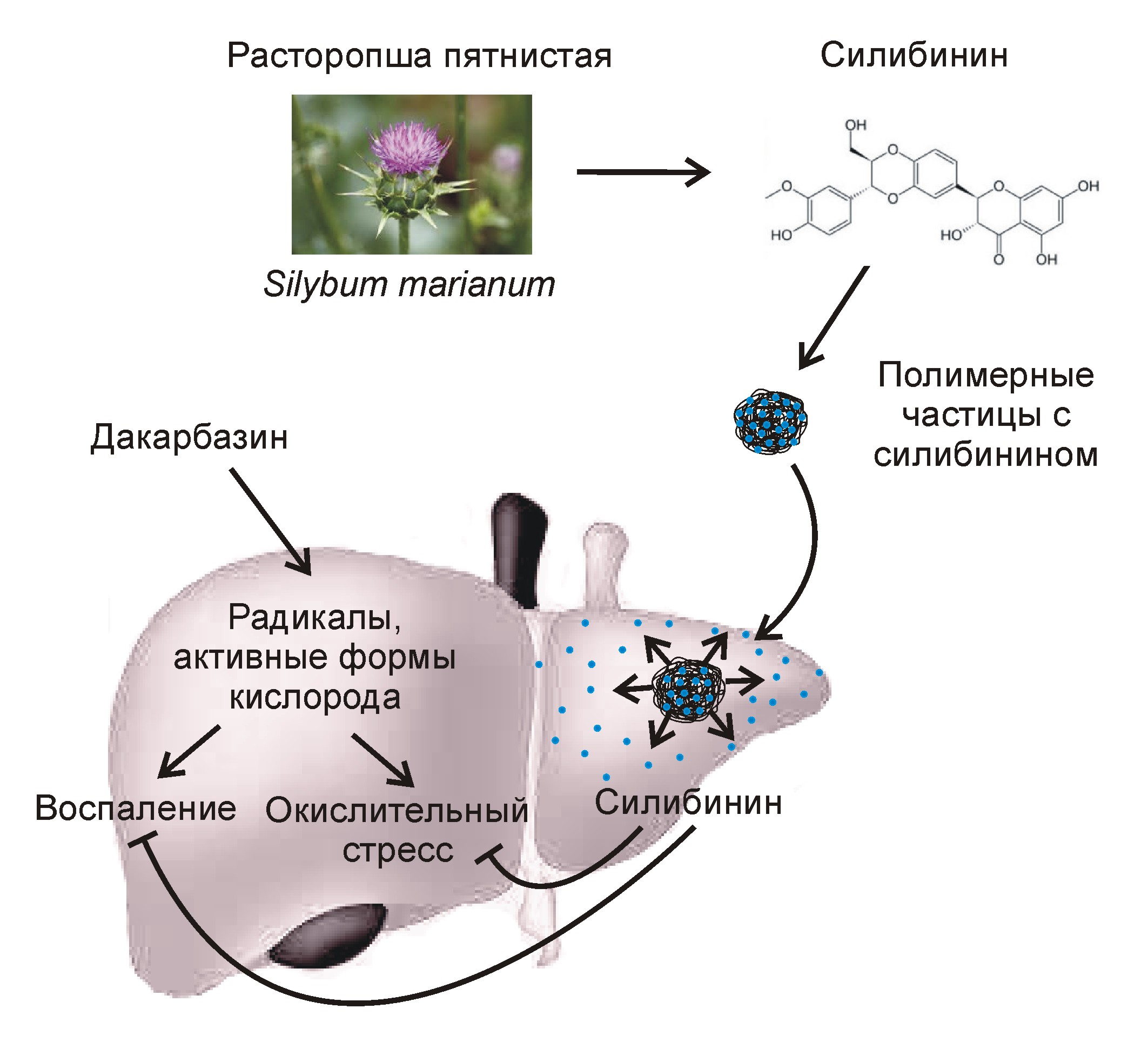
Новый препарат стал результатом совместной работы химиков и специалистов по биомедицинской инженерии. Его активным компонентом является силибинин, а носителем служат нанокапсулы из полилактид-ко-гликолида — безопасного биоразлагаемого полимера (рис. 1). Разработанный метод инкапсуляции позволил получить однородные по размеру наночастицы с высоким содержанием силибинина (его массовая доля составила 15%). Одним из достоинств данного препарата является то, что активный компонент медленно выделяется из нанокапсул, что обеспечивает его повышенную концентрацию в тканях печени в течение продолжительного времени.
Рисунок 1. Препарат на основе силибинина и полимерных наночастиц для защиты печени от побочных эффектов противоракового лекарства (дакарбазина).
рисунок автора статьи
Превратить недостатки полимеров в достоинства
Любопытно, что классическим «недостатком» полимерных носителей для адресной доставки лекарств обычно считается их быстрое накопление в печени. Это серьёзно ограничивает возможности терапии с использованием полимерных носителей, т.к. в идеале они должны достигать очага поражения, минуя здоровые ткани и органы, в особенности — печень. Но в данном случае задача адресной доставки была совсем иной. Необходимо было обеспечить попадание молекулы-протектора именно в печень, и учёные превратили ключевой «недостаток» полимерных носителей в ощутимое преимущество.
Стоит отметить, что использование нанокапсул снижает риск локализации гепатопротектора в опухоли, что неизбежно при пероральном приеме таблеток. Таким образом, удаётся избежать возможного нежелательного воздействия этих молекул на эффективность противораковой терапии.
Опсонизация — процесс адсорбции опсонинов (специальных белков) на поверхности инородных частиц, который стимулирует и облегчает их фагоцитоз.
Испытания на животных
В качестве противоопухолевого препарата, от которого нужно защищать печень, исследователи выбрали дакарбазин. Его часто используют для лечения злокачественных опухолей меланомы. К сожалению, несмотря на высокую терапевтическую эффективность, многочисленные исследования сообщают о гепатотоксических побочных эффектах лекарства, которые зачастую вынуждают прекращать терапию [4], [9]. В клинической практике наблюдались случаи острой печёночной недостаточности, веноокклюзионной болезни печени и даже смерти в течение нескольких дней после приёма дакарбазина.
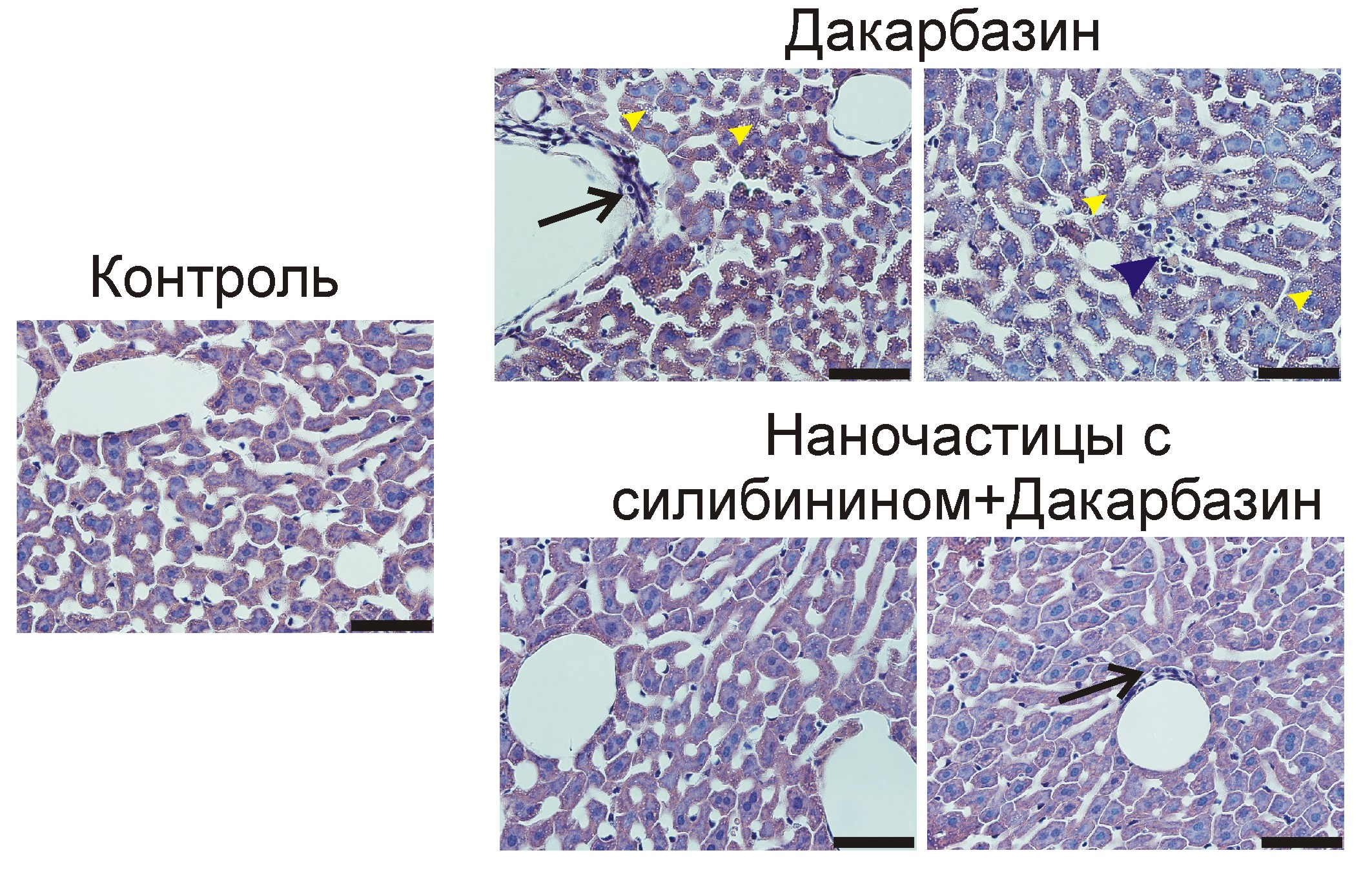
В ходе доклинических испытаний животные с раковыми опухолями подвергались химиотерапии путём системного введения дакарбазина. Часть мышей проходила предварительную «подготовку», получая разработанный учёными препарат для защиты печени. Исследователи подобрали оптимальный временной интервал между введением протектора и дакарбазина, позволяющий получить наилучший защитный эффект. У животных, прошедших стандартную химиотерапию, были обнаружены признаки серьёзного повреждения печени — некроз сосудистого эндотелия, вакуолизация и некроз гепатоцитов. А морфология печени мышей, предварительно получавших протектор на основе нанокапсул и силибинина, была близка к нормальной (рис. 2).
Рисунок 2. Морфология печени мышей, подвергавшихся воздействию дакарбазина и нового гепатопротектора. Контроль (нормальная морфология); дакарбазин (признаки повреждения печени); наночастицы с силибинином + дакарбазин (нормальная морфология, признаки повреждения отсутствуют). О некрозе гепатоцитов свидетельствует скопление лейкоцитов, поглощающих остатки погибших клеток (синяя стрелка). О некрозе сосудистого эндотелия свидетельствует скопление лейкоцитов в области эндотелия (чёрная стрелка). О вакуолизации свидетельствует наличие внутриклеточных пузырьков в гепатоцитах (жёлтые стрелки). Срезы окрашены гематоксилином и эозином.
Выбор оптимальных условий
Одним из механизмов действия силибинина является активация транскрипционного фактора Nrf2, который, в свою очередь, запускает в клетках экспрессию антиоксидантных ферментов, ферментов, восстанавливающих редокс-потенциал, и ферментов, способствующих деактивации свободных радикалов. Перед тем, как определиться с интервалом между введением протектора и дакарбазина, учёные поставили эксперимент, в котором определили, спустя какое время после однократного внутривенного введения протектора экспрессия этих ферментов в печени достигает максимальных значений. Именно это время соответствует наилучшей «подготовленности» клеток к встрече с цитотоксическим лекарством. Оно и было выбрано для дальнейших экспериментов в качестве интервала между введением протектора и дакарбазина (24 часа).
«Возможно, благодаря новой разработке удастся снять ограничения с широкого ряда лекарственных препаратов, использование которых лимитируется их гепатотоксичностью. Презентация наших работ в Бостоне на конференции CRS (Controlled Release Society) вызвала интерес со стороны фармацевтических компаний. Возможно, этот интерес перерастёт в проведение клинических испытаний», — отметил руководитель лаборатории, профессор Государственного университета Южной Дакоты Джошуа Рейнеке.
Все составные части разработанного препарата являются биосовместимыми и уже применяются в медицинской практике, что повышает шансы на ускоренный путь нового лекарства к клиническому использованию.
Лекарственное поражение печени при проведении химиотерапии
Профессор Драпкина О.М.: – Мы сейчас, так сказать, переносимся, в проблемы онкологии. И помочь разобраться нам с лекарственными поражениями печени при проведении химиотерапии поможет как раз профессор Ларионова Вера Борисовна.
Профессор Ларионова В.Б.: – Лекарственные повреждения печени – это очень важная проблема развитых стран. Во-первых, высок удельный вес лекарственной гепатотоксичности в структуре острой печёночной недостаточности, здесь привожу данные зарубежных авторов. (Демонстрация слайда). Также серьёзные этические проблемы и финансовые расходы лечения этого осложнения, которые ложатся бременем не только для учреждения, не только в целом для здравоохранения, но и порой для семьи, в которой находится пациент. А так же, малоутешительны результаты до сих пор при развитии фульминантной печёночной недостаточности, обусловленной лекарственной гепатотоксичностью несмотря на то, что сейчас в арсенале врачей находятся и экстракорпоральные методы детоксикации и методы заместительной терапии трансплантации печени, летальность остаётся достаточно высока.
Очень много лекарственных средств, в частности хим. препаратов, которые обладают генетической гепатотоксичностью. Хочу обратить ваше [внимание], вот здесь представлены препараты, которые часто дают лекарственную гепатотоксичность, но хочу обратить ваше внимание на то, что применение комплекса хим. препаратов усугубляет лекарственную гепатотоксичность. Вот я привела здесь одну из схем, которая достаточно часто используется в онкологии, и лекарственная гепатотоксичность при использовании этой схемы может достигать 80%.
Контроль органной токсичности полихимиотерапии очень важен. Это один из разделов изучения Международной ассоциации сопроводительной терапии рака, которая была организована в 1991-м году и ещё раз подчёркивает важность сопроводительной терапии в привлечении онкологических пациентов.
ВОЗ классифицируют более 20 видов побочных действий противоопухолевой химиотерапии и среди них выделяют и гепатотоксичность. Однако до сих пор остается много неразрешённых проблем. Одна из них – это отсутствие документальной регистрации гепатотоксичности при проведении химиотерапии. Также ведущие, научные общества, которые занимаются изучением лечения онкологических пациентов, здесь я представила, они также не представили практических рекомендаций по лечению гепатотоксичности.
Информация об элементах сопроводительной терапии при лекарственных поражениях печени в онкологии разбросана в специальной литературе, что создаёт большие сложности для врачей, которые занимаются сопроводительной терапией, в частности лечением органной или печёночной токсичности при использовании хим. препаратов. И вот, чтобы не быть голословным, я здесь привела trial поиска литературы, который касается исследований по лекарственной гепатотоксичности. И вот 0 исследований по запросу «гепатотоксичность, индуцированная химиотерапией». А также анализ базы данных проводимых исследований по нежелательным, серьёзным явлениям, [по] записи от 1958-го по 2007-е годы этот поиск проведён. И вот всего зарегистрировано около 37 тысяч случаев нежелательных побочных явлений, и только 26-50% для онкологических пациентов.
Чем же обусловлена лекарственная гепатотоксичность или гепатотоксичность противоопухолевых препаратов? Во-первых, это неизбирательность действия большинства цитостатиков, что сопровождается разнообразными поражениями печени, и сопровождается функциональными нарушениями различных органов. Естественно, при развитии того или иного осложнения, в частности гепатотоксичности, нарушаются протоколы лечения, то есть мы вынуждены прерывать курсы лечения, вынуждены редуцировать дозы препаратов. Конечно, это сказывается и на успехи самого онкологического заболевания. То есть итог – ухудшение результатов лечения. Таких работ достаточно много.
Другая проблема, которая существует при использовании хим. препаратов у онкологических пациентов. Что мы знаем о механизмах и патогенезе гепатотоксичности при химиотерапии? Механизмы лекарственного поражения печени – гораздо сложнее, чем мы себе это представляем. Вот здесь я представила наиболее важные моменты. Это нарушение метаболических процессов в гепатоцитах, токсическая деструкция субклеточных структур, индукция иммунных реакций, канцерогенез, нарушение кровоснабжения гепатоцитов и обострение ранее имевшегося гепатоцеллюлярного поражения.
В данной табличке представлены группы противоопухолевых препаратов, которые могут вызывать различные виды гепатотоксичности. К ним относятся алкилирующие агенты, и антиметаболиты, и производные нитрозомочевины, и противоопухолевые антибиотики. Так же это винкаалколоиды, производные платины, интерфероны, интерлейкины, гормонотерапия, а так же модные сейчас, современные таргетные препараты. И как вы видите, они в той или иной степени повреждают сам гепатоцит – основную клетку печёночную паренхимы.
И чтобы также не быть голословным, я здесь представила работу, достаточно новую, не одну, в которой очень чётко представлено, что при использовании хим. препаратов неоднократно усугубляется лекарственная токсичность, что сопровождается также вероятностью более частого летального исхода при развитии стеатогепатита.
Следующая проблема. Как же диагностировать и оценить гепатотоксичность? Отсутствуют специфические биомаркеры для постановки диагноза лекарственного поражения печения при химиотерапии. Чувствительность традиционных функциональных проб очень низка. Они информативны лишь в диагностике имеющейся патологии, но малополезны в оценке метаболического и экскреторного потенциала печени, и врачу приходится порой очень задумываться, когда он встречается с лекарственным поражением печени. В чём же причина? Как поступить в данной ситуации? В клинике мы для оценки гепатотоксичности используем классификацию, которая предложена национальным институтом рака, в которой выделены 4 степени поражения печени в зависимости от изменений тех или иных биохимических показателей, как представлено в это табличке. Я не буду её комментировать, потому что при желании вы найдёте её в специальной литературе, она достаточно широко обсуждается.
В клинике, всё-таки, в первичной диагностике лекарственных поражений печени мы чаще всего используем вот эти критерии диагностики, которые были представлены ещё в 90-х годах Советом международных медицинских научных организаций, до сих пор не претерпели каких-либо изменений. И особенность этих критериев заключается в том, что здесь нам не нужно никакого специального инструментального исследования, и учитываются лишь абсолютные значения активности ферментов. Хочу только подчеркнуть их относительные величины к высшей границе нормы. В зависимости от этого выделяют гепатоцеллюлярные поражения, холестатические поражения и смешанный тип поражения.
Мониторинг АЛТ, как метод диагностики в онкологии при лекарственной гепатотоксичности, всё-таки имеет право на существование. Здесь я представила достаточно новую работу, где показано, что чувствительность, специфичность и диагностическая точность достаточно высоки. Но этот метод имеет и свои ограничения, потому что мы знаем, что повышение трансаминаз больше 3 норм отмечается у 1% пациентов при использовании плацебо. Мониторинг АЛТ не позволяет нам идентифицировать идиосинкразические реакции, которые наиболее часто мы отмечаем при использовании хим. препаратов. И режим мониторинга АЛТ часто нарушается в реальной клинической практике.
Следующая проблема, которая стоит перед специалистами-онкологами, которые занимаются лечением, которые используют химиотерапию в лечении онкологических пациентов – как же «защитить печёночную клетку» при химиотерапии? Как же выбрать гепатопротектор? Выбор гепатопротектора должен основываться в первую очередь на принципах доказательной медицины. Это наша точка зрения. Я хочу сегодня остановиться на препарате гептрал или адеметионин, который имеет широкую доказательную клиническую базу, востребован и широко применяется в онкологической клинике. Вот здесь ссылка «уровень доказательности» I при алкогольном циррозе, то есть по общей смертности и смертности от заболеваний печени. Также «уровень доказательства» I у гептрала при эффективности воздействия на показатели биохимические у больных пациентов с холестазом. Это достаточно большое исследование на большом количестве пациентов. А также «уровень доказательности» II при оценке эффекта гептрала при астении и усталости тоже на большом количестве пациентов.
Почему мы говорим об S-адеметионине или о гептрале? Это физиологический метаболит, дефицит которого наблюдается при всех патологиях печени, в том числе при гепатотоксичности. Он выполняет важную роль в метаболических процессах, реакциях трансметилировании, транссульфировании, аминопропилировании. Назначая гептрал, врач всегда предполагает его детоксикационный эффект, антиоксидантный, антидепрессивный, нейропротективный, регенерирующий, холеретический и холекинетический эффекты.
Каковы же преимущества гептрала перед другими препаратами целенаправленного действия на печёночную клетку? Это достаточная абсорбция, естественный метаболизм при патологии печени – наличие эффекта первого прохождения через печень и отсутствие токсичности. Немножечко поясню. Очень часто, открывая инструкцию, пациент видит, что при пероральном приёме лишь 5% обладает биодоступностью. Да, действительно, вы должны объяснить пациенту 5%, потому что 95% этого препарата непосредственно включается в метаболизм в печени. Выраженная способность предупреждать или нейтрализовать образование высокоактивных повреждающих соединений, снижать воспаление, подавлять формирование соединительной ткани, стимулировать процессы регенерации – это реакция аминопропилирования. И наличие двух форм применения, что тоже очень важно, особенно в онкологии для достижения быстрого эффекта, потому что у онколога порой не бывает времени для того, чтобы не продолжить химиотерапию этой серьёзной болезни.
Как же применять гептрал у онкологических пациентов при проведении химиотерапии? Это парентеральное введение, пероральный приём, ступенчатая терапия, и комбинация внутривенного и перорального способов применения для того, чтобы ускорить эффект действия данного препарата. И гептрал в программах сопроводительной терапии в онкологии при лекарственных поражениях печени обладает лечебным и профилактическим эффектом, повышая эффективность химиотерапии, а так же антидепрессивный эффект и лечение разных форм печёночной энцефалопатии. Улучшение субъективного состояния и изменения качества жизни пациентов, потому что это очень важно, немножко позже я скажу об этом.
Каковы же проблемы ещё, которые встают при развитии гепатотоксичности при химиотерапии? Профилактика или лечение – какой же подход выбрать, какой оптимален? И вот я хочу представить наш опыт в практику врача-онколога. Во-первых, при развитии гепатотоксичности нам приходится снижать дозы цитостатиков при критерии, которые представлены ВОЗ. Но не всегда в практике мы придерживаемся этого, особенно если брать больных гематологического профиля в онкогематологии, когда есть первичное поражение печени, когда мы можем подарить шанс на излечение нашему пациенту.
Рациональный подход к предупреждению гепатотоксичности лекарственных средств при невозможности их отмены – предшествующее или одновременное назначение препарата гептрал. Предшествующее или одновременное назначение гептрала у многих пациентов позволяет проводить полноценные протоколы химиотерапии, не изменяя их режимов, не изменяя их доз. И вот здесь показана в этой работе, достаточно недавно эта работа опубликована, показана эффективность профилактического использования адеметионина на больных онкологического профиля. Здесь больные, которые имеют раковую опухоль толстой кишки, использовалась FolFox-терапия, которая включала фторурацил, оксаплатин, лейковарин и элоксатин. И показано, что у пациентов, которые принимали адеметионин в дозе 800 миллиграмм, профилактически у них ни одноного пациента не было отмены терапии, и лишь у 11% пациентов был отсрочен курс, если сравнивать с группой, у которой адеметионин не использовался в качестве профилактики. И снижение доз также было значительно меньше у пациентов, которые получали адеметионин.
Назначение гептрала «по факту печёночной токсичности» целесообразно для препаратов с низкой вероятностью развития гепатотоксических реакций (антибиотики, нестероидные противовоспалительные средства, статины), которые наши пациенты достаточно часто получают в программах сопроводительной терапии.
Говоря о гепатотоксичности, я не могу остановиться и не сказать о печёночной энцефалопатии. Мы знаем, что печень – это центральный орган образования и обезвреживания аммиака, и развитие печёночной энцефалопатии – это комплекс потенциально обратимых нервно-психических нарушений, которые возникают в результате печёночной недостаточности и портосистемного шунтирования крови. То есть мы знаем, что наши многие пациенты получают амбулаторную химиотерапию, и при развитии печёночной комы, печёночной энцефалопатии, мы обязаны этих пациентов госпитализировать в стационар, потому что это возможно излечить и дать шанс больному продолжить полноценную жизнь. Говоря о печёночной энцефалопатии, хочу особое внимание обратить на минимальную печёночную энцефалопатию, которая регистрируется у 85% пациентов. Как я уже говорила, что наши пациенты многие получают амбулаторную химиотерапию, и это развитие минимальной печёночной энцефалопатии, которая требует специальных тестов диагностики, которые не всегда используются в клинике, она может быть стадией – предвестником развития клинически выраженной печёночной энцефалопатии. И психические нарушения, которые возникают у пациентов, мы очень часто говорим, пациент, который получает химиотерапию, у него меняется характер, он становится скверным. Это может оказывать отрицательное влияние на качество жизни пациентов.
Терапия минимальной печёночной энцефалопатии остаётся предметом дискуссий. Здесь я привожу схему, которую мы используем при лечении наших пациентов. И при хронической печёночной энцефалопатии в период ремиссии, также необходимо принимать курсовые дозы, которые режимы, и длительность приёма определяется врачом, который с данным пациентом работает.
И необходимо, хочу призвать всех врачей, разрабатывать стандарты сопроводительной терапии и создавать междисциплинарные протоколы профилактики гепатотоксичности при химиотерапии в Российской Федерации, потому что их нет, а тема очень актуальна. Это приведёт к повышению эффективности лечения онкологических пациентов.
И хочу предложить всё-таки вопросы для дискуссии. Это алгоритм обследования при лекарственной гепатотоксичности, выбор гепатопротектора, схемы применения гепатопротекторов, лечение по «факту» или профилактическое назначение гепатопротекторов, терапия хронической лекарственной печёночной недостаточности, и терапия минимальной печёночной энцефалопатии.
Благодарю за внимание!
Профессор Драпкина О.М.: – Спасибо большое, Вера Борисовна! У нас ещё 7 минут, и вам пришли вопросы. Можно ли назначать химиотерапию пациентам с высоким уровнем трансаминаз на фоне вирусного гепатита?
Профессор Ларионова В.Б.: – Вопрос сложный. Я думаю, что вы не будете на фоне высоких трансаминаз назначать. Во-первых, причина повышения трансаминаз. Обусловлена она самим вирусным гепатитом или она обусловлена всё-таки воздействием хим. препаратов? Это очень важно, потому что порой я сама занимаюсь химиотерапией гемобластозов, и порой мы пациенту проводим сначала противовирусную терапию, проводим применение гепатопротекторов, а потом назначаем уже химиотерапию, потому что риск огромный потерять пациента на фоне лечения. У нас есть такие пациенты, достаточно много, особенно в гематологии.
Профессор Драпкина О.М.: – Вопрос по поводу гептрала: во время или после химиотерапии?
Профессор Ларионова В.Б.: – Это вопрос дискутабельный. Я уже сказала, у нас есть свой опыт уже ведения этих больных. Если больной относится к группе риска, мы этим пациентам даём на фоне химиотерапии гептрал – обязательно. У нас это уже отработано.
Профессор Драпкина О.М.: – Есть ли противопоказания у пациентов с онкологическими заболеваниями в применении гептрала?
Профессор Ларионова В.Б.: – Нет.
Профессор Драпкина О.М.: – Нет. И последний вопрос: какая группа препаратов для химиотерапии требует наиболее пристального мониторинга поражения печени?
Профессор Ларионова В.Б.: – Я вот показала те препараты, которые уже генетически имеют токсичность. К ним относятся метотрексат, циклофосфан, препараты платины, а также полихимиотерапия. И вот мы уже наблюдали таргетные препараты, в частности препарат велкейд, когда мы у пациентов из группы риска, пациент, который был курильщиком, который принимал алкоголь, у него трансаминазы зашкаливали уже после первого курса велкейда. Мы ему провели лечение гептралом, но это заняло, больной с миеломной болезнью, достаточно длительно, где-то около трёх недель, но в последующем, мы немного редуцировали дозы велкейда, изменили режим, но продолжили на фоне гептрала и сейчас он проводит трансплантацию с успехом этот пациент.
Профессор Драпкина О.М.: – Спасибо большое, Вера Борисовна! Спасибо!
Профессор Ларионова В.Б.: – Пожалуйста!