Как подключают больного к ивл
Искусственная вентиляция легких (ИВЛ): инвазивная и неинвазивная респираторная поддержка
К искусственной вентиляции легких (ИВЛ) прибегают для оказания помощи пациентам с острой или хронической дыхательной недостаточностью, когда больной не может самостоятельно вдыхать необходимый для полноценного функционирования организма объем кислорода и выдыхать углекислый газ. Необходимость в ИВЛ возникает при отсутствии естественного дыхания или при его серьезных нарушениях, а также во время хирургических операций под общим наркозом.
Что такое ИВЛ?
Искусственная вентиляция в общем виде представляет собой вдувание газовой смеси в легкие пациента. Процедуру можно проводить вручную, обеспечивая пассивный вдох и выдох путем ритмичных сжиманий и разжиманий легких или с помощью реанимационного мешка типа Амбу. Более распространенной формой респираторной поддержки является аппаратная ИВЛ, при которой доставка кислорода в легкие осуществляется с помощью специального медицинского оборудования.
Показания к искусственной вентиляции легких
Искусственная вентиляция легких проводится при острой или хронической дыхательной недостаточности, вызванной следующими заболеваниями или состояниями:
Инвазивная вентиляция легких
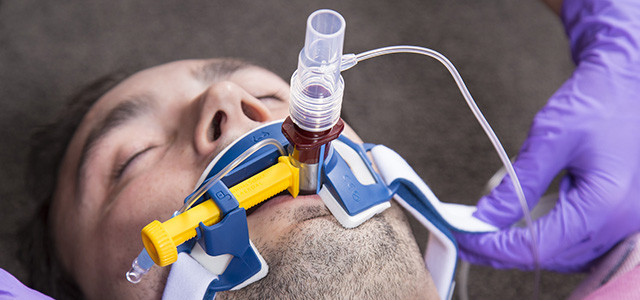
Эндотрахеальная трубка вводится в трахею через рот или через нос и подсоединяется к аппарату ИВЛ
При инвазивной респираторной поддержке аппарат ИВЛ обеспечивает принудительную прокачку легких кислородом и полностью берет на себя функцию дыхания. Газовая смесь подается через эндотрахеальную трубку, помещенную в трахею через рот или нос. В особо критических случаях проводится трахеостомия – хирургическая операция по рассечению передней стенки трахеи для введения трахеостомической трубки непосредственно в ее просвет.
Инвазивная вентиляция обладает высокой эффективностью, но применяется лишь случае невозможности помочь больному более щадящим способом, т.е. без инвазивного вмешательства.
Кому и когда необходима инвазивная ИВЛ?
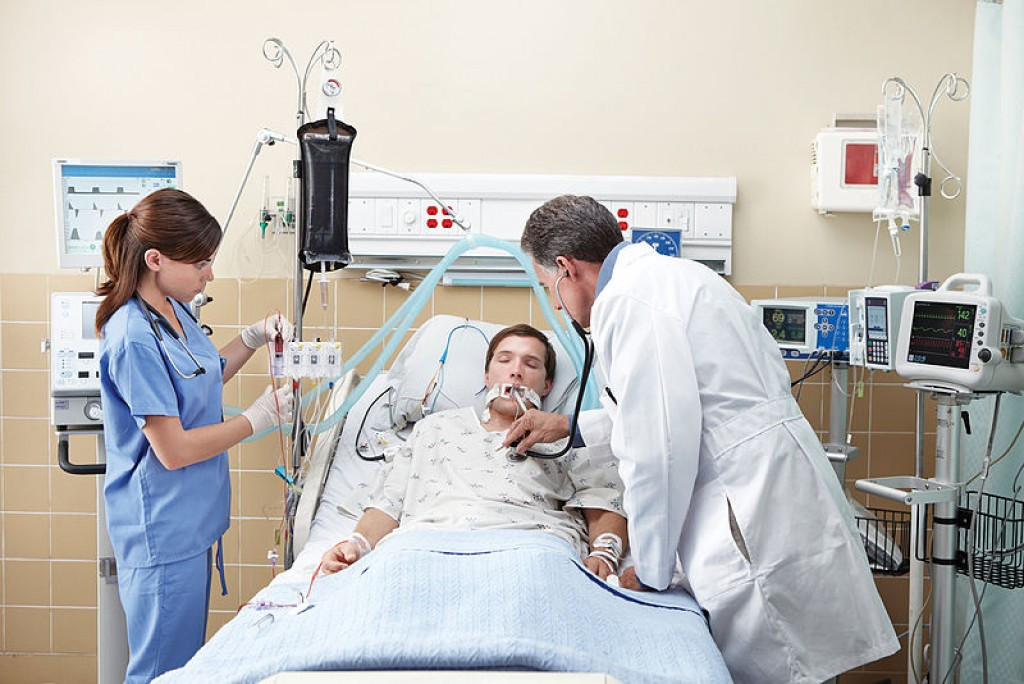
Подключенный к аппарату ИВЛ человек не может ни говорить, ни принимать пищу. Интубация доставляет не только неудобства, но и болезненные ощущения. Ввиду этого пациента, как правило, вводят в медикаментозную кому. Процедура проводится только в условиях стационара под наблюдением специалистов.
Инвазивная вентиляция легких отличается высокой эффективностью, однако интубация предполагает введение пациента в медикаментозную кому. Кроме того, процедура сопряжена с рисками.
Традиционно инвазивную респираторную поддержку применяют в следующих случаях:
Как работает аппарат инвазивной ИВЛ?
Принцип работы приборов для инвазивной ИВЛ можно описать следующим образом.
Особенности оборудования для инвазивной вентиляции
Оборудование для инвазивной вентиляции легких имеет ряд характерных особенностей.
Неинвазивная вентиляция легких
За последние два десятилетия заметно возросло использование оборудования неинвазивной искусственной вентиляции легких. НИВЛ стала общепризнанным и широко распространенным инструментом терапии острой и хронической дыхательной недостаточности как в лечебном учреждении, так и в домашних условиях.
Одним из ведущих производителей медицинских респираторных устройств является австралийская компания ResMed
НИВЛ — что это?
Неинвазивная вентиляция легких относится к искусственной респираторной поддержке без инвазивного доступа (т.е. без эндотрахеальной или трахеостомической трубки) с использованием различных известных вспомогательных режимов вентиляции.
Оборудование подает воздух в интерфейс пациента через дыхательный контур. Для обеспечения НИВЛ используются различные интерфейсы – носовая или рото-носовая маска, шлем, мундштук. В отличие от инвазивного метода, человек продолжает дышать самостоятельно, но получает аппаратную поддержку на вдохе.
Когда применяется неинвазивная вентиляция легких?
Ключом к успешному использованию неинвазивной вентиляции легких является признание ее возможностей и ограничений, а также тщательный отбор пациентов (уточнение диагноза и оценка состояния больного). Показаниями для НИВЛ являются следующие критерии:
Как подключают больного к ивл
Метод проведения ИВЛ способом «изо рта в рот» самый эффективный, однако, при оральном контакте возможна передача многих видов инфекции. Как предохранить себя от этого? Рекомендуется использование нескольких способов.
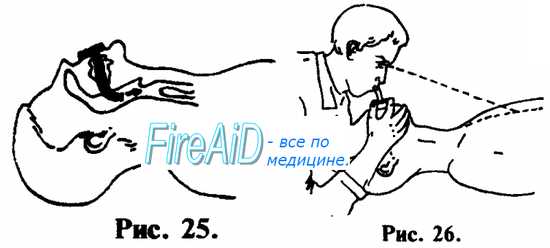
1. При возможности, лучше производите ИВЛ через S-образный воздуховод, или воздуховод любой другой конструкции (см. рис. 25, 26).
2. Если нет воздуховода, используйте прокладку из 2-х слоев марли, но не более. При 3—4 и более слоях марли, проведение ИВЛ будет затруднительно чисто физически. То же самое можно сказать и в отношении попыток производить ИВЛ, используя в качестве прокладки носовой платок или любую другую материю.
3. После проведения реанимационного пособия, включавшего в свой состав производство ИВЛ методом «рот в рот», хорошо прокашляйтесь и прополощите ротовую полость любым антисептическим раствором или, в крайнем случае, водой.
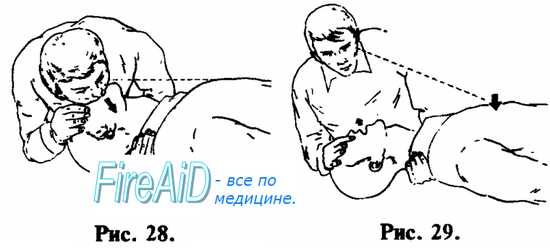
ИВЛ методом «изо рта в рот» осуществляется следующим образом. Оказывающий помощь одной рукой, помещенной на лбу пострадавшего, отгибает его голову назад, одновременно поддерживая ее другой рукой, подложенной под шею и затылок (см. рис. 27). Пальцами руки, расположенной на лбу, закрывают нос, чтобы не было утечки воздуха. Оказывающий помощь плотно охватывает своим ртом рот пострадавшего и производит выдох в его дыхательные пути. Критерий контроля эффективности — увеличение объема грудной клетки пострадавшего (см. рис. 28). После того, как грудная клетка расправилась, оказывающий помощь поворачивает свою голову в сторону и у больного происходит пассивный выдох (см. рис. 29). Интервалы дыхательных циклов должны быть в пределах физиологической нормы — не чаще 10—12 в 1 мин. (1 дыхательный цикл на 4—5 счетов). Объем выдыхаемого воздуха должен быть примерно на 50% больше обычного объема.
Если реаниматор действует в одиночку, отношение частоты сдавливаний грудной клетки к темпу ИВЛ должно составлять 15:2. В этих случаях проверяют пульс после завершения четырех циклов ИВЛ, а затем каждые 2—3 мин. Не стремитесь делать ИВЛ в режиме максимальных вдохов и выдохов в сочетании с большой частотой. Это чревато возникновением осложнений уже у реаниматора.
На фоне усиленной искусственной гипервентиляции, да еще в сочетании с естественным волнением за судьбу больного, может очень быстро развиться декомпенсированный дыхательный алкалоз с кратковременной потерей сознания, что создаст дополнительные трудности членам реанимационной бригады.
К проведению ИВЛ методом «изо рта в нос» прибегают в том случае, если нет возможности использовать вышеуказанный метод (например, при челюстно-лицевых травмах). Сразу следует отметить, что проводить ИВЛ данным способом более тяжело чисто физически. В основе этого лежат анатомические особенности верхних дыхательных путей (нос, носоглотка): они значительно уже просвета ротовой полости. Методика проведения данного пособия заключается в следующем. Оказывающий помощь одной рукой, расположенной на лбу пострадавшего, запрокидывает его голову назад, а другой рукой поднимает нижнюю челюсть вверх, закрывая рот (см. рис. 30). Дополнительно можно закрыть рот пострадавшего пальцами руки, поднимающей челюсть. Затем реаниматор охватывает нос пострадавшего своими губами и производит выдох (см. рис. 31). Оценка эффективности ИВЛ — см. выше.
При проведении ИВЛ у детей, учитывая небольшое расстояние между носом и ртом, следует сразу захватывать своими губами рот и нос пострадавшего, частота дыхания должна быть не менее 18—20 в 1 мин., с соответствующим уменьшением дыхательного обьема (ориентиром частоты дыхания и дыхательного объема могут служить величины нормы для конкретного возраста).
Предотвращению раздувания желудка при отсутствии интубации трахеи способствует поддержание дыхательных путей в открытом состоянии не только во время вдоха (медленное выполнение которого обеспечивает реаниматор), но и во время пассивного выдоха. Несмотря на это, раздувание желудка все же возможно, особенно если реаниматор один (в одиночку непрерывно поддерживать дыхательные пути в открытом состоянии невозможно).
В стремлении уменьшить растяжение желудка нельзя надавливать на область эпигастрия (это вызывает рвоту, если желудок наполнен). Вместо этого продолжают основные реанимационные мероприятия, уделяя особое внимание правильному проведению ИВЛ. Для проведения ИВЛ можно использовать дыхательный мех (мешок Амбу). Он улучшает физиологические параметры ИВЛ (пострадавший получает атмосферный воздух, не выдыхаемый; бесспорно, этот способ более гигиеничен). Трахеостомия ургентно не выполняется, т. к. даже самый высококлассный специалист быстрее, чем за 3 мин., ее не сделает.
Проведение вспомогательной ИВЛ
Когда пациенту не под силу самостоятельно делать вдохи, его жизнь спасает вспомогательная искусственная вентиляция легких. Данная процедура обеспечивает в механическом режиме естественное, ритмическое нагнетание воздуха в альвеолы легких. Но выдох при этом осуществляется в пассивном режиме при помощи легких и грудной клетки пациента. Таким образом, поддерживается нормальный уровень кислорода в крови болеющего человека.
Клинические показания к ВИВЛ:
Способы вспомогательной ИВЛ
Существует два современных, аппаратных метода вспомогательной ИВЛ: триггерный и адаптационный. В зависимости от того, полностью или частично тяжелобольной может дышать, подбирают тот или иной способ.
Триггерный способ
Для применения триггерного метода необходима специальная аппаратная система с распределением устройства с вдоха на выдох (либо же, наоборот) в момент дыхательного усилия пациента. Триггерный блок (система «откликания») регулируется согласно показателям давления, интенсивности самостоятельных выдохов пациента и скорости поступления воздуха в альвеолы легких. Особенно важно «время задержки». Вспомогательный вдох системы «откликания» в строгом порядке должен соответствовать началу, а не концу самостоятельного вдоха пациента. Если триггерный блок будет плохо отрегулирован, то больному человеку придется прилагать слишком большое усилие, чтобы привести в движение автоматический вспомогательный вдох. А общее самочувствие пациента не всегда позволит сделать это. Либо же будет происходить секундная задержка активации вспомогательного вдоха. Тогда больной уже будет выдыхать воздух, но триггерный блок еще не завершит вспомогательный вдох. Вместо полноценной адаптации пациенту придется тратить значительно больше усилий, чтобы пересилить возникающие дискомфортные ощущения и приспособиться к ритму блока. И хотя в наши дни доктора профессионально настраивают триггерную систему, все же этим способом пользуются ограниченно. Потому как в бессознательном состоянии пациент даже жестами не подтвердит отсутствие затруднений в период проведения процедуры и терпимое самочувствие.
Адаптационный способ
Широко применяется на практике адаптационный метод ВИВЛ. В этом случае аппарат работает в автоматическом режиме. При этом тяжелобольной хоть и продолжает самостоятельно дышать, точнее, делать выдохи, но в тоже время подстраивается под заданный ритм дыхательного аппарата. Адаптационный период пациента проходит намного продуктивнее. Так как все параметры блока строго соответствуют «спонтанному» дыханию больного. К этому способу прибегают доктора в том случае, когда тяжелобольной способен дышать самостоятельно.
Оказание помощи методами вспомогательной ИВЛ может длиться пару часов или несколько месяцев, в зависимости от степени тяжести больного. В последнем случае, чтобы убедиться в хорошей адаптации пациента к респиратору, контролируют следующие симптомы: идентичные шумы в легких с обеих сторон, естественный окрас кожных покровов без испарины, нормальные показатели пульса и АД.
Как подключают больного к ивл
Проблема поражения легких при вирусной инфекции, вызванной COVID-19 является вызовом для всего медицинского сообщества, и особенно для врачей анестезиологов-реаниматологов. Связано это с тем, что больные, нуждающиеся в реанимационной помощи, по поводу развивающейся дыхательной недостаточности обладают целым рядом специфических особенностей. Больные, поступающие в ОРИТ с тяжелой дыхательной недостаточностью, как правило, старше 65 лет, страдают сопутствующей соматической патологией (диабет, ишемическая болезнь сердца, цереброваскулярная болезнь, неврологическая патология, гипертоническая болезнь, онкологические заболевания, гематологические заболевания, хронические вирусные заболевания, нарушения в системе свертывания крови). Все эти факторы говорят о том, что больные поступающие в отделение реанимации по показаниям относятся к категории тяжелых или крайне тяжелых пациентов. Фактически такие пациенты имеют ОРДС от легкой степени тяжести до тяжелой.
В терапии классического ОРДС принято использовать ступенчатый подход к выбору респираторной терапии. Простая схема выглядит следующим образом: низкопоточная кислородотерапия – высокопоточная кислородотерапия или НИМВЛ – инвазивная ИВЛ. Выбор того или иного метода респираторной терапии основан на степени тяжести ОРДС. Существует много утвержденных шкал для оценки тяжести ОРДС. На наш взгляд в клинической практике можно считать удобной и применимой «Берлинскую дефиницую ОРДС».
Общемировая практика свидетельствует о крайне большом проценте летальных исходов связанных с вирусной инфекцией вызванной COVID-19 при использовании инвазивной ИВЛ (до 85-90%). На наш взгляд данный факт связан не с самим методом искусственной вентиляции легких, а с крайне тяжелым состоянием пациентов и особенностями течения заболевания COVID-19.
Тяжесть пациентов, которым проводится инвазивная ИВЛ обусловлена большим объемом поражения легочной ткани (как правило более 75%), а также возникающей суперинфекцией при проведении длительной искусственной вентиляции.
Собственный опыт показывает, что процесс репарации легочной ткани при COVID происходит к 10-14 дню заболевания. С этим связана необходимость длительной искусственной вентиляции легких. В анестезиологии-реаниматологии одним из критериев перевода на спонтанное дыхание и экстубации служит стойкое сохранение индекса оксигенации более 200 мм рт. ст. при условии, что используются невысокие значения ПДКВ (не более 5-6 см. вод. ст.), низкие значения поддерживающего инспираторного давления (не более 15 см. вод. ст.), сохраняются стабильные показатели податливости легочной ткани (статический комплайнс более 50 мл/мбар), имеется достаточное инспираторное усилие пациента ( p 0.1 более 2.)
Достижение адекватных параметров газообмена, легочной механики и адекватного спонтанного дыхания является сложной задачей, при условии ограниченной дыхательной поверхности легких.
При этом задача поддержания адекватных параметров вентиляции усугубляется присоединением вторичной бактериальной инфекции легких, что увеличивает объем поражения легочной ткани. Известно, что при проведении инвазинвой ИВЛ более 2 суток возникает крайне высокий риск возникновения нозокомиальной пневмонии. Кроме того, у больных с COVID и «цитокиновым штормом» применяются ингибиторы интерлейкина, которые являются выраженными иммунодепрессантами, что в несколько раз увеличивает риск возникновения вторичной бактериальной пневмонии.
В условиях субтотального или тотального поражения дыхательной поверхности легких процент успеха терапии дыхательной недостаточности является крайне низким.
Собственный опыт показывает, что выживаемость пациентов на инвазивной ИВЛ составляет 15.3 % на текущий момент времени.
Алгоритм безопасности и успешности ИВЛ включает:
В связи с тем, что процент выживаемости пациентов при использовании инвазивной ИВЛ остается крайне низким возрастает интерес к использованию неинвазивной искусственной вентиляции легких. Неинвазивную ИВЛ по современным представлениям целесообразно использовать при ОРДС легкой степени тяжести. В условиях пандемии и дефицита реанимационных коек процент пациентов с тяжелой формой ОРДС преобладает над легкой формой.
Тем не менее, в нашей клинической практике у 23% пациентов ОРИТ в качестве стартовой терапии ДН и ОРДС применялась неинвазивная масочная вентиляция (НИМВЛ). К применению НИМВЛ есть ряд ограничений: больной должен быть в ясном сознании, должен сотрудничать с персоналом. Допустимо использовать легкую седацию с целью обеспечения максимального комфорта пациента.
Критериями неэффективности НИМВЛ являются сохранение индекса оксигенации ниже 100 мм рт.ст., отсутствие герметичности дыхательного контура, возбуждение и дезориентация пациента, невозможность синхронизации пациента с респиратором, травмы головы и шеи, отсутствие сознания, отсутствие собственного дыхания. ЧДД более 35/мин.
В нашей практике успешность НИМВЛ составила 11.1 %. Зав. ОАИР: к.м.н. Груздев К.А.
Чурсин В.В. Искусственная вентиляция легких (учебно-методическое пособие)
Информация
Физиология дыхания
Анатомия
Проводящие пути
Нос — первые изменения поступающего воздуха происходят в носу, где он очищается, согревается и увлажняется. Этому способствует волосяной фильтр, преддверие и раковины носа. Интенсивное кровоснабжение слизистой оболочки и пещеристых сплетений раковин обеспечивает быстрое согревание или охлаждение воздуха до температуры тела. Испаряющаяся со слизистой оболочки вода увлажняет воздух на 75-80%. Длительное вдыхание воздуха пониженной влажности приводит к высыханию слизистой оболочки, попаданию сухого воздуха в легкие, развитию ателектазов, пневмонии и повышению сопротивления в воздухоносных путях.
Трахея — основной воздуховод, в ней согревается и увлажняется воздух. Клетки слизистой оболочки захватывают инородные вещества, а реснички продвигают слизь вверх по трахее.
Бронхи (долевые и сегментарные) заканчиваются концевыми бронхиолами.
при низком давлении растяжения, уменьшает действие сил, вызывающих накопление жидкости в тканях. Кроме того, сурфактант очищает вдыхаемые газы, отфильтровывает и улавливает вдыхаемые частицы, регулирует обмен воды между кровью и воздушной средой альвеолы, ускоряет диффузию СО2, обладает выраженным антиокислительным действием. Сурфактант очень чувствителен к различным эндо- и экзогенным факторам: нарушениям кровообращения, вентиляции и метаболизма, изменению РО2 во вдыхаемом воздухе, загрязнению его. При дефиците сурфактанта возникают ателектазы и РДС новорожденных. Примерно 90-95% альвеолярного сурфактанта повторно перерабатывается, очищается, накапливается и ресекретируется. Период полувыведения компонентов сурфактанта из просвета альвеол здоровых легких составляет около 20 ч.
увеличением скорости потока (форсирование вдоха или выдоха) сопротивление дыхательных путей увеличивается.
Сопротивление дыхательных путей зависит также от объема легких. При большом объёме паренхима оказывает большее «растягивающее» действие на дыхательные пути, и их сопротивление уменьшается. Применение ПДКВ (PEEP) способствует увеличению объема легких и, следовательно, снижению сопротивления дыхательных путей.
Сопротивление дыхательных путей в норме составляет:
Острая дыхательная недостаточность
Классификация ОДН
В соответствии с вышеизложенным (с позиции оказания экстренной помощи), в первую очередь нужно классифицировать ОДН по тяжести.
Наиболее удобно в реаниматологии классифицировать все синдромы, связанные с органной недостаточностью (точнее – с функциональной недостаточностью того или иного органа) по степени компенсации – способности выполнять свои функции. Любую недостаточность можно разделить на компенсированную, субкомпенсированную и некомпенсированную.
Взяв для аналогии классификации Дембо А.Г. (1957), Rossier (1956), Малышева В.Д. (1989) можно разделить ОДН на:
— Некомпенсированную, когда при выраженных нарушениях механики дыхания не поддерживается нормальный газовый состав крови и уже абсолютно не удовлетворяются метаболические потребности организма. Клинически в состоянии покоя ЧДД более 35 в мин или брадипноэ ( 1, увеличивается физиологическое мертвое пространство, сокращается площадь реального газообмена. Как итог, прогрессирует гипоксемия и гипоксия, которые невозможно компенсировать развивающимся тахипноэ. Для ТЭЛА, кроме того, характерны выраженные гемодинамические нарушения и явления правожелудочковой недостаточности, что усугубляет ситуацию.
Искусственная вентиляция легких
Однако на практике существенное отрицательное влияние ИВЛ на функцию почек наблюдается достаточно редко. Вероятно, положительное влияние на оксигенацию адекватно проводимой ИВЛ все-таки превалирует над отрицательным антидиуретическим эффектом. И в практике автора, и по данным литературы нередки случаи, когда при развивающейся олигурии на фоне гипоксии различного генеза (ОРДС, артериальная гипотен-зия, гестозы) перевод больных на ИВЛ (в комплексе с другой терапией) сопровождался увеличением диуреза вплоть до полиурии. Надо думать, это связано с устранением гипоксии, снижением уровня катехоламинов, купированием спазма артериол и т. д. Прогрессирование олигурии чаще всего обусловлено другой причиной (например, органическими изменениями почек, нескоррегированной гиповолемией, эндогенной или экзогенной интоксикацией).
Возможное отрицательное действие ИВЛ на функцию печени и ЖКТ связано со следующими механизмами:
Принципы работы аппаратов ИВЛ
Существуют несколько способов осуществления цикличности:
— По давлению – аппарат контролирует давление в дыхательном контуре и по заданным величинам давления в конце вдоха и выдоха обеспечивает цикличную ИВЛ. Принцип работы следующий – генератор сжатой газовой смеси (компрессор, турбина) осуществляет вдох – раздувает лёгкие, пока в них не поднимется давление, например до 18 см.вод.ст., после чего срабатывают клапана и лёгким пациента даётся возможность освободиться от избыточного давления, удалив отработанную газовую смесь и снизив давление, например до 0 см вод.ст. Затем опять начинается вдох, опять до достижения 18 см.вод.ст. и т.д. Изменяя величины давления для срабатывания клапанов и производительность генератора можно менять параметры ИВЛ – ДО, ЧД и МОД.
— По частоте – аппарат контролирует время фаз дыхательного цикла – вдоха и выдоха. Зная частоту дыхания и соотношения длительности фаз, можно рассчитать длительность вдоха и выдоха. Например, ЧД – 10 в минуту, значит на один дыхательный цикл (вдох+выдох) уходит 6 секунд. При соотношении вдох:выдох (I:E) – 1:2, длительность вдоха составит 2 секунды, выдоха 4 секунды. Принцип работы следующий – генератор сжатой газовой смеси (компрессор, турбина) осуществляет вдох – раздувает лёгкие в течении 2-х секунд, после чего срабатывают клапана и лёгким пациента даётся возможность освободиться от отработанной газовой смеси в течении 4-х секунд. Изменяя ЧД (и/или I:E) и производительность генератора можно менять ДО и МОД.
— По объёму – аппарат контролирует объём газовой смеси, нагнетаемой в лёгкие пациента, обеспечивая ДО. Затем даётся время для освобождения от отработанной газовой смеси. Изменяя ДО и производительность генератора (МОД), при заданном соотношении I:E, можно изменять ЧД.
Достаточно давно появился (ещё в РО-5), но только сейчас широко используется ещё один принцип управления цикличностью:
— По усилию пациента – когда сам больной инициирует вдох и генератор нагнетает в его лёгкие заданный ДО. В этом случае такие показатели как ЧД и, соответственно МОД, определяются самим пациентом. Эти триггерные (откликающиеся) системы определяют попытки самостоятельного вдоха а) по созданию небольшого отрицательного давления в дыхательном контуре или б) по изменению потока газовой смеси.
В более современном представлении классификацию по принципу обеспечения цикличности можно представить в следующем виде:
— Аппараты или режимы ИВЛ с контролем дыхательного объёма. Работая «по частоте», т.е. в рамках расчётного времени на вдох, аппарат рассчитывает с какой скоростью надо доставить заданный ДО в лёгкие пациента.
— Аппараты или режимы ИВЛ с контролем давления на вдохе. Работая также «по частоте», т.е. в рамках расчётного времени на вдох, аппарат с определённой скоростью и до достижения установленного давления в дыхательных путях, нагнетает в лёгкие пациента ДО, измеряя его величину.