Лютеинизация неовулировавшего фолликула что это
Лютеинизация неовулировавшего фолликула что это
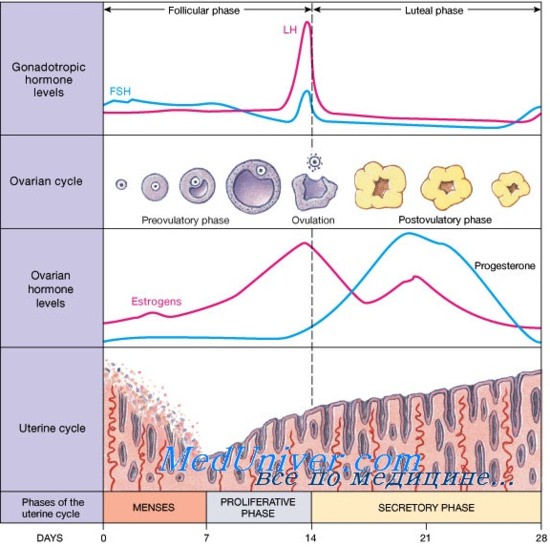
В лютеиновую фазу яичники секретируют прогестерон, что подготавливает эндометрий к имплантации эмбриона. Рецепторы к ЛГ на гранулезных клетках играют важную роль в процессах лютеинизации, способствуя превращению постовуляторного фолликула в желтое тело. Гранулезные клетки становятся гранулезолютеиновыми, получают собственное кровоснабжение и начинают секретировать эстроген и прогестерон. Высвобождение из желтого тела большого количества прогестерона приводит к секреторным изменениям эндометрия и окончательному формированию его рецептивности.
Гонадотропный рилизинг гормон (ГнРГ) и гонадотропины лютеиновой фазы менструального цикла
В лютеиновую фазу частота импульсного выброса ГнРГ уменьшается, а амплитуда возрастает. Изменения частоты выбросов зависят от продолжительности воздействия прогестерона, а изменения амплитуды — от его концентраций.
Содержание ЛГ и ФСГ в лютеиновую фазу достигает минимальных значений за счет повышения концентрации эстрогена, прогестерона и ингибина А. Тем не менее функционирование желтого тела зависит от продолжающегося воздействия минимальных концентраций гипофизарных гонадотропинов в течение всей лютеиновой фазы. Импульсные выбросы ЛГ стимулируют импульсную секрецию прогестерона желтым телом. Более того, уменьшение частоты и амплитуды выбросов ЛГ с помощью агониста ГнРГ в лютеиновую фазу приводит к ее укорочению.
Гормоны яичников лютеиновой фазы менструального цикла
После овуляции происходит лютеинизация гранулезных клеток и клеток theca доминирующего фолликула. Лютеинизация подразумевает как химические, так и морфологические изменения. Гранулезные и клетки theca гипертрофируются и усиливают стероидогенез. Кроме того, разрушение базальной мембраны, ранее разделявшей гранулезные клетки и клетки theca, приводит к прорастанию капилляров в комплекс гранулезо-лютеиновых клеток.
Теперь гранулезолютеиновые клетки приобретают способность синтезировать прогестерон непосредственно из липопротеинов низкой плотности путем расщепления боковой цепи с помощью 3b-гидроксистероиддегидрогеназы. Концентрация мРНК для этих целей достигает максимума в раннюю лютеиновую фазу. Запуск экспрессии рецепторов к липопротеинам низкой плотности гранулезных клеток происходит в ответ на выброс ЛГ и является одним из ранних признаков лютеинизации. Объем секреции прогестерона коррелирует с количеством рецепторов к ЛГ и активностью аденилатциклазы. Пиковой концентрации прогестерон достигает в середине лютеиновой фазы.
Гранулезолютеиновые клетки не могут синтезировать эстрогены непосредственно из холестерина, так как в них нет фермента Р450с17. Однако они сохраняют возможность ароматизировать андрогены, синтезируемые тека-лютеиновыми клетками, до эстрогенов, благодаря чему концентрация последних остается высокой в течение почти всей лютеиновой фазы.
В гранулезолютеиновых клетках синтез ингибина переключается с ингибина В на ингибин А. Соответственно содержание ингибина В в лютеиновую фазу падает до минимума, в то время как концентрация ингибина А достигает максимальных значений. Секреция ингибина А гранулезолютеиновыми клетками регулируется ЛГ. Ингибин А, как и ингибин В, снижает количество ФСГ.
Синдром лютеинизации неовулирующего фолликула
Одной из причин бесплодия является синдром лютеинизации неовулирующего фолликула.
Согласно статистике, синдром достаточно распространен и является причиной возникновения сложностей с зачатием примерно у тридцати процентов женщин фертильного возраста.
Впервые синдром ЛНФ был описан в семидесятые годы XX века.
Как отмечают специалисты, синдром Гейса-Генеса (еще одно название все того же нарушения) достаточно часто присутствует у женщин с бесплодием неустановленной этиологии. Кроме того, он часто сопутствует эндометриозу и, с точки зрения многих специалистов, может расцениваться как его осложнение.
Сам механизм развития синдрома пока изучен недостаточно. По мнению одних авторов, он возникает вследствие неадекватной первой фазы менструального цикла, другие связывают его развитие с дегенерацией клеток фолликула на стадии, предшествующей овуляции, на фоне недостаточной выработки простагландинов.
Есть также гипотеза, указывающая на связь между развитием ЛНФ и нарушениями функций гипоталамо-гипофизарной системы, возникшими вследствие гиперандрогении, психических травм, различных заболеваний, имеющих инфекционную природу и т.д.
Существует версия о том, что в основе ЛНФ лежит низкое давление внутри фолликула и размягчение его стенок, вызванное воздействием протеаз.
Многие специалисты считают, что развитие синдрома во многом обусловлено нарушением синтеза гормонов, вследствие чего в яичниках возникают нарушения эндокринного характера.
Без дополнительных исследований распознать ЛНФ достаточно сложно. Дело в том, что у женщины не происходит видимых нарушений менструального цикла, однако из-за того что овуляция отсутствует, беременность наступить не может, и женщина становится бесплодной.
Для синдрома характерно увеличение длительности второй фазы базальной температуры (повышение температуры), однако при этом разница температур между показателями в первой и второй фазе не велика.
У женщин может наблюдаться слабо выраженное оволосение по мужскому типу.
В процессе УЗ-исследования врачи отмечают небольшое увеличение яичников, которые напоминают поликистозные.
Поскольку патогенез этой патологии так и не определен, какого-то алгоритма лечения не существует. Обычно назначается витаминотерапия. Если существуют воспалительные процессы органов половой системы, назначаются противовоспалительные препараты. Производится гормональная стимуляция овуляции после нормализации уровня пролактина.
После наступления беременности женщины с синдромом ЛНФ должны регулярно наблюдаться у врача. По показаниям наблюдение может происходить в условиях стационара.
Эндокринное бесплодие
К эндокринному бесплодию относятся своеобразные формы дисфункции яичников:
— недостаточность желтого тела или недостаточность лютеиновой фазы (НЛФ);
— синдром лютеинизации неовулировавшего фолликула (ЛНФ).
Недостаточность лютеиновой фазы менструального цикла – это нарушение функции желтого тела. Желтое тело – это временная железа, которая образуется после овуляции и вырабатывает гормон прогестерон.
Менструальный цикл делится на две фазы:
— фолликулярная (от начала менструации до овуляции, длится 12-14 дней);
— лютеиновая фаза (начинается после овуляции, длится 14 дней).
В лютеиновой фазе фолликул трансформируется в желтое тело. При нарушениях функции желтого тела происходит снижение выработки прогестерона. Прогестерон – это женский половой гормон, который поддерживает беременность. Снижение выработки прогестерона ведет к формированию неполноценного эндометрия, который не способен имплантировать оплодотворенную яйцеклетку и развитию беременности.
Симптомы на которые должна обратить внимание женщина:
1. Нарушение менструального цикла (нерегулярные месячные, укорочение цикла, скудные месячные с мажущими выделениями менее трех дней).
2. Самопроизвольное прерывание беременности на первом триместре.
3. Невынашивание беременности.
4. Бесплодие (беременность не наступает при регулярной половой жизни без предохранения в течение 1 года).
Диагностика:
1. УЗИ малого таза. Оценивается рост фолликулов, толщина эндометрия, интенсивность кровотока в яичниках.
2. Измерение базальной температуры.
3. Исследование гормонального статуса (ФСГ, ЛГ, Эстрадиол, Прогестерон, Пролактин).
4. Биопсия эндометрия.
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
Согласно определению ВОЗ (1993), бесплодным считается брак, в котором, несмотря на регулярную половую жизнь в течение года без применения каких-либо контрацептивных средств, беременность не наступает, при условии, что супруги находятся в детородном возрасте.
Согласно данным эпидемиологических исследований, частота бесплодных пар среди супругов детородного возраста колеблется от 8 до 15%. Различают также первичное и вторичное бесплодие, женское и мужское бесплодие.
Первичное женское бесплодие — бесплодие у женщин, живущих регулярной половой жизнью без предохранения и не имевших ни одной беременности; вторичное — беременность в прошлом наступала, но после этого отсутствует в течение 1 года регулярной половой жизни без предохранения. Женское бесплодие — это неспособность женщины к зачатию в репродуктивном возрасте.
Различают первичное, вторичное и абсолютное женское бесплодие. Абсолютное женское бесплодие означает, что возможность беременности полностью исключена (отсутствие матки, яичников и другие аномалии развития половых органов). Выделение этих основных групп не всегда может объяснить все причины бесплодия, поэтому выделена группа больных, с так называемым, необъяснимым бесплодием, причину которого применяемыми методами исследования установить не удается.
Мужское бесплодие — это снижение способности мужчины к зачатию вследствие разнообразных нарушений состояния его здоровья. В основном, это плохое качество спермы, патология сексуальной или семяизвергающей функции. Диагностика и лечение мужского бесплодия находятся в компетенции врача – андролога или уролога. На долю мужского бесплодия приходится 45%.
Причиной бесплодия могут быть нарушения репродуктивной системы у одного или обоих супругов. Стандартизированная программа ВОЗ (1997) по обследованию и лечению бесплодных супружеских пар содержит полный набор клинических и диагностических тестов, в ней выделен 21 фактор женского и 19 факторов мужского бесплодия.
Основными причинами женского бесплодия являются:
Сочетанная форма бесплодия — сочетание мужского и женского бесплодия, встречается до 25% случаев.
 |
Это единый комплекс клинических исследований и анализов, цель которых заключается в выявлении причин бесплодия. Диагностика бесплодия — обязательна для обоих супругов. Это позволяет не только оперативно и точно выявлять истинные причины бесплодия, но и назначать правильное и эффективное лечение. Ведь окончательные выводы относительно нарушений репродуктивных функций мужчины и женщины можно сделать только после всего комплекса диагностических процедур.
Эндокринное бесплодие — это бесплодие, характеризующееся нарушением процесса овуляции. Ановуляция — одна из наиболее частых причин бесплодия. Хроническая ановуляция — гетерогенная группа патологических состояний, характеризующихся нарушением циклических процессов в гипоталамо-гипофизарно-яичниковой системе. Многообразие клинических, биохимических, морфологических нарушений характерно для эндокринного бесплодия.
Клинический спектр эндокринного бесплодия представлен дисфункциональными маточными кровотечениями, олигоменореей, аменореей, при наличии или отсутствии галактореи, гирсутизма, а в ряде случаев — вирилизации. Содержание в крови андрогенов и лютеинизирующий гормон (ЛГ) при ановуляции может быть как нормальным, так и достигать высоких цифр. Размеры яичников также варьируют в широких пределах — от нормальных до увеличенных в несколько раз. Регулярный менструальный цикл наблюдается у 33,2%, нерегулярный — у 23,6 %, аменорея — у 43,2 % из них.
Типичными синдромами, объединяющими такие симптомы как бесплодие, аменорея, олигоменорея и ановуляторные циклы, являются «синдром поликистозных яичников», постпубертатная форма адреногенитального синдрома, различные формы гиперпролактинемии, гиперандрогении, послеродовой нейроэндокринный синдром и другие синдромы. Частота эндокринного бесплодия колеблется от 4 до 40%. Использование современных методов исследования позволяет снизить частоту необъяснимого бесплодия от 7,6 до 4,8%. Недостаточность лютеиновой фазы (НЛФ). Понятие о НЛФ менструального цикла четко не определено, хотя существует довольно давно. НЛФ — это нарушение функции яичников, характеризующееся гипофункцией желтого тела яичника.
Недостаточный синтез прогестерона ведет к недостаточной секреторной трансформации эндометрия, изменению функции маточных труб, нарушению имплантации оплодотворенной яйцеклетки, что клинически проявляется бесплодием либо спонтанным выкидышем в I триместре беременности.
Причины НЛФ менструального цикла:
Диагностика НЛФ (бесплодия)
Диагностика НЛФ основывается на клинических проявлениях и дополнительных методах исследования. Основным симптомом НЛФ может быть бесплодие или скудные кровянистые выделения за 4-5 дней до начала менструации.
При диагностике НЛФ применяют следующие методы:
Лечение НЛФ менструального цикла
Комбинированные эстроген-гестагенные препараты назначают в целях reboud-эффекта в течение 2-3 курсов. Кломифен по обычной схеме: с 5-го по 9-й день цикла по 50 мг, при недостаточном эффекте дозу можно увеличить до 100-150 мг/сут. Кломифен с 5-го по 9-й день цикла, ХГ по 2000-3000 ME 184 2-4-6-й день повышения базальной температуры. Пергонал в сочетании с ХГ. При гиперпролактинемии рекомендуется лечение парлоделом по 2,5-7,5 мг/сут. в течение 4-6 циклов. При гиперандрогении назначают дексаметазон — по 0,25-0,5 мг/сут., дексаметазон с кломифеном. При НЛФ, обусловленной латентной гиперпролактинемией и гиперандрогенией, рекомендуется лечение дексаметазоном — по 0,75 мг/сут. в течение 10 дней, затем по 0,5 мг/сут., и парлоделом по 2,5 мг/сут. Имеются сообщения о благотворном влиянии терапии НЛФ люлиберином.
Имеются сообщения о лечении НЛФ с помощью блокаторов простагландинов (индометацин, напроссин). В заключение следует отметить, что НЛФ — это мультифакториальное патологическое состояние, ведущее к бесплодию. Поэтому и лечение его довольно сложно, эффективность лечения повышается при выяснении причины НЛФ и проведении патогенетической терапии. Профилактика заключается в предупреждении тех патологических состояний, которые способствуют развитию НЛФ.
Причина ЛНФ-синдрома не установлена. Существует точка зрения, что ЛНФ-синдром может быть случайным явлением и встречается не в каждом цикле и что в его возникновении могут играть роль стресс и гиперпролактинемия. Немаловажную роль в развитии ЛНФ-синдрома играют обменные нарушения в самом яичнике, характеризующиеся нарушением синтеза гормонов, ингибинов, статинов, кининов и пр.
Диагноз ЛНФ-синдрома. Наиболее информативными являются ультразвуковая эхография в течение менструального цикла и лапароскопия, производимая во вторую фазу цикла. Лапароскопия: лютеинизированный неовулировавший фолликул характеризуется наличием геморрагического тела без овуляционной стигмы.
Лечение ЛНФ-синдрома. Специального лечения ЛНФ-синдрома не существует, так как этиология и патогенез не установлены. Беременность у больных с ЛНФ наступает одинаково часто на фоне лечения кломифеном и без него.
Лечение ановуляции
В настоящее время существует пять основных методов лечения ановуляции:
Кломифен и беременность
Нарушение функции маточных труб
К нарушению функции маточных труб приводят многочисленные причины: хронический психологический стресс по поводу бесплодия, нарушение синтеза половых гормонов и особенно их соотношения, простагландинов, нарушение глюкокортикоидной функции коры надпочечников и симпатико-адреналиновой системы, увеличение метаболитов простациклина и тромбоксана.
Выраженные нарушения сократительной активности маточных труб отмечаются на фоне гиперандрогении, причем при субклинической форме надпочечниковой гиперандрогении они выражены больше, чем при смешанной яичниково-надпочечниковой гиперандрогении. Доказательством этому является тот факт, что у 54 % женщин трубная беременность наступает на фоне различных гормональных дисфункций, причем у 40 % из них установлена надпочечниковая гиперандрогения. Безусловно, воспалительные процессы в маточных трубах и в области малого таза отражаются на функциональной активности маточных труб.
Непроходимость маточных труб
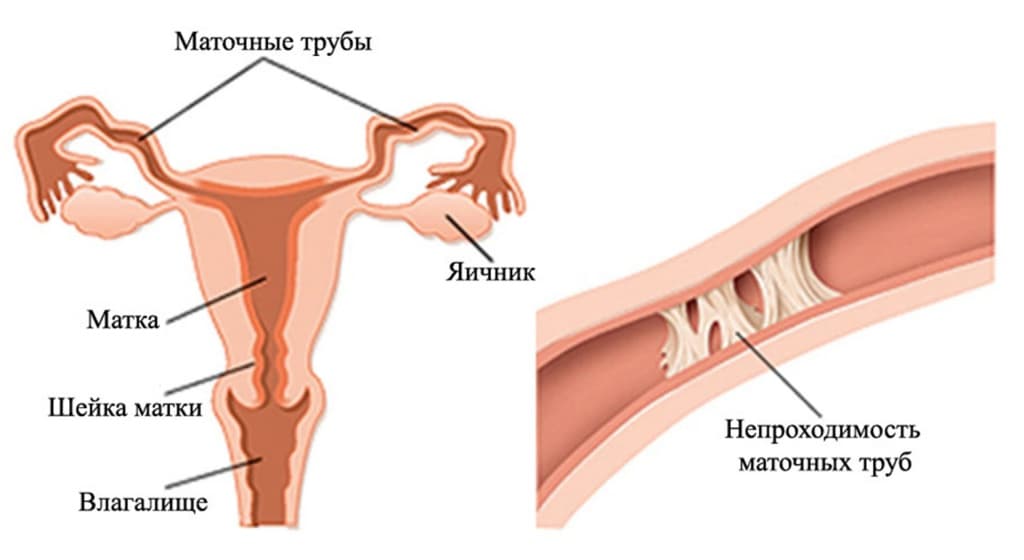
Диагностика трубного бесплодия
Прежде всего, в диагностике трубного бесплодия имеет значение анамнез: указания на хронические воспалительные заболевания половых и других органов и систем (хронический тонзиллит, колит, пиелонефрит, аппендицит), особенности течения послеабортных, послеродовых, послеоперационных периодов; наличие «синдрома тазовых болей», боли при половом сношении, альгодисменорея; частота половых сношений, смена партнеров, воспалительные заболевания у партнеров, характер болей.
Среди методов специального исследования в диагностике трубного бесплодия применяют бактериологическое, кольпоскопию, гистеросальпингографию, рентгенокимографию, кимографическую пертубацию, радио-изотопное сканирование, лапароскопию, микробиопсию маточных труб и др.
Гистеросальпингография (ГСГ) является одним из основных методов диагностики при подозрении на непроходимость маточных труб; ГСГ может дать относительную информацию и о спаечном процессе в малом тазу. Предпочтение отдают проведению ГСГ водными растворами и в первую фазу цикла. Во вторую фазу менструального цикла иногда выраженные секреторные изменения в эндометрии могут явиться препятствием для прохождения контрастного вещества. Временная блокада прохождения контрастного вещества в интерстициальной части маточной трубы может быть вызвана слизистой пробкой, сгустком фибрина, аллергическим отеком слизистой оболочки.
Наиболее информативным методом в диагностике трубного бесплодия является лапароскопия, которую проводят при сомнительных данных ГСГ, а также при бесплодии неясного генеза. Лапароскопию выполняют через 1-3 мес. после ГСГ и через 6 мес. при нормальных данных ГСГ.
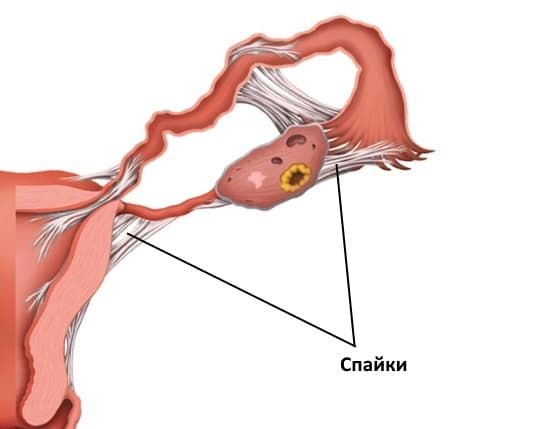
В диагностике перитонеальной формы бесплодия важную роль играют данные анамнеза, указания на перенесенные воспалительные заболевания, оперативные вмешательства на органах малого таза и брюшной полости. Особого внимания заслуживают частые инвазивные процедуры: ГСГ, гидротубации, кимопертубации, диагностические выскабливания. Признаки спаечного процесса (ограничение подвижности и изменение положения матки, укорочение сводов влагалища, тяжистость в области придатков матки) позволяют заподозрить перитонеальную форму бесплодия.
S. Hulka (1978) разработал классификацию, основанную на степени вовлечения в спаечный процесс придатков. При I и II степени распространения спаечного процесса обнаруживают пленчатые, легко разрываемые сращения вокруг маточных труб и яичников. При III и IV степени распространения спаечного процесса в малом тазу спайки чаще бывают плотными, они снабжены сосудами, трудно поддаются разделению; в патологический процесс вовлечены матка, кишечник, сальник. Таким образом, диагностическая ценность двуручного гинекологического исследования, кимографической пертубации, ГСГ высока лишь при выраженных спаечных процессах в малом тазу. Для диагностики менее выраженных процессов необходима лапароскопия.
Лечение трубного бесплодия
Лечение функционального трубного бесплодия (без анатомических изменений) предполагает использование психотерапии, аутосуггестии, седативных средств, транквилизаторов, спазмолитических препаратов, блокаторов простагландинов (напроссин, индометацин) в предовуляторные дни цикла, коррекцию гормональных нарушений. Широкое применение при лечении трубного бесплодия нашла бальнеотерапия — сероводородные ванны и преформированные физические факторы — ультразвук в импульсном режиме, электростимуляция маточных труб.
Лечение трубного бесплодия при органических поражениях маточных труб довольно сложное. Применяют как консервативное, так и оперативное лечение. Консервативная терапия, применяемая при лечении хронического воспаления придатков матки, недостаточно эффективна. При длительном консервативном лечении трубного бесплодия развиваются грубые анатомо-функциональные нарушения в трубах: дистрофические изменения, срастание складок слизистой оболочки, развитие соединительной ткани в слизистом и мышечном слое; нарушается рецепторный аппарат, чувствительность которого к гормонам и без того снижена вследствие хронического воспаления, что обусловливает нарушение процесса стероидогенеза.
При отсутствии эффекта от комплексной консервативной терапии трубного бесплодия в течение 1,5-2 лет показано применение хирургических, в частности, микрохирургических методов лечения.
Успех микрохирургических пластических операций при лечении трубного бесплодия во многом зависит от правильного послеоперационного ведения больных, которое должно включать рассасывающую терапию — электрофорез цинка и меди, магнитотерапию, ультразвук, ферментные препараты, прямую электростимуляцию маточных труб после сальпингостомии, а также ранние гидротубации без гидрокортизона. После операции рекомендуется контрацепция в течение 3-4 мес. В случае необходимости проводят гормональную коррекцию, а также терапию, направленную на восстановление сократительной активности маточных труб.
В последние годы, благодаря внедрению в гинекологию микрохирургии, частота наступления беременности после пластических операций на маточных трубах возросла до 30-60%. Некоторые авторы рекомендуют после таких операций проводить раннюю лапароскопию (через 6-30 дней) с целью лизиса послеоперационных спаек.
Довольно перспективной при лечении трубного бесплодия является оперативная лапароскопия, при которой возможно выполнение сальпингоовариолизиса, коагуляции эндометриоидных гетеротопий и других вмешательств.
Перитонеальная форма бесплодия
При лечении перитонеальной формы бесплодия оптимальной является противовоспалительная терапия (продигиозан, антибактериальные препараты, физические факторы). При наличии операционного лапароскопа во время исследования производят разделение и коагуляцию спаек. Применение эндоскопической хирургии способствовало наступлению беремененности у 31 % женщин, страдающих перитонеальной формой бесплодия.
При трубном бесплодии, обусловленном органическими изменениями, следует шире и на ранних стадиях использовать экстракорпоральное оплодотворение и перенос эмбриона в матку.
Профилактика трубного бесплодия предусматривает профилактику и своевременное лечение воспалительных заболеваний половых органов супругов, рациональное ведение родов и послеродового периода, своевременную диагностику и лечение аппендицита. Профилактика перитонеальной формы бесплодия включает предупреждение и лечение воспалительных заболеваний органов малого таза, рациональное ведение послеоперационного периода и раннюю реабилитацию после оперативных вмешательств на органах малого таза и брюшной полости, ограничение числа гидротубации и широкое использование водорастворимых веществ для производства ГСГ.
Аменорея маточная
Причинами маточной формы аменореи могут быть повторные диагностические выскабливания слизистой оболочки матки; послеродовые и послеоперационные осложнения; воздействие химических прижигающих веществ; эндометриты различной этиологии.
Диагностика маточной формы аменореи основывается на следующих факторах:
субъективные ощущения циклических изменений в организме при сохраненной функции яичников;
обследование по тестам функциональной диагностики и определение уровней Е2 и прогестерона указывает на сохранение функции яичников;
гормональные пробы с прогестероном, комбинированными эстроген-гестагенными препаратами в циклическом режиме отрицательные;
при гистерографии и УЗИ слизистая оболочка матки истончена или имеются внутриматочные синехии;
гистероскопия позволяет уточнить расположение и характер синехий.
Лечение маточной формы аменореи
Заключается в разрушении синехий под контролем гистероскопии сразу же после окончания очередной менструации с назначением циклической гормонотерапии на 2-3 менструальных цикла. После отмены гормонотерапии проводится контрольная ГСГ. В последние годы мы отказались от введения ВМС, которые сами по себе могут поддерживать вялотекущий эндометрит и способствовать образованию синехий. Прогноз при маточной форме аменореи довольно сложный и зависит от степени и глубины поражения базального слоя эндометрия.
Цервикальная форма бесплодия
Играет важную роль в транспорте сперматозоидов. Цервикальная слизь шейки матки представляет собой вязкоэластичный полужидкий гель, состоящий из матрицы нерастворимого гликопротеина (муцина) и воды, содержащей растворимые компоненты. Под влиянием стероидов матрица слизи подвергается структурным изменениям, вызывающим в свою очередь, изменения ее реологических свойств. Цервикальная слизь предотвращает проникновение в матку микроорганизмов и жидкостей; сперматозоиды могут мигрировать через слизь в полость матки, в основном, только в середине менструального цикла. В другие периоды цикла реологические свойства слизи таковы, что миграция сперматозоидов затруднена или невозможна. Предполагают, что структурная особенность гликопротеинов слизи определяет возможность миграции сперматозоидов или ее подавление.
В день овуляции средний диаметр межструктурных каналов в норме составляет 3,21 мкм, при бесплодии — 1,4 мкм; средний диаметр головки сперматозоида 2,5-3 мкм. Размер межструктурных каналов зависит от толщины нитей, которая при бесплодии значительно увеличена. Возможно, это связано с увеличением концентрации в слизи белка плазмы крови, обладающего адгезивными свойствами. При цервикальной форме бесплодия нарушена и геометрия слизи: чаще встречается перекрест нитей слизи. Выявленные изменения объясняют степень гидратации, так как содержание воды увеличивается в фазу овуляции до 98 % по сравнению с 92-94 % в другие фазы менструального цикла. Следовательно, изменение структуры слизи может быть причиной развития цервикального фактора бесплодия. Причины цервикальной формы бесплодия в шеечной слизи: воспалительные изменения; гормональные нарушения, особенно выраженная гипоэстрогения; наличие антител к сперматозоидам; анатомические изменения шейки матки (врожденные или приобретенные — после абортов, родов, операций).
Лечение цервикальной формы бесплодия:
нормализация функций яичников;
барьерная терапия при наличии антител к сперматозоидам предполагает использование презерватива в течение 6 мес. либо применяется внутриматочная инсеминация;
при анатомических изменениях показаны реконструктивно-пластические операции.
Иммуннитет и бесплодие
Бесплодие, обусловленное иммунологическими факторами, относится к числу наименее изученных, частота его составляет около 2%. Это бесплодие обусловлено образованием антиспермальных антител, которые возникают как у мужчин, так и у женщин, причем у последних значительно реже. Известно примерно 40 антигенов эякулята мужчин, к которым образуются антитела. Основными реакциями антиспермального иммунитета являются образование тканевых гуморальных антител и фагоцитоз сперматозоидов. Чаще всего и наиболее активно происходит образование антител в шейке матки, реже — в эндометрии и трубах. Шейка матки является основным звеном так называемого локального иммунитета. В ней образуются иммуноглобулины IgA, кроме того, иммуноглобулины классов IgA, IgJ, IgM абсорбируются из плазмы. Установлено, что концентрация иммуноглобулинов в шейке матки меняется в течение менструального цикла, уменьшаясь в период овуляции. Антитела к антиспермальным антигенам обладают преципитирующими, агглютинирующими, иммуномобилизующими свойствами.
Психогенное бесплодие
У подавляющего большинства женщин с бесплодием выявляются различные нарушения психоэмоциональной сферы: чувство неполноценности, одиночества, истерические состояния в период очередной менструации. Комплекс этих симптомов составляет «симптом ожидания беременности». Нередко беременность наступает в тот момент, когда женщина решает вопрос о прекращении лечения. При изучении психологического статуса у 100 супружеских пар, лечившихся по поводу бесплодия, установили, что у женщин с прервавшейся беременностью отмечена неполная семья в связи с необоснованной критической оценкой супруга, постоянными воспоминаниями о прежних партнерах, высокой производственной загруженностью. У родивших женщин это наблюдалось реже. Показано наблюдение этой группы женщин у невропатолога, психоневролога.
«Синдром гиперстимуляции яичников» (СГЯ)
Классификация синдрома гиперстимуляции яичников:
1. Легкая форма СГЯ:
1-я степень — клиническая симптоматика отсутствует, содержание эстрадиола в плазме более 150 мкг, в моче прегнадиола выше 10 мг;
2-я степень — к этим биохимическим изменениям присоединяется увеличение яичников до 5 см в диаметре.
2. Форма средней тяжести СГЯ:
3-я степень — боли, чувство тяжести внизу живота и изменения, описанные во 2-й степени;
4-я степень — присоединяется тошнота, рвота, понос, размеры яичников — более 5 см в диаметре.
3. Тяжелая форма СГЯ:
5-я степень — к описанным симптомам присоединяется асцит, гидроторакс, яичники более 12 см в диаметре;
6-я степень — состояние крайне тяжелое, помимо асцита и гидроторакса развивается гиперкоагуляция, уменьшается перфузия почек, осложняющаяся олигурией и почечной недостаточностью; яичники резко увеличены, отмечают их разрывы и перекрут.
При анализе СГЯ отмечают, что при стимуляции кломифеном указанный синдром протекает в более легкой форме, применение гонадотропных препаратов в 4 раза чаще приводит к развитию синдрома; установлена также прямая связь между дозой и длительностью применения гонадотропных препаратов. Чаще всего тяжелые формы синдрома гиперстимуляции яичников наблюдают при применении агонистов РГ ЛГ.
Лечение гиперстимуляции яичников. При легкой форме СГЯ во время лечения необходимо динамическое ультразвуковое наблюдение за размерами яичников, желательно определение эстрадиола плазмы.
При СГЯ средней тяжести помимо наблюдения, назначают глюкокортикоидные, антигистаминные, антипростагландиновые препараты. Рекомендуется активированный уголь. Как правило, симптомы гиперстимуляции яичников проходят через 3-6 недель от начала их проявления, при наступлении беременности могут длиться несколько дольше. Тяжелая форма СГЯ требует интенсивного лечения.
В связи с тем, что в основе патогенеза синдрома гиперстимуляции яичников лежит острый переход жидкой части крови в брюшную, плевральную полости и перикард, тактика лечения должна быть направлена на восстановление и поддержание объема циркулирующей крови. Показано внутривенное капельное введение растворов, способствующих удержанию жидкости в кровяном русле (плазма, протеин, альбумин). Одновременно, для стимуляции диуреза в случаях олиго- или анурии, показано использование низкомолекулярных декстранов, способствующих изменению реологических свойств крови. Из них наиболее показаны реополиглюкин и поливинилпирролидон. В качестве трансфузионных сред, способствующих восстановлению водно-электролитного баланса, целесообразно применение гемодеза, неокомпенсана и других растворов. Для снижения проницаемости капилляров показано применение кортикостероидных, антипростагландиновых и антигистаминных препаратов.
В случае тромбоэмболии или резкого повышения гемокоагуляции целесообразна терапия антикоагулянтами. При прогрессирующем асците рекомендуется аспирация жидкости через задний свод влагалища. Процедура проводится под ультразвуковым контролем, во избежание повреждения увеличенного в размерах яичника.
Консервативную терапию следует проводить под контролем определения электролитов, белка, остаточного азота и мочевины, альдостерона, гематокрита и коагулограммы крови; учета гемодинамических показателей, количества введенной и выделенной жидкости и массы тела.
Показанием к хирургическому лечению являются симптомы внутреннего кровотечения вследствие разрыва яичника. Объем оперативного вмешательства должен быть щадящим — с максимальным сохранением яичниковой ткани.
Для профилактики СГЯ следует проводить тщательный отбор больных, подлежащих стимуляции овуляции, с учетом исходного уровня эстрогенов мочи или крови, а также величины яичников. Дозы гонадотропинов и кломифена должны подбираться индивидуально. Лечение следует начинать с небольших доз, по мере необходимости постепенно повышая их. Крайне важным является тщательное ежедневное наблюдение за общим состоянием больных, размерами яичников в период лечения и в течение 2-3 недель после его отмены. При лечении гонадотропинами желателен ежедневный контроль за уровнем эстрогенов в плазме крови, а также УЗИ, позволяющее следить за величиной яичников и величиной фолликула.
Профилактика гиперстимуляции яичников
Основными мерами профилактики СГЯ являются:
прекращение стимуляции при выраженной тенденции к развитию СГЯ или снижение дозы гонадотропных препаратов;
отмена введения овуляторной дозы хорионического гонадотропина или поддерживающих доз; аспирация максимально возможного числа фолликулов и кист, возникающих в процессе стимуляции;
отмена процедуры транспорта эмбриона, криоконсервация его и перенос в полость матки в очередном менструальном цикле.
У женщин с синдромом поликистозных яичников и получавших в предыдущих циклах препараты хорионического гонадотропина, а также при наступлении беременности риск развития СГЯ значительно выше. Чаще возникает СГЯ у женщин с высоким уровнем эстрадиола крови перед началом стимуляции суперовуляции, а также у женщин, у которых после стимуляции при эхоскопическом контроле в яичниках обнаруживают множество кистозных образований.
Методы диагностики бесплодия у женщин:
1. Клинические: сбор анамнеза, общее медицинское обследование, гинекологическое исследование;
2. Лабораторно – диагностические:
Тесты функциональной диагностики позволяют оценить уровень эстрогенной насыщенности организма женщины (проводится врачом).
Инфекционное обследование методом ПЦР (урогенитальный соскоб) и ИФА (кровь) (хламидии, микоплазма гениталис, микоплазма гоминис, уреаплазма, гонорея, трихомонада, герпес, цитомегаловирус) и бактериологическое исследование вагинального секрета.
Гормональное обследование крайне необходимо для определения функционального состояния репродуктивной системы и выяснения причин бесплодия.
Ультразвуковое исследование является эффективным, безопасным и не инвазивным методом. Диагностическая ценность этого метода высока, он позволяет выявить образования матки, яичников, внутриматочную патологию, патологию эндометрия, динамику фолликулогенеза и овуляцию. Рекомендуется как обязательный метод обследования при бесплодии.
УЗИ щитовидной железы.
Эндоскопические методы. Лапароскопия и гистероскопия являются наиболее информативными методами обследования, при проведении которых возможно не только точно оценить состояние органов малого таза, полости матки и выявить патологические изменения, но и устранить их.
Методы диагностики мужского бесплодия включают:
Лечение бесплодия методом вспомогательных репродуктивных технологий