Мегалобластная анемия что это такое симптомы у женщин причины возникновения и лечение
Мегалобластная анемия что это такое симптомы у женщин причины возникновения и лечение
Мегалобластическая анемия коренным образом отличается от гипохромной анемии, при которой нарушение касается клеточного созревания (за счет неполноценности синтезирования гемоглобина), равно как и от апластической анемии, при которой нарушается дифференциация «клеток-штамм» в кровяные клетки.
Мегалобластоз — патофизиологические рамки, морфология
Основным нарушением, обусловливающим мегалобластическую морфологию является недостаточное синтезирование ДНК (биохимическими механизмами, описанными далее). Результаты этого дефицита следующие:
а) Увеличивается межмитотическая фаза, во время которой продолжается синтез РНК и белков. Это объясняет утрату количественного равновесия между ДНК и РНК, что, в морфологическом плане проявляется изменением отношения ядро-цитоплазма в пользу последней.
б) Кровяные клетки не подвергаются нормальному числу делений (в основном это касается последних трех делений эритробластического ряда) (Weicker, Rohr), при этом ядро остается большим и выглядит как «молодое », в то время как в цитоплазме развивается характеристика зрелой клетки (асинхронизм созревания ядра и цитоплазмы).
Нарушение механизма деления ядра проявляется атипическими митозами (многополюсными, с тонкими хромосомами, под острым углом и неоднородно распределенными), тенденцией к почкованию ядра и чрезмерным сегментированием (в гранулоцитном и мегакариоцитном рядах), аспектами кариорексиса и ядерных остатков (в эритроидном ряде); при этом наличие полиплоидных клеток (4n, 8n или даже более, с единым или множественным ядром) отражают тяжелый дефицит.
в) Отмеченное мегалобластическое расстройство обусловливает усиленное внутрикостномозговое разрушение этих клеток, пропорционально степени дефицита (неэффективность кроветворения, отражающаяся в высоком уровне лактикодегидрогеназы и билирубина, и ростом «ранней фракции» последней). Показатель разрушения находящихся в кровообращении элементов также высок, а средняя продолжительность жизни эритроцитов равняется 1/2—1/3 нормы.
г) Последствием неполноценного кроветворения является анемия, которая (под стимулирующим влиянием эритропоэтина) способствует развитию эритробластической гиперплазии (при изменении отношения Э:Г, росте клеточной костаномозговой массы и гематопоэтической преобразовании жирного костного мозга), что усиливает дефицит фолиевой кислоты или витамина В12 (за счет увеличенного расхода) и замыкает порочный круг усугублением мегалобластоза и анемии.
В основе количественных и качественных изменений остальных двух костномозговых рядов находятся те же нарушения, которые поражают и эритробластный ряд. Неэффективный грапулоцитопоэз поддерживается не только морфологическими альтерационными изменениями, но также повышением уровня мурамидазы в сыворотке (Perillie).
Неэффективность мегакариопоэза, отмечаемая при мегалобластной анемии, которую подсказывал контраст между ростом общей массы мегакариоцитов костного мозга и периферической тромбоцитопзнией, была подтверждена работами Harker и Finch, установивших среднюю выработку, на ядерную единицу, шести тромбоцитов вместо сорока (норма). Рост разрушения гранулоцитов и тромбоцитов на периферии — возможно путем увеличенной секвестрации селезенкой — может способствовать, в различной степени, развивающейся при этом цитопении.
Подобные клеточные альтерационные изменения наблюдаются и в других клеточных системах, в основном у тех, характерной чертой которых составляет коэффициент быстрого деления, в том числе эпителий пищеварительного тракта (в отдельных случаях и клетки зародыша, плодных придатков). В этом следует искать объяснение некоторых клинических признаков или осложнений (глоссит, затруднения пищеварения, расстройство поглощения, перинатальные осложнения и пр.).
Общим диагностическим элементом мегалобластных анемий является определение мегалобластной морфологии всех кровяных клеток костного мозга и периферической крови.
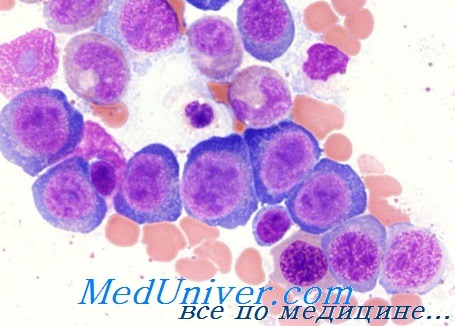
Термином мегалобласт определяются предшественники эритроцитов. В принципе мегалобласт крупнее соответствующего нормального эритробласта с измененным отношением ядро-цитоплазма в пользу последней. Ядро промегалобласта (диаметром 20—30 u) объемистое, нередко расположено эксцентрично, хроматинная структура в виде жемчужин, содержит несколько крупных ядрышек синеватой окраски; цитоплазма синего цвета, наиболее ясная зона расположена вокруг ядра, причем может сохраниться и на последующих стадиях.
На стадии базофильного мегалобласта ядро уменьшается, отсутствуют ядрышка, хроматинная структура более плотная, однако не наблюдаются характерные для базофильного нормобласта скопления, базофильность цитоплазмы станитовся более резкой. На стадии полихроматофильного мегалобласта отражен наиболее ярко асинхронизм созревания между ядром (еще крупным, с едва начинающим организоваться в виде блоков хроматинном) и цитоплазмой (растянутой, полихроматофильной, нередко с наличием телец Жолли). Диаметр оксифильного мегалобласта колеблется от 10 до 18 u, его цитоплазма полностью оксифильная и хроматинная структура ядра еще выявима.
Мегалоцит характеризуется более крупными размерами (от 12 до 14 u), отсутствием ясной центральной зоны (большей толщиной) и часто чуть овальной формой.
Происходящие в гранулоцитном ряде мегалобластические изменения отражаются в увеличенном, в принципе, размере клетки и обильности цитоплазмы. Эти признаки проявляются более четко в гигантских метамиелоцитах, имеющих крупное ядро, весьма скудную хроматинную структуру, не соответствующей форме ядра, при этом цитоплазма продолжает оставаться базофильной. Наблюдается тенденция к гиперсегментированию в результате чего образуется форма гиперсегментированных гранулоцитов (6, 8, 10 и более сегментов), хроматинная структура которых, однако, менее плотная (в отдельных случаях сегментирование частичное, в виде надреза).
Изменения мегакариоцитов менее четкие, в некоторых случаях их размеры отклоняются от нормы, зернистость недостаточная. Хроматинная структура менее плотная, естественная тенденция к сегментированию ядра усиливается, появляются отделившиеся сегменты или сегменты в виде «виноградной грозди» или «взрывных» мегакариоцитов. Тромбоциты крупнее (макро- или даже мегатромбоциты) с лучше выраженной структурой, чем нормальная.
Что касается этиопатогенеза мегалобластической анемии отмечаем, что значительные достижения последних двух десятилетий в изучении этого заболевания привели к выделению следующих трех основных категорий, из них первые две включают случаи, обусловливаемые недостатком витамина В12 и фолиевой кислоты (с возможным их сочетанием при определенных обстоятельствах), а третья — более редкие случаи этого заболевания, независимые от первых двух недостатков, вызываемые известными или еще неизвестными причинами.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Анемия пернициозная (В12-дефицитная, фолиеводефицитная, мегалобластная)
Терминология
Длинный, но не полный список диагнозов-синонимов, послуживший заголовком статьи, нуждается в комментарии; попутно прояснится и содержание этих терминов.
Из чего состоит наша кровь, в чем заключается ее биологическая роль, что такое анемия – этим вопросам посвящены материалы «Клинический анализ крови» и «Анемия. Кровь и бескровие». Более подробно о витаминах группы В можно узнать из статей «Витамин В. Гиповитаминоз» и «Витамин В. Гипервитаминоз».
Пернициозная в переводе с латыни на русский означает «опасная», а в переводе на медицинский – «тяжелая, протекающая злокачественно, прогностически неблагоприятная».
Мегалобластная (иногда пишут «мегалобластическая») означает, что в костном мозге находится большое количество крупных клеток, представляющих собой «недоэритроциты» – одну из промежуточных, незрелых форм красных кровяных телец.
В12 – это витамин (понятно, какой группы), иначе называемый фактором Касла и представленный четырьмя различными кобальтсодержащими веществами с одинаковыми биологическими свойствами, что и позволило выделить их в единую подгруппу витамина В.
Фолиевая (досл. «лиственная») кислота – витамин той же группы, а именно В9.
Таким образом, получаем: опасная, злокачественно протекающая В-витаминодефицитная незрело-эритроцитная анемия. Раньше ее так и называли: злокачественная анемия или злокачественное малокровие. Но еще ее называют болезнью Аддисона-Бирмера или бирмеровой анемией, и вот почему.
В 1822 году симптомы некоего тяжелого заболевания крови впервые упомянул английский врач Дж.С.Комб. В 1849 году его соотечественник, выдающийся врач и ученый Томас Аддисон дал более развернутое описание и толкование. Существенно позже, – в 1871 году, но независимо от Аддисона, – немецкий исследователь Микаэль Антон Бирмер в деталях изучил и охарактеризовал это заболевание, которому дал название прогрессирующая пернициозная анемия.
Позже лечение от анемии напряженно искал американец Уильям Мерфи (от анемии вообще, без нозологического деления), производя эксперименты на искусственно обескровленных собаках. Мерфи кормил их различными продуктами и сравнивал темпы восстановления; его внимание обратила на себя сырая печень. С 1920-х годов усилиями У.Мерфи, Дж.Уиппла и Дж.Майнота пернициозная анемия перестала быть однозначно и стопроцентно летальной болезнью: спасительное лекарство крылось именно в печени. А закончилось все тем, что Мерфи, Уиппл и Майнот в 1934 году получили Нобелевскую премию, – за то, что выделили вещество (группу соединений, как выяснилось), известное сегодня под названием витамин В12.
В серии статей о витаминах Лахта Клиника неоднократно обращала внимание на то, что история открытия и изучения этих удивительных веществ оказалась очень непростой, извилистой, порой драматичной. Но человечество вообще и медицина в частности отличаются невероятным самосохранительным упрямством, когда что-то угрожает нам по-настоящему. Сегодня на очереди сердечнососудистая патология, злокачественные опухоли, вирусные гепатиты, аутоиммунные и наследственные болезни. И никуда, образно говоря, эти убийцы от нас не спрячутся, – как не спрятались чума и лепра, авитаминозы и анемии: истинные причины будут изобличены, патогенез досконально изучен, лекарства найдены. Поскорее бы только, господа ученые. Поскорее бы. Мы знаем, что делается все мыслимое и немыслимое; знаем, что где-то в лабораториях, клиниках, университетских центрах морщат высокие лбы и трут воспаленные от бессонницы глаза современные Каслы, Аддисоны, Бирмеры, Дженнеры, Мечниковы, Флемминги. И все-таки – поторопитесь, пожалуйста…
Возвращаясь к запутанной проблеме В12-дефицитной анемии: анемия пернициозная – это не синоним, это частный случай. Как уже ясно из сказанного, недостаток кобальтсодержащих витаминов и фолиевой кислоты в организме может быть обусловлен двумя принципиально разными причинами.
Причины
Первая причина – дефицит внешнего фактора Касла, каковой фактор должен регулярно поступать с пищей. В сравнении с другими незаменимыми нутриентами, фолатов и витаминов В12 нужно не так много, но все-таки они жизненно необходимы. Соответственно, их дефицит может быть обусловлен недостаточным и несбалансированным питанием (в том числе вегетарианством, отказом от пищи ради «модельной фигуры», нервно-психической анорексией и т.п.).
Вторая группа причин значительно обширней: она охватывает множество заболеваний и состояний, снижающих концентрацию внутреннего фактора Касла, – желудочного мукопротеида, без которого даже при достаточном поступлении витаминов В9 и В12 невозможно их усвоение. К таким состояниям относится ряд желудочно-кишечных заболеваний, особенно тех, что поражают тонкий кишечник (в т.ч. инфекционные энтериты, болезнь Крона и мн.др.); постоперационные синдромы, связанные с частичной резекций желудка и/или кишечника; патология печени (в печени содержится депо данной группы витаминов, которого хватает на несколько лет). Недостаток транскобаламина (белка, осуществляющего транспорт витаминов В12) в редких случаях может быть наследственным. К нарушениям метаболизма внешнего фактора Касла приводит также избыточный и слишком продолжительный прием антибиотиков, антацидов, пероральных контрацептивов; гельминтозы; гиперактивность некоторых бактериальных культур; аутоиммунные расстройства; онкопроцессы; химические ожоги слизистой желудка; алкоголизм.
Потребность в фолатах и В12 возрастает при беременности.
Распространенность данной разновидности анемии в общей популяции оценивается на уровне 1%, с преобладанием женщин. В выборках пожилого и старческого возраста доля лиц с В12-дефицитной анемией возрастает до 10% и более, – за счет инволюционных изменений в тканях, секреторных процессах и общем метаболизме.
Симптоматика
Помимо общеанемической симптоматики, обусловленной хроническим кислородным голоданием тканей (астенический синдром, признаки дыхательной недостаточности, кардиальные нарушения), типичными симптомами пернициозной анемии выступают поражение желудочно-кишечного тракта, центральной и периферической нервной системы. Характерен «лакированный» малиновый язык (глоссит, воспаление), ахилия (пищеварительная несостоятельность желудочного сока), атрофия слизистых ЖКТ, мышечная слабость, нарушения координации, походки, чувствительности. В некоторых случаях развиваются энкопрез и энурез. При длительной анемии дегенеративно-дистрофические процессы поражают миокард, обнаруживается демиелинизация нейронных оболочек. Выраженные нарушения наблюдаются со стороны ЦНС – от депрессивной подавленности до галлюцинаторно-бредовых психозов и деменции. Повышается онкологический риск на фоне атрофических и воспалительных процессов.
Диагностика
Быстрое и доказательное установление точного диагноза требует от врача высокой квалификации, большого опыта, а также постоянной настороженности в отношении гиповитаминозов. Подозрение на анемию, вызванную дефицитом внутреннего фактора Касла (пернициозная форма) или алиментарным, пищевым фактором, вызывается сочетанием неспецифических и характерных симптомов на фоне сниженного гемоглобина в общеклиническом анализе крови. При наличии такого подозрения назначается батарея лабораторных анализов, производится инструментальное обследование органов ЖКТ (рентгенография, ФГДС, ирригография, УЗИ и др.); по мере необходимости к лечебно-диагностическому процессу привлекаются кардиолог, невролог и другие специалисты.
Лечение
Терапевтическая стратегия определяется установленной этиологией анемии. Обязательными являются нормализация рациона, специальная диета, интенсивное лечение основного заболевания (если оно есть). Заместительная терапия цианкобаламином должна тщательно рассчитываться с учетом всех индивидуальных особенностей случая. Иногда имеются показания к назначению гормональных средств. При развитии жизнеугрожающего состояния прибегают к гемотрансфузиям. Паллиативные меры принимаются в зависимости от конкретного симптомокомплекса. Категорически исключен алкоголь – безжалостный антагонист витаминов группы В.
При поздней диагностике, длительном течении и запоздалом начале терапии изменения со стороны нервной системы могут оказаться глубокими и необратимыми.
Некоторые больные получают поддерживающее лечение пожизненно. Необходим также регулярный онкоконтроль.
Мегалобластная анемия что это такое симптомы у женщин причины возникновения и лечение
Тиамин-зависимая мегалобластная анемия (TRMA) была впервые описана в 1969 г. Роджерсом и соавт. [1, 2]. Они выдвинули гипотезу, что причиной анемии является нарушение метаболизма витамина B1, что было эмпирически подтверждено коррекцией последней после перорального приема тиамина. Дисфункция высокоаффинного переносчика тиамина (THTR-1), ответственного за трансмембранный транспорт витамина B1, вызывает анемию, а также экстрамедуллярное повреждение (бета-клетки и клетки внутреннего уха) [3]. Редкость данного заболевания и неосведомленность медицинского персонала часто являются причиной задержки начала диагностики и лечения. Как правило, источником информации о данной патологии в научной печати являются отдельные сообщения о клинических случаях.
Патология встречается редко, в литературе описано менее ста отдельных клинических случаев [1]. Распространенность и заболеваемость доподлинно неизвестны. Большинство случаев происходит из изолированных сообществ или других общин, где распространены близкородственные связи (что объясняется аутосомно-рецессивным характером наследования). Как правило, это страны Ближнего, Среднего Востока или Центральной Азии: Иран, Турция, Индия, Пакистан. Опубликованы случаи диагностики в Китае и Японии [1, 4]. В Европе описано несколько случаев у представителей европеоидов без анамнеза близкородственных связей [1, 5].
Витамин B1 – водорастворимый витамин, который в высоких концентрациях содержится во всех тканях, особенно в скелетных мышцах, сердце, печени, почках и головном мозге. Его основная активная форма – пирофосфат тиамина. Он участвует в нескольких основных энергетических метаболических процессах: превращении пирувата в ацетил-коэнзим А в цикле Кребса (как кофактор пируватдегидрогеназы и альфа-кетоглутаратдегидрогеназы), пентозофосфатном пути (как кофакторе транскелотазы) [1, 6], и в катаболизме разветвленных аминокислот, таких как лейцин, изолейцин и валин [1, 7, 8]. Витамин B1 также играет пока не совсем ясную роль в нервной проводимости, независимо от его роли в качестве кофактора [6].
1) при физиологических концентрациях в плазме (
Анемия: причины развития, симптоматика и терапия
Анемия — это заболевание, связанное с уменьшением количества красных кровяных телец (эритроцитов). Многим анемия известна по другому названию — малокровие. Заболевание довольно опасное, так как с уменьшением эритроцитов снижается и уровень гемоглобина — железосодержащего белка, выполняющего важнейшую функцию газообмена, перенося к тканям и органам кислород и забирая углекислый газ. Одновременно с понижением гемоглобина в крови падает другой показатель — гематокрит. Это процентное отношение красных кровяных телец к плазме крови.
В 90% обнаруживают железодефицитную разновидность малокровия.
По степени тяжести анемия бывает легкой, когда уровень гемоглобина составляет 100-119, средней с показателем 70-100, тяжелой, при которой уровень гемоглобина менее 80 г/л.
Показатели нормы эритроцитов, указывающих на развитие анемии, отличаются у мужчин, женщин и детей. Для мужчин уровень гемоглобина должен составлять более 130 г/л, гематокрит при этом более 42%. У женщин показатель гемоглобина должен быть выше 120 г/л, а гематокрит выше 37%. Отклонение от этих значений меньшую сторону свидетельствует о развивающемся или развившемся малокровии. У детей показатели регулярно меняются в зависимости от возраста, поэтому для постановки диагноза используют возрастные таблицы.
Анемию провоцируют разные причины. Это наследственный фактор, патологические процессы, недостаток витаминов и микроэлементов в организме. Для назначения правильной терапии важно выяснить, почему развилось малокровие.
Существует ряд патологий, из-за которых у близких родственников в нескольких поколения наблюдается анемия, которую называют генетической.
Помимо этого анемия бывает клиническим симптомом онкологических заболеваний, патологий, связанных с обильной или постоянной потерей крови (геморрой, язва, эрозивные заболевания органов пищеварительной системы).
Иногда малокровие связано с недостатком витаминов группы В, железа. Провоцирует ее развитие и проблема с их усвояемостью (например, нарушение всасывания в кишечнике).
Малокровие развивается при недостатке питания, нарушении транспортной функции гемоглобина к органам и тканям. У женщин развитие анемии провоцируют обильные менструации, а во время беременности возросшая потребность в железе. У детей частыми причинами являются недостаток потребления железа и витаминов с продуктами питания.
Нередко анемия развивается у вегетарианцев и веганов. Железа в растениях содержится намного меньше, чем в мясе и субпродуктах, и усваивается оно хуже. В растительной пище содержится фитиновая кислота, которая в совокупности с железом образует нерастворимые комплексы, ухудшающие его всасывание. В мясных продуктах имеется белок миоглобин, способствующий улучшению всасываемости железа в кишечнике, поэтому из мяса железо усваивается намного лучше.
Но основной причиной анемии врачи считают нарушение кроветворения в основных «фабриках производства кровяных телец» — костный мозг и селезенка, некоторые хронические, инфекционные заболевания, острые и хронические потери крови.
Условно в 1 мл крови содержится примерно 0,5 мг железа. При острых или хронических кровотечениях анемия появляется из-за резкого уменьшения массы эритроцитов. Зависит она от количества потерянной крови и от механизма компенсации активирования кроветворения. Хронические кровотечения истощают запасы железа в организме, что провоцирует развитие анемии. Даже кровоточащий геморрой ежедневно уносит 5 мг железа (если кровопотеря составляет пару чайных ложек или 10 мл). Это превышает суточное поступление железа.
Характерные признаки малокровия
Анемия сопровождается определенной симптоматикой. В целом она не имеет четко выраженных границ, особенно в начальной стадии. Признаки появляются только при падении гемоглобина до нижних границ. Более выражены признаки при стремительном развитии малокровия, связанным с заболеваниями инфекционной, воспалительной природы, эрозивными и язвенными болезнями. Человека беспокоит слабость, частые головокружения, обмороки, тахикардия, повышенная утомляемость, сонливость, сухость кожных покровов, шум в ушах, понижение концентрации внимания и памяти. У детей страдает нервная система. Они становятся вялыми, раздражительными, беспокойными, плохо спят поверхностным сном, отстают в развитии от сверстников. У женщин наблюдаются скудные выделения при менструации или полное их прекращение.
В некоторых случаях конкретные симптомы указывают на причины возникновения анемии:
Анемия оказывает негативное влияние на повседневную жизнь человека. Он испытывает постоянный упадок сил, сонливость, невозможность сконцентрироваться. В результате сложно учиться, работать, заниматься спортом. Страдает и иммунитет, человек становится уязвимым перед инфекционными заболеваниями. Влияет малокровие на дыхательную и сердечно-сосудистую систему. Из-за недостаточного количества кислорода и снабжения им тканей возникает тахикардия, одышка, может развиться сердечная недостаточность. Анемия у беременных ведет к нарушению внутриутробного развития плода. У матерей с таким диагнозом дети часто рождаются недоношенными, с низкой массой тела, пониженным уровнем железа.
При наличии подозрительных признаков следует проконсультироваться с терапевтом. Он назначит общий анализ крови и биохимию.
На малокровие в общем анализе крови указывают:
Могут наблюдаться изменение формы и размеров красных и белых кровяных телец.
В биохимическом анализе крови при малокровии отмечается:
Для подтверждения некоторых форм анемии достаточно лишь ОАК и биохимии. После получения результатов анализов потребуется консультация гематолога или других специалистов-медиков. Они проводят ряд лабораторных и инструментальных исследований для дифференцирования разновидностей заболевания.
Лечение малокровия подразумевает выяснение причины его появления. Основой терапии железодефицитной анемии (самой распространенной из всех видов малокровия) считается восполнение запасов гемоглобина в организме, нормализация гематокрита и количества здоровых красных кровяных телец. Чаще всего назначают препараты двухвалентного железа. Самостоятельно принимать их без консультации с врачом ни в коем случае нельзя, это чревато негативными последствиями. Дополнительно изменяют диету в пользу увеличения продуктов с высоким содержанием железа (красное мясо, субпродукты, горький шоколад).
При других видах анемии требуется восполнить запасы фолиевой кислоты, витамина В12, выявить и лечить хронические заболевания, являющиеся первопричинами малокровия.
Для терапии апластической анемии часто требуется переливание эритроцитарной и тромбоцитарной массы, трансплантация костного мозга, иммуномодулирующие средства, антибиотики, глюкокортикоиды.
Гемолитические анемии устраняют гормонами, цитостатиками, переливанием плазмы крови, плазмоферезом, удалением селезенки, пересадкой костного мозга.
Прогноз при пониженном уровне гемоглобина зависит от вида анемии. Лучше всего поддается лечению малокровие, вызванное недостатком минералов или витаминов. При соблюдении всех правил терапии, которую прописал специалист, уровень гемоглобина удается восстановить достаточно быстро. Немного сложней ведется лечение анемии, вызванной хроническими заболеваниями. И не очень благоприятный прогноз относится к малокровию, вызванному различными видами опухолей, генетических нарушений. Они плохо поддаются терапии.