Микрогастрия у плода что
Микрогастрия у плода что
Желудок, который выглядит значительно меньше ожидаемого размера, также может быть признаком скрытой аномалии. Обнаружение маленького желудка при динамическом наблюдении свидетельствуете необходимости детального морфологического исследования структур плода. Было обнаружено, что 27 из 52 (52%) плодов с маленькими желудками имели неблагорпиятный перинатальный исход.
Тем не менее, если этот признак отмечается изолированно и носит транзиторныи характер с дальнейшей нормализацией размеров желудка при последующих обследованиях, исход, наиболее вероятно, будет благоприятным, как это было отмечено у всех 12 таких плодов в вышеупомянутом исследовании.
Обнаружение уменьшения размеров или отсутствия желудка, наболее вероятно, свидетельствует о возможности неблагоприятного исхода при наблюдении после 24 нед беременности, чем в более ранние сроки.
Помимо того, что отсутствие эхотени желудка или его маленькие размеры могут являться как потенциальными признаками атрезии пищевода, так и нормальным вариантом развития, эти признаки также обнаруживаются при целом ряде других патологических состояний. Было установлено, что отсутствие жидкости в желудке связано с нехваткой плоду амниотической жидкости для глотания.
По данным публикаций о невизуализации желудка маловодие часто регистрируется при различных патологических состояниях плода, включая аномалии мочеполовой системы, хромосомные нарушения и задержку внутриутробного развития плода (ЗВРП). Это также может быть связано с расстройствами нормального механизма глотания, как это, возможно, происходит у плодов с пороками ЦНС, расщелиной губы и нейромышечными заболеваниями.
И наконец, желудок может содержать жидкость, но не обнаруживаться, если он смещен с ожидаемого места расположения в верхнем левом квадранте, как это бывает у плодов с диафрагмальной грыжей.
Иногда при эхографическом обследовании в пренатальном периоде в желудке плода могут определяться гиперэхогенные включения, которые были названы «псевдосодержимое» желудка, поскольку обычно они представляют собой транзиторно визуализируемые конгломераты проглоченных скоплений клеток или их фрагментов. «Псевдосодержимое» желудка плода следует дифференцировать с такими с патологическими образованиями, как опухоль желудка. Его обнаружение обычно не сочетается с наличием какой-либо другой патологии.
Хотя иногда «псевдосодержимое» может возникать вследствие заглатывания крови, излившейся в околоплодные воды после амниоцентеза или при отслойке плаценты. В этой связи при его обнаружении необходимо провести тщательный осмотр области прикрепления плаценты для исключения признаков ее отслойки. Кроме того, необходимо также обратить внимание на расширение петель тонкого кишечника в брюшной полости плода, поскольку вероятность наличия «псевдосодержимого» желудка увеличивается при замедлении перистальтики кишечника на фоне его обструкции.
При отсутствии клинических или эхографических признаков отслойки плаценты или пороков развития плода изолированное выявление «псевдосодержимого» желудка может быть интерпретировано как вариант нормального состояния, которое не требует дальнейшего специального наблюдения.
Прочие нарушения состояния желудка, которые могут определяться пренатально, включают в себя варианты обструкции его пилорического отдела, такие как мембрана, стеноз или атрезия привратника, а также грыжи пищеводного отверстия. Гипертрофический стеноз привратника обычно формируется через несколько недель после рождения, но очень редко может обусловливать расширение желудка во внутриутробном периоде.
Обнаружение у плода аномального расширения желудка может представлять определенную трудность, поскольку его нормальные размеры могут значительно варьировать. Дополнительными признаками в этих случаях могут служить многоводие, утолщение стенок желудка, воронкообразная суженная форма преддверия желудка и исчезновение изгиба его малой кривизны. Потенциально сложной Для антенатальной диагностики также является грыжа пищеводного отверстия, поскольку она может иметь сходство с диафрагмальной грыжей, при которой только часть желудка выходит в грудную полость.
Таким образом, и та и другая грыжи могут приводить к возникновению в грудной полости кистозной структуры, у которой будет прослеживаться связь с желудком. Специфический диагноз грыжи пищеводного отверстия должен рассматриваться только в тех случаях, когда небольшой участок желудка выходит в грудную полость, а дополнительные признаки, характерные для диафрагмальной грыжи, отсутствуют, а именно: смещение органов средостения, уменьшение окружности брюшной полости, многоводие, плевральный или перикардиальный выпот и другие структурные аномалии.
Важность дифференцирования этих двух пороков состоит в том, что грыжа пищеводного отверстия имеет лучший прогноз, чем грыжа диафрагмы. Она обычно не сочетается с другими структурными или хромосомными аномалиями и не рассматривается как потенциальное показание к проведению внутриутробных хирургических вмешательств.
Аномалии и патологии органов пищеварительной системы плода, выявляемые на УЗИ
» data-image-caption=»» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2018/05/patologii-zhkt-ploda.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2018/05/patologii-zhkt-ploda.jpg?fit=805%2C536&ssl=1″ />
Патологии органов пищеварительной системы встречаются у плода нередко как самостоятельно, так и в комплексе с другими аномалиями внутренних органов. На них приходится до 21% пороков у новорождённых и 34% случаев младенческой смертности.
патологии жкт плода
» data-image-caption=»» data-medium-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2018/05/patologii-zhkt-ploda.jpg?fit=450%2C300&ssl=1″ data-large-file=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2018/05/patologii-zhkt-ploda.jpg?fit=805%2C536&ssl=1″ loading=»lazy» src=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2018/05/patologii-zhkt-ploda.jpg?resize=805%2C536″ alt=»патологии жкт плода» width=»805″ height=»536″ srcset=»https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2018/05/patologii-zhkt-ploda.jpg?w=805&ssl=1 805w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2018/05/patologii-zhkt-ploda.jpg?resize=450%2C300&ssl=1 450w, https://i0.wp.com/medcentr-diana-spb.ru/wp-content/uploads/2018/05/patologii-zhkt-ploda.jpg?resize=768%2C511&ssl=1 768w» sizes=»(max-width: 805px) 100vw, 805px» data-recalc-dims=»1″ />
Причины нарушений формирования органов ЖКТ у плода, статистика
Аномалии строения органов ЖКТ связаны с нарушением эмбриогенеза на стадии 4-8 недель беременности, когда идёт образование отверстия пищеварительной трубки. Изначально она заканчивается с обоих концов, однако к концу 8 недели происходит образование каналов, а слизистый эпителий закрывает просвет кишечной трубки.
Среди наиболее часто встречающихся патологий можно выделить стенозы (сужения или растяжки стенок) или атрезии (сращивания).
Больше всего страдает 12-перстная кишка, что связано с особенностями её эмбриогенеза. 1/2 случаев сопровождается пороками других внутренних органов — сердца, сосудов, прямой кишки, печени, желудка. Некоторые случаи настолько тяжёлые, что малышу при жизни придётся сделать множество операций, и они не будут являться гарантом его нормального существования.
Аномалии органов ЖКТ на УЗИ видны на сроке 11 недель. Ультразвуковая диагностика не является 100% гарантией того, что у малыша будут серьёзные отклонения, поэтому её результаты являются основанием для более детального обследования женщины.
Беременной делают кариотипирование на выявление хромосомных нарушений. Также она проходит анализ амниотической жидкости, и по результатам обследования (если они плохие и диагноз подтвердится) ей рекомендуют прервать беременность
Патологии кишечника
К аномалиям 12-перстной кишки относятся:
Атрезия. Встречается в 1 случае из 10 000. Заключается в полной непроходимости кишечника вследствие патологического сращения стенок органа. В 37% случаев сопровождается другими аномалиями — конской стопой, слиянием шейных позвонков, несимметричным положением рёбер и пр.
Ещё в 2% случаев атрезия кишечника сопровождается атрезией пищевода, гигромой заднего прохода, незавершённом поворотом желудка и т.п. В основном это типично для плода с хромосомными нарушениями, в частности с трисомией по 21 хромосоме.
90% беременностей заканчиваются выкидышем или замиранием развития в течение первых 2-х триместров. Остальные 10% беременностей с патологией 12-перстной кишки завершаются рождением детей, страдающих различными пороками: у 31% имеется обструкция дыхательных путей (закупорка инородным телом вроде кисты, опухоли), 24% — парез лицевого нерва (нарушением функциональности мимических мышц).
Только 1% малышей ведёт относительно нормальный образ жизни после проведения сложнейшей операции при условии отсутствия хромосомных нарушений.
Патология не является показанием для прерывания беременности. В зависимости от расположения мембраны она удаляется после рождения малыша методом дуоденотомии (вскрытием просвета кишечника с последующим удалением мембраны).
Мальротация. Заключается в нарушении нормального вращения и фиксации 12-перстной кишки. Если средняя кишка совершила полный оборот на кровоснобжающей ножке, это может привести к прекращению кровоснабжения и отмиранию средней кишки.
Пренатальный диагноз можно поставить с 24 недели, причём в 61,5% беременностей наблюдалось многоводие. На УЗИ выявляется анэхогенный double-buble 3 следствие расширение кишки и желудка.
Хотя даже незначительное расширение на сроке 16-22 недели должно вызывать тревогу. В норме 12-перстная кишка видна на УЗИ только с 24 недели. Дополнительно в 62% случаев выявляются у плода пороки развития сердца, мочеполовой системы, других органов ЖКТ. После исследования на кариотип в 67% случаев выявляются хромосомные отклонения, из которых на 1 месте стоит синдром Дауна.
Стеноз. Выявляется у 30% новорождённых, в основном у мальчиков. Это частичная непроходимость 12-перстного кишечника, локализованная в одном месте. В основном наблюдается в верхних отделах и сопровождается аномалиями поджелудочной железы. На УЗИ отчётливо виден на сроке от 24 недель при использовании допплеровского метода в изучении кровотока кишечника.
Патология выявляется не ранее чем на 16 неделе. Она свидетельствует об отклонении в развитии плода. Повышенная эхогенность случается при преждевременном старении плаценты, внутренних инфекциях, несоответствии размеров плода сроку беременности, эндокринном заболевании муковисцидозе, кишечной непроходимости (стенозе).
УЗИ следует пройти в нескольких разных клиниках во избежание ошибки специалиста. Только при окончательном подтверждении диагноза женщину отправляют на более детальное обследование — биохимический скрининг, анализ на ТОРЧ-инфекции, кордоцентез и анализ амниотической жидкости. Окончательный диагноз ставится на основе комплексного анализа, а не только УЗИ обследования.
Дивертикулы (кисты). Они имеют разные названия — дупликационные кисты, удвоенная кишка, энтерогенная дивертикула. Заключается в отпочковании от стенок кишки образования в эмбриональный период. Образуются не только в кишечнике, но и по всему ЖКТ от гортани до ануса.
Считается, что причиной раздвоения стенок служит нарушение кровоснабжения пищеварительной трубки плода. Кисты на УЗИ гипоэхогенны, бывают как однокамерными, так и многокамерными. Стенки кист двухслойны и имеют повышенную перистальтику, имеют гиперэхогенность, если содержат кровь.
Визуализируются кисты кишечника на 2 триместре и часто сочетаются с другими патологиями. Точность визуализации кист кишечника у плода составляет 66,6%. Данная патология не является показанием к прерыванию беременности, потому что в неосложнённых случаях оперируется и устраняется.
Аномалия формы, размера, положения и подвижности кишечника. Ко 2 триместру беременности должен обратиться вокруг брыжеечной артерии против часовой стрелки на 2700. При нарушении эмбриогенеза можно выделить следующие патологии: отсутствие поворота, несостоявшийся поворот и неполный поворот.
На УЗИ при аномалиях поворота кишечника у плода отмечается многоводие и расширение петель кишечника без перистальтики. В случае перфорации кишечника возникает микониевый перитонит — заражение вследствие выхода наружу содержимого кишечника. Обнаруживается патология поздно, только на 3 триместре, что требует немедленной подготовки женщины к родоразрешению.
Патологии печени у плода
Печень визуализируется на ультразвуковом обследовании уже на 1-м скрининге. На сроке 11-14 недель можно увидеть в верхней части брюшной полости гипоэхогенное образование в виде месяца. К 25 неделе эхогенность повышается и становится такой же, как у кишечника, а перед родами превышает по плотности кишечник.
Очень важна оценка состояния кровотока печени. Вена пуповины плода входит в печень, во 2 триместре визуализируется воротная вена. Её диаметр в норме равен 2-3 мм, а к родам увеличивается до 10-11 мм. Желчные протоки в норме визуализироваться у плода не должны.
Одна из часто встречающихся патологий плода — гепатомегалия печени — увеличение размеров органа. Для выявления аномалии применяется 3D датчик, способный визуализировать срез в продольном, поперечном и вертикальном срезах. Также можно увидеть увеличение размеров печени и на обычном УЗИ аппарате по выступающему животику, охват которого значительно превышает норму.
Одновременно с этим на экране видны различные гиперэхогенные включения. Как правило, аномалия дополняется увеличением селезёнки.
Среди причин, приводящих к увеличению размеров органов пищеварения, выделяют скрытые инфекции (токсоплазмоз, сифилис, ветрянка), а также хромосомные мутации (синдромы Дауна, Зельвегера, Беквета-Видемана).
В 87,5% случаев причиной увеличения печени и образования кальцификатов являются внутриутробные инфекции. Также у большинства беременных диагностируется гиперэхогенный кишечник, изменение структуры плаценты, а также большие размеры селезёнки. Патология на 3 триместре возникает в случае резус-конфликта между матерью и ребёнком.
Также не исключены и метаболические нарушения. Увеличение печени встречается при галактоземии (генетическое нарушением углеводного обмена, из-за которого галактоза не преобразуется в глюкозу), трипсинемии (отсутствия выработки пищеварительного гормона трипсина), метилмалоновой ацидемии (отсутствии превращения D-метилмалоновой кислоты в янтарную кислоту), нарушениях выделения мочевины.
Одиночные гиперэхогенные включения большого размера гораздо лучше, чем множественные разрозненные образования в сочетании с другими патологиями. Практически в 100% случаев гиперэхогенные включения большого размера устраняются до рождения малыша или в первый год жизни.
В некоторых случаях порок органов брюшной полости ставится ошибочно. Такое бывает, если брюшная полость малыша сдавливается стенками матки, патологиях миометрия или других факторах.
На экране монитора видна псевдоомфалоцеле — ошибочная визуализация выхода органов брюшной полости за пределы брюшной стенки. Иногда УЗИ «не видит» значительных пороков. Так, грыжа по форме и эхоструктуре напоминает петли кишечника, в этом плане большую помощь оказывает допплерометрия, позволяющая увидеть кровоток.
Наша клиника имеет прекрасный 4D аппарат, оснащённый всеми современными возможностями, исключающими ошибки диагностики.
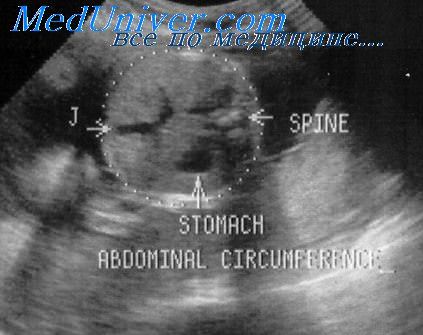
Желудок
На 16-20 неделе визуализируется желудок плода как анэхогенное образование круглой или овальной формы в верхних отделах брюшной полости. Если желудок не наполнен амниотическими водами, то можно говорить об атрезии пищевода (полном отсутствии просвета).
При диафрагмальной грыже желудок смещён и также не может быть определён на УЗИ. Также амниотическая жидкость отсутствует при поражении ЦНС у плода.
Если плод заглатывает вместе с жидкостью кровь, в желудке визуализируются гиперэхогенные включения. Они также видны при опухолях желудка, но они обычно сопровождаются другими пороками развития. Размеры органа увеличиваются при кишечной непроходимости, многоводии, утолщении стенок, отсутствии малой кривизны.
Уменьшение размеров желудка типично для микрогастрии, которая возникает на фоне отсутствия мочевого пузыря или неправильного положения печени. В 52% случаев плод погибает до 24-й недели беременности, ребёнок рождается нежизнеспособным.
Щелевидный желудок характерен для недоразвитии на ранних стадиях беременности. Данная патология исправляется после рождения малыша: ребёнку конструируют желудок из части тонкого кишечника. Операция крайне сложная, но аномалия не является показанием для выполнения аборта.
Атрезия желудка характеризуется отсутствием эхотени и предполагает образование плёнки с отверстием или без него, расположенной поперёк стенок желудка. Если это изолированная патология, то в 90% случаев она устраняется хирургически. Но обычно атрезия желудка сочетается со сращиванием пищевода, асцитом (излишним скоплением жидкости), недоразвитостью лёгких.
Агенезия желудка предполагает полное отсутствие органа. Это типично для тяжёлых хромосомных аномалий, от которых плод погибает в пренатальный период. Большое значение в диагностике имеет УЗИ на 22 неделе. некоторые отклонения исчезают сами собой, а некоторые требуют немедленного вмешательства.
Микрогастрия у плода что
Врожденные пороки развития (ВПР) – это структурные или функциональные отклонения от нормы, которые проявляются в период внутриутробного развития и могут быть выявлены до рождения, во время рождения или на более поздних этапах жизни [1].
По оценке Всемирной организации здравоохранения (ВОЗ) ВПР являются наиболее часто встречаемой патологии у детей периода новорожденности и младенчества и остаются основной причиной заболеваемости, инвалидности и смертности в данной возрастной группе [1]. В мире рождается более 5,5 % детей с ВПР, летальность, при этом, составляет около 30–40 % [2]. При этом среди причин неонатальной смертности ВПР составляет 7 % [3]. В Республике Казахстан за последние годы ВПР занимает лидирующее место среди причин младенческой смертности, составляя 22,6–22,8 % и не имеет тенденции к снижению, а в Карагандинской области 35,4–30,8 %, занимает второе место после перинатальных причин [2, 4, 5].
При этом в общей структуре врожденных пороков доля патологии желудочно-кишечного тракта (ЖКТ) составляет от 21,7 % до 25 % от всех пороков и занимает третье место. В странах Европы ВПР ЖКТ встречаются с частотой 13–26,4 на 1000 живорожденных, число летальных исходов среди новорожденных детей с диагнозом ВПР ЖКТ входит в размах от 25 % до 57 % [6].
Цель работы: обзор литературных данных о частоте, структуре, причинах, диагностике и выживаемости наиболее часто встречаемой врожденной патологии ЖКТ – атрезии ЖКТ.
Причины возникновения ВПР ЖКТ полностью не исследованы. В зависимости от этиологиологических факторов, повлекших за собой развитие порока, условно выделяют наследственные, экзогенные и мультифакториальные ВПР: хромосомные нарушения 5 %, мутации отдельных генов 2–3 %, факторы внешней среды 1–2 %, полигенно-мультифакториальные 90 %. Но более чем в 70 % случаев ВПР причины их развития остаются неизвестными [7, 8]. Однако имеются исследования, доказывающие, что в развитии врожденных пороков развития новорожденного большую роль играет антенатальный период и возникающие в данном периоде различные факторы. К ним можно отнести различные осложнения беременности, острые заболевания матери, возникшие в течение беременности, а также применение в лечении антибактериальной и гормональной терапии во время беременности. Детальный анализ различных научных исследований за последнее двадцатилетие, преимущественно в Соединенных Штатах Америки, отразил значительную частоту появления на свет детей с аноректальными пороками от родителей, зависящих от никотина и употребляющих алкоголь, матерей страдающих ожирением и сахарным диабетом (в том числе гестационным) [9]. В числе наиболее значимых внешних факторов, оказывающих большое влияние на возникновение ВПР, выделяют возрастной аспект, а именно: возраст родителей старше 35 лет; большой перерыв между первой и повторной беременностями у матерей старшего возраста; рождение первого ребенка у пожилых родителей. Важное место в формировании ВПР имеют условия и характер труда родителей, а именно наличие профессиональных вредностей. Особое значение этот факт имеет в случаях, когда негативные условия труда имеются у обоих родителей [10].
Патогенез ВПР ЖКТ связан с нарушением образования отверстий пищеварительной трубки в периоде от 4-й до 8-й недели внутриутробного развития, так как вначале эта трубка заканчивается слепо с обоих концов. Имеет значение и задержка реканализации, так как на 8-й неделе внутриутробной жизни растущий эпителий полностью закрывает просвет кишечной трубки, который в дальнейшем восстанавливается при формировании слизистой оболочки [11].
В классификации врожденных пороков пищеварительной системы можно выделить пороки развития брюшной стенки и врожденные пороки непосредственно органов ЖКТ. Однако наиболее встречаемой патологией в структуре врожденных пороков ЖКТ являются атрезии того или иного участка пищеварительной системы.
В частности, атрезия пищевода (АП) составляет примерно 30 % всех случаев атрезий пищеварительного тракта [12]. Врожденные аномалии пищевода встречаются 1 раз на 3000–5000 рождений [13, 14]. По результатам различных научных и клинических исследований АП встречается в среднем с частотой 2,0–4,0 на 10 000 рождений, или 1 случай на 2500–4500 рождений [15, 16]. При этом зачастую в 50–70 % случаев АП входит в структуры множественных пороков развития (МВПР) [17], и лишь в единичных случаях встречается изолированно. Клинические варианты врожденных пороков развития пищевода согласно классификации Кларк 1999 [18]:
1. АП с дистальным трахеопищеводным свищом, составляет около 86 % всех случаев порока.
2. Изолированная АП без свища, встречается в 7 % всех случаев.
3. Трахеопищеводный свищ без атрезии, или Н-тип, составляет 4 %.
4. АП с проксимальным трахеопищеводным свищом. Это редкая форма порока, составляющая примерно 2 % всей группы АП.
5. АП с проксимальным и дистальным трахеопищеводными свищами, не превышает 1 %.
В международной классификации болезней 10 пересмотра выделяют только лишь следующие формы АП:
1. Врожденная АП без свища.
2. Врожденная АП с трахеопищеводым свищом.
В 5–7 % случаев АП сопровождается хромосомными аномалиями (трисомия 18, 13 и 21) [17]. В 10–30 % случаев АП является одним из клинических проявлений VATER- или VACTERL-ассоциации [12], где своеобразие сочетаний аномалий развития обозначены по начальным латинским буквам следующих пороков [17]:
V – пороки позвоночника;
А – пороки заднего прохода;
С – кардиальные пороки;
T – трахеопищеводный свищ;
E – атрезия пищевода;
R – дефекты лучевой кости;
L – пороки конечностей.
Существующие сведения свидетельствуют о том, что частота встречаемости данного порока пищевода остается сравнительно стабильной в течение долгого времени в разных странах [12]. На международном уровне самая высокая частота этого заболевания зарегистрирована в Финляндии, где АТ встречается в одном случае на 2500 рождений [19]. В мировой статистике соотношение встречаемости порока у мальчиков и девочек составляет 1,26:1,0. Среди всех новорожденных с атрезией пищевода она отмечается у 21 % недоношенных детей и у 19 % маловесных [20], в 30–40 % случаев дети с АП имеют задержку внутриутробного развития [21].
Частота встречаемости атрезии двенадцатиперстной кишки (ДПК) составляет в среднем один случай на 10 000 живорожденных [22]. На выявленных ВПР ЖКТ, 2/3 случаев атрезии ДПК являются составной частью множественных пороков развития, в том числе VACTERL ассоциация [23, 24]. В 79 % случаев имеются сопутствующие пороки: например, трисомия 21, пороки сердца, кольцевидная поджелудочная железа, АП, незавершенный поворот кишечника (мальротация), атрезия других отделов ЖКТ, атрезия ануса [25, 26].
Однако атрезия толстого кишечника встречается реже, в одном случае на 20 000 живорожденных детей [27, 28].
Атрезия ануса и прямой кишки является довольно изученным пороком, а также поддается ранней диагностике. По статистическим данным из различных литературных источников, встречается с частотой от 1:1500 до 1:5000 новорожденных [24, 29]. Практически в 80 % случаев атрезия ануса и прямой кишки сочетается в другими врожденными аномалиями, такими как пороки развития мочеполовой системы, сердца, желудочно-кишечного тракта и позвоночника, особенно его каудального отдела. Атрезия ануса и прямой кишки входит в состав VACTER- и VACTERL-ассоциаций [23, 24, 30], а также может встречаться как системный ВПР, сочетаясь с атрезией пищевода [25].
Диагностика ВПР ЖКТ возможна уже с антенатального периода – с 12–23 недели гестации [17]. Основным диагностическим методом антенатальной диагностики пороков развития является ультразвуковое исследование (УЗИ) [31], которое позволяет с первых недель обнаружить ВПР. В Российской Федерации (РФ) УЗИ с целью перенатальной диагностики пороков развития проводится на трех уровнях: 1 уровень – общее акушерское УЗИ. Цель: определение «нормы» или «отклонения от нормы»; 2 уровень – специализированное перинатальное УЗИ, с целью определения наличия или отсутствия нарушений в развитии плода, при подозрении на таковые при первом УЗИ исследовании; 3 уровень – экспертное перинатальное УЗИ, целью которого является постановка окончательного диагноза и, как следствие, определение дальнейшей тактики ведения беременности и родов [31]. Согласно Национально-клиническому протоколу «Ведение физиологической беременности» в РК обязательной является постановка на учет по беременности в срок до 12 недель и на каждый триместр беременности, согласно скринингу, предусматривается УЗИ плода для выявления антенатальной патологии. При выявлении некорректируемых и, как следствие, несовместимых с жизнью ВПР решается вопрос о прерывании беременности [31]. В мировой практике применяется геномное/генетическое тестирование с использованием фетальных клеток, как один из обязательных методов антенатальной диагностики ВПР [32].
При проведении антенатальной УЗИ-диагностики пороков развития пищеварительного тракта зачастую можно столкнуться с некоторыми трудностями [33], хотя практически каждый из пороков имеет специфические перинатальные эхографические признаки, многие из них остаются только косвенными. Например, диагностическая ценность УЗИ АП составляет 25–56 %. Ультразвуковая диагностика АП базируется на основании многоводия, связанного со снижением оборота околоплодных вод по пищеварительной система плода, вследствие непроходимости пищевода; отсутствия эхографического изображения желудка или его маленьких размеров [19] при проведении динамического УЗИ наблюдении начиная с 14–16 недели гестации [30]. Неонатальная диагностика АП проста и может быть проведена еще до начала развития клинической картины: при попытке введения назогастрального зонда на расстоянии 10–12 см возникает сопротивление для дальнейшего прохождения зонда [26], данный метод не является рутинным и применяется только при наличии подозрения на АП. Более модифицированным методом диагностики АП считается проба Элефанта, когда при быстром введении через зонд воздуха, он с характерным шумом выходит обратно через нос и рот [8, 32]. Также подтвердить диагноз можно выставить по яркой клинической картине – это наличие пенистых слизистых выделений изо рта и носа новорожденного, появляющиеся с первых часов. Эпизоды ухудшения состояния ребенка при наличии АП будут чётко связаны с кормлением, в связи с тем, что молоко вытекает через нос и рот. При отсутствии правильной тактики в ведении ребенка с АП, данное состояние неизбежно приведет к развитию аспирационной пневмонии [8, 32] и как следствие, целому ряду дальнейших осложнений.
Основным антенатальным эхографическим маркером атрезии ДПК является акустический феномен «double – bubble» (двойной пузырь), соответствующий увеличению желудка в сочетании с расширением постпилорического и престенотического участков ДПК [24, 34]. Частым сопровождением пороков развития ДПК является многоводие, и чаще он встречается при поражениях проксимальных отделов кишки. Пропустить или не увидеть эти признаки просто, так как второе УЗИ делается в сроке 18–20 недель, а пренатальный диагноз чаще ставится в срок 24 недель. Но на последнем УЗИ, в 32–34 недели, данная патология визуализируется четко и ясно, и это помогает в дальнейшей тактике ведения родов (определение уровня родильных и перинатальных центров). Наиболее ранним и постоянным клиническим проявлением атрезии ДПК является рвота [26, 35]. Рвотные массы могут содержать желчь, а также могут быть без нее в зависимости от уровня непроходимости ДПК. Если непроходимость локализуется выше фатерового соска, то рвотные массы будут без примеси желчи, при этом будет отходить меконий, так как он образуется из продуктов переработки желчи, которая выделяется в данном случае в «отводящую» кишку. Если же проходимость ДПК затруднена ниже фатерового соска, то в рвотных массах можно увидеть примеси желчи, а из прямой кишки будет отходить только лишь прозрачная слизь [36]. Характерна прогрессивная потеря массы тела, со вторых суток становятся четко выраженными признаки обезвоживания. Живот вздут, увеличен в проксимальных отделах [30, 35], за счет растянутого желудка и ДПК. После обильной рвоты вздутие в надчревной области уменьшается [35]. У всех детей с атрезией ДПК рано появляется и быстро прогрессирует иктеричность кожных покровов, причина данного состояния заключается в снижении экскреции билирубина со стулом [34].
Ультразвуковая диагностика нарушений проходимости тонкого кишечника становится возможной после 25–28 недель беременности. Основной диагностический признак данной патологии – это наличие множественных кистозных образований, расположенных в верхних и средних отделах брюшной полости приблизительно одинакового диаметра. Петли кишечника, расположенные ниже, выглядят незаполненными и четко не дифференцируются [36]. Многоводие, по данным различных авторов, встречается в 30–70 % случаев [22]. Клинически атрезия тонкого отдела кишечника проявляется задержкой мекония, кишечной непроходимостью с рвотой желчью и вздутием живота [14, 25].
Ультразвуковые признаки обструкции толстой кишки проявляются преимущественно после 30 недель беременности. Последнее связано с достаточно хорошей абсорбцией жидкости слизистой оболочкой кишечника. При ультразвуковом исследовании выявляются расширенные петли толстого кишечника до 2,0–3,0 см с наличием в их просвете мелкодисперсной взвеси и отсутствие гаустр [23], усилена перистальтика [37]. Многоводие не наблюдается [23]. При атрезии нижних отделов кишечника преобладают симптомы низкой кишечной непроходимости. Ребенок рождается с вздутым животом, из желудка выделяется застойное содержимое, вместо мекония из прямой кишки отходит светлая слизь [34]. При проведении очистительной клизмы получают только слепки неокрашенной слизи [37]. В связи с перерастяжением петель кишечника отмечается беспокойство ребенка, болевой синдром, усиливающийся при пальпации [37]. При пальцевом ректальном исследовании в случае атрезии толстой и сигмовидной кишки может быть выявлено запустение ампулы прямой кишки [34].
В некоторых случаях рекомендуют рассмотреть применение магнитно-резонансной томографии плода, чтобы подтвердить ВПР ЖКТ и оценить дополнительные структурные аномалии [32].
Уже в неонатальном периоде наибольшую информативность в инструментальной диагностике ВПР ЖКТ составляет рентгенологическое исследование, которое при различных пороках проводится различными методиками. Рентгенологическое исследование необходимо начинать с обзорной рентгенограммы в вертикальном положении ребенка, желательно в прямой и боковой проекции, а только затем переходить к другим методам, в том числе и к контрастированию [31].
При диагностике АП бесконтрастным методом считается рентгенография, с введением рентгенконтрастного катетера, конец которого отчетливо виден в слепом отрезке пищевода [17], отмечается компрессия и отклонение трахеи [32]. Выявление газового пузыря в желудке и пневмотоза кишечника свидетельствует о наличии АП с дистальным ТПС [34]. При бессвищевых формах газ в желудке отсутствует [17]. При проведении контрастной рентгенографии категорически противопоказано применение бариевой взвеси [31], в данном случае непосредственно в зонд вводится водорастворимое контрастное вещество. При наличии АП четко виден слепой конец пищевода, а при наличии трахео-пищеводных свищей наблюдается затекание контраста в трахею [17].
Рентген-диагностика атрезии ДПК начинается с обзорной рентгенографии в прямой и боковой проекциях [33]. На рентгенографии так же, как и при антенатальной УЗИ диагностике, обнаруживается два газовых пузыря с уровнем жидкости в верхнем этаже и отсутствие воздуха в остальных отделах кишечника [25, 26, 34, 35]. Такая рентгенологическая картина абсолютно достоверна и не требует проведения дополнительных методов исследований, в том числе и с использованием контраста [31, 34]. До проведения обзорной рентгенографии у детей с подозрением на атрезию ДПК не следует зондировать желудок и делать клизму, так как это может снизить информативность рентгенологической картины [31, 34].
При атрезии тонкого кишечника на обзорной рентгенограмме повышенное наполнение петель тонкой кишки, множественные уровни жидкости, затемнение нижней половины брюшной полости, при ирригоскопии кишечник сужен, гаустрация выраженная [37]. Проводится обзорная рентгенография брюшной полости в переднезадней проекции лежа на спине, а также в боковой проекции слева, где определяются уровни жидкости слева и справа в зависимости от уровня обструкции [25].
При атрезии толстого кишечника на обзорной рентгенограмме брюшной полости в вертикальном положении можно выявить повышенное газонаполнение петель кишечника, дилятированные петли, иногда наличие уровней жидкости [37].
Для установления диагноза атрезии аноректальной области необходимо провести специализированное рентгенологическое исследование – рентгенографию по Вангестину. Техника данного метода заключается в том, что исследование проводится в положении вниз головой, наложив контрастную метку на место отсевающего ануса. Рентгенография проводится через 12–18 ч после рождения, после заполнения прямой кишки воздухом. На рентгенограмме обнаруживается область, не заполненная газами кишечника. По расстоянию между слепым концом кишки (газовый пузырь) и условной меткой на промежности судят о высоте атрезии [38]. Если наложена калостома, следует провести рентгенологическое исследование с контрастным веществом дистального отдела кишечника для установления уровня, на котором оканчивается прямая кишка, а также наличия или отсутствия свища [26].
Благодаря своевременной диагностике порока развития, оказании помощи в высокоспециализированном медицинском учреждении в более ранние сроки, раннее взятие беременных на диспансерный учет, использование УЗИ экспертного класса, использование других современных методов антенатальной диагностики ВПР, такого как генетический анализ, развитию организации хирургической помощи выживаемость новорожденных с ВПР ЖКТ имеет тенденцию к повышению за последние 30 лет [23, 39, 40]. При необходимости, учитывая высокую летальность при определенных пороках развития, необходимо решение вопроса о прерывании беременности [40].
Большое влияние на выживаемость оказывает форма ВПР ЖКТ и его сочетанность с другими пороками развития. Например, при изолированной форме атрезии пищевода выживаемость составляет 78–95 % [39]. Прогноз при атрезии ДПК напрямую зависит от характера поражения, его сочетанности с другими пороками, а также со своевременностью диагностики. Процент выживаемости детей после хирургического вмешательства при атрезии ДПК лежит в размахе от 42 до 86 % [22]. Выживаемость детей при атрезии тонкого кишечника в последние годы составляет 84–96 % [40]. Выживаемость новорожденных при атрезии толстого кишечника варьирует от 39 до 100 % [23]. Ранняя диагностика и достижения в области неонатальной анестезии, хирургической техники, лечения сопутствующих аномалий и интенсивной терапии улучшили прогноз. В мировой практике, несмотря на увеличение числа пациентов с тяжелыми врожденными аномалиями, уровень выживаемости достиг 95 % [13].
Традиционно прогноз для детей с ВПР ЖКТ основывался на весе при рождении и наличии сопутствующей патологии, но благодаря достижениям в тактике ухода за новорожденными масса тела при рождении менее влияет на выживаемость, даже если она является очень низкой [13]. Таким образом, остается актуальной антенатальная профилактика развития ВПР ЖКТ, заблаговременное планирование беременности. При ведении беременности, в пренатальный период, стоит уделять значительное внимание соматическому и акушерскому анамнезу матери, необходимо своевременно оценить степень риска развития ВПР ЖКТ. Ввиду недостаточной выявляемости и своевременной ранней диагностике ВПР ЖКТ на ранних этапах развития, согласно приказу о регионализации перинатальной помощи РК от 21 декабря 2007 г. № 746, необходимо направлять определенный контингент беременных женщин, с наличием риска развития ВПР, в соответствующие организации, обеспеченные УЗИ аппаратами экспертного класса и высококвалифицированными специалистами [41]. С последующим решением о тактике ведения беременности, с возможной элиминацией и\или коррекцией беременности.
1. Частота ВПР ЖКТ не имеет тенденции к снижению во многих странах мира.
2. Причины возникновения ВПР ЖКТ остаются малоизвестными.
3. Антенатальная диагностика ВПР ЖКТ возможна благодаря УЗИ-диагностике, достоверность же зависит от порока, а также от качества УЗИ аппарата (экспертное УЗИ) и опыта специалиста.
4. ВПР ЖКТ с первых дней жизни ребенка оказывает прямое влияние на тяжесть состояния новорожденного и требуют своевременной диагностики в родильном доме, квалифицированной неонатальной стабилизации состояния и выхаживания в предоперационный период, грамотной хирургической помощи в период хирургического вмешательства и дальнейшего постоперационного восстановления ребенка.
5. Своевременная антенатальная и неонатальная диагностика ВПР ЖКТ и, как следствие, грамотная тактика ухода за новорожденным и ранняя квалифицированная хирургическая помощь в условиях специализированного медицинского учреждения напрямую влияет на выживаемость новорожденных.
6. На прогноз уровня жизни, инвалидности и выживаемости детей с пороками ЖКТ оказывает влияние форма порока и его сочетанность с другими ВПР.
Авторы выражают благодарность научному руководителю, доценту, кандидату медицинских наук, профессору КГМУ К.А. Кенжебаевой как наставнику, обеспечивающему всяческую поддержку в работе.