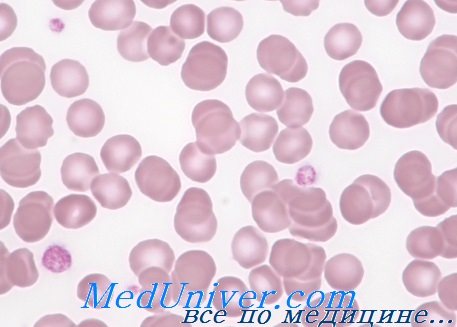
Много тромбоцитов в крови у ребенка что это значит
Много тромбоцитов в крови у ребенка что это значит
Тромбоцитоз – это значительное увеличение количества тромбоцитов в крови, что нарушает свойства крови и повышает вероятность тромбоза (закупорки) сосудов. Тромбоциты – клетки, которые отвечают за свертывание крови.
Тромбоцитоз может быть как самостоятельным заболеванием, так и следствием ряда болезней крови или каких-либо органов.
Первичная тромбоцитемия встречается чаще всего у людей старше 60 лет. Прогноз при этом благоприятный – продолжительность жизни пациентов первичным тромбоцитозом при правильном наблюдении и лечении практически не отличается от таковой у здоровых людей.
Вторичному тромбоцитозу больше подвержены дети младшего возраста. Количество тромбоцитов обычно нормализуется после выздоровления от основного заболевания.
Эссенциальная тромбоцитемия, первичная тромбоцитемия, вторичная тромбоцитемия, тромбоцитофилия, хроническая тромбоцитемия, хронический мегакариоцитарный лейкоз, идиопатическиая тромбоцитемия.
Синонимы английские
Primary thrombocythemia, essential thrombocythemia, idiopathic thrombocythemia, primary thrombocytosis, essential thrombocytosis, secondary thrombocytosis, reactive thrombocytosis, secondary thrombocythemia.
Симптомы обычно развиваются постепенно и на начальных стадиях заболевания могут отсутствовать. Основные проявления тромбоцитоза обусловлены двумя факторами: образованием тромбов в кровеносных сосудах и увеличением кровоточивости. При вторичной тромбоцитемии вероятность этих нарушений ниже, так как количество тромбоцитов меньше, чем при первичной тромбоцитемии.
Основные симптомы тромбоцитоза:
Общая информация о заболевании
Тромбоциты представляют собой мелкие бесцветные пластинки, не содержащие ядра. Они образуются в костном мозге и являются «осколками» мегакариоцитов – гигантских многоядерных клеток. Из костного мозга тромбоциты поступают в кровь, а часть из них задерживается в селезенке. Они существуют около 7-10 дней, а затем уничтожаются клетками печени и селезенки. Тромбоциты отвечают за свертываемость крови и остановку кровотечений. Их нормальное количество в крови составляет 150-450×10 9 /л.
Выделяют два варианта тромбоцитоза.
1. Первичный тромбоцитоз. В этом случае в костном мозге образуется повышенное количество мегакариоцитов, что увеличивает количество тромбоцитов, имеющих нормальную продолжительность жизни, но неправильное строение и нарушенные функции. Тромбоциты крупные, усиливается тенденция к образованию сгустков, закупоривающих кровеносные сосуды, и к кровотечениям. Кровотечения возникают за счет нарушения слипания тромбоцитов, а также из-за того, что большая их часть может использоваться для образования кровяных сгустков. Это может приводить к тяжелым осложнениям: инсульту, инфаркту миокарда, желудочно-кишечным кровотечениям. Причины нарушения деления мегакариоцитов в костном мозге до конца неизвестны, однако есть информация о наличии у пациентов мутации в гене V617F. Первичный тромбоцитоз относится к миелопролиферативным заболеваниям, при которых нарушается кроветворная функция костного мозга, что стимулирует образование клеток крови.
2. Вторичный (реактивный) тромбоцитоз. При нем тромбоциты функционируют нормально, а причиной самого заболевания является какое-то другое отклонение, одно из нижеприведенных.
Такой тромбоцитоз всегда длится недолго и исчезает при нормализации состояния пациента.
Вероятность образования сгустков и кровотечений при вторичном тромбоцитозе ниже, чем при первичном.
Кто в группе риска?
Часто тромбоцитоз протекает бессимптомно. Врач может заподозрить его во время стандартного профилактического осмотра. Важным моментом диагностики является определение вида тромбоцитоза – первичный или вторичный. В случае вторичного тромбоцитоза врач может назначить ряд дополнительных исследований, необходимых для выяснения его причины.
Лечение первичного тромбоцитоза зависит от риска возникновения осложнений – тромбозов и кровотечений. Это определяется возрастом, наличием сопутствующих заболеваний (например, сахарного диабета, сердечно-сосудистых заболеваний), уровнем тромбоцитов. Если вероятность осложнений велика, то используют:
Лечение вторичного тромбоцитоза определяется его непосредственной причиной. Как правило, при выздоровлении пациента от основного заболевания уровень тромбоцитов нормализуется. Кроме того, длительный вторичный тромбоцитоз может развиться после спленэктомии, тогда пациенту назначают небольшие дозы аспирина или лекарств, его содержащих, для предотвращения осложнений.
Профилактики первичного тромбоцитоза нет.
Профилактика вторичного тромбоцитоза заключается в профилактических осмотрах и своевременном выявлении болезней, способных привести к вторичному увеличению количества тромбоцитов.
Много тромбоцитов в крови у ребенка что это значит
Тромбоцитопения — состояние, при котором количество тромбоцитов ниже 150х109/л. Риск кровотечений зависит от количества тромбоцитов.
• Тяжёлая тромбоцитопения (количество тромбоцитов
Диагностика иммунной тромбоцитопении у детей
Иммунная тромбоцитопения — диагноз исключения, поэтому необходимо уделить большое внимание анамнезу, клиническим особенностям и мазку крови для того, чтобы быть уверенным, что ни один более тяжёлый диагноз не был пропущен. У детей младшего возраста необходимо предположить врождённые причины (такие как синдромы Вискотта-Олдрича или Бер-нара-Сулье). Любые атипичные клинические проявления, как, например, наличие гепатоспленоме-галии или выраженной лимфаденопатии, требуют немедленного исследования костного мозга для исключения острой лейкемии или апластической анемии.
Необходимо провести исследование костного мозга, если планируется лечение ребёнка глюкокортикоидами, поскольку эта терапия может временно маскировать эти заболевания. Также необходимо предположить СКВ. Однако если имеются характерные клинические симптомы при отсутствии изменений в крови, за исключением низкого количества тромбоцитов, и нет намерения проводить лечение, то исследование костного мозга не требуется.
При иммунной тромбоцитопении, за исключением выразительных кожых проявлений и значительно сниженного количества тромбоцитов, состояние хорошее и у большинства пациентов происходит быстрая ремиссия без каких-либо вмешательств.
Ведение детей с иммунной тромбоцитопенией
Приблизительно у 80% детей болезнь протекает остро, доброкачественно и обычно спонтанно разрешается в течение 6-8 нед. Большинству детей помощь может оказываться на дому, госпитализация и не требуется. Подход к лечению противоречивый. Большинству детей не требуется никакая терапия, даже если количество тромбоцитов составляет менее 10х109/л, однако необходимо начать лечение, если есть признаки массивного кровотечения (например, внутричерепного или желудочно-кишечного) или продолжающееся небольшое кровотечение (например, постоянная кровоточивость ротовой полости).
Для лечения используется преднизолон внутрь или иммуноглобулин внутривенно, однако оба они имеют значительные побочные эффекты и не влияют на шанс достижения полной ремиссии. Инфузии иммуноглобулина обычно приводят к более быстрому увеличению числа тромбоцитов, чем глюкокортикоиды. Трансфузии тромбоцитарной массы оставляют для жизнеугрожающих кровотечений, поскольку они поднимают уровень тромбоцитов лишь на несколько часов. Преднизолон должен применяться лишь короткими курсами независимо от числа тромбоцитов. У родителей должен быть свободный 24-часовой доступ в клинику.
Ребёнок должен избегать травм, насколько это возможно, и контактных видов спорта до тех пор, пока сохраняется очень низкое число тромбоцитов.
Хроническая иммунная тромбоцитопения у детей
У 20% детей количество тромбоцитов остаётся низким через 6 мес после установления диагноза, это известно как хроническая иммунная тромбоцитопения у детей. Никакое лечение не проводится до тех пор, пока не произойдет массивное кровотечение. Как и при острой иммунной тромбоцитопении у детей, не должны применяться длительные курсы глюкокортикоидной терапии. Поэтому терапия в основном поддерживающая, ребёнок должен избегать контактных видов спорта, однако должен стимулироваться для продолжения нормальной жизнедеятельности, в том числе посещения школы.
Как и при острой иммунной тромбоцитопении у детей, родителям необходим 24-часовой доступ к медицинской помощи. Семье может пойти на пользу общение с группой поддержки родителей детей, страдающих иммунной тромбоцитопенией. У большинства детей наступает выздоровление в течение 3 лет или стабилизация с сохранением умеренной асимптомной тромбоцитопении. Случаи профузных кровотечений являются редкими и требуют помощи специалистов. Спленэктомия является, вероятно, наиболее эффективным лечением в этой группе пациентов, но приводит к значительному увеличению заболеваемости и в 25% случаев может оказаться бесполезным. Если иммунная тромбоцитопения у ребёнка переходит в хроническую форму, требуется проведение регулярных обследований на наличие СКВ, поскольку тромбоцитопения может предшествовать появлению маркёров этого заболевания.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
С эволюционной точки зрения клеточные медиаторы гемостаза и иммунной защиты не всегда были разделены. У беспозвоночных тип клеток, называемый гемоцитом, защищает хозяина от вторжения микробов, и эта же клетка также предотвращает потерю «крови» (т.е. гемолимфы) при повреждении, вызывая коагуляцию. У высокоразвитых видов гемостаз и иммунный ответ разделены, и лейкоциты возобновляют функции иммунного ответа, в то время как тромбоциты поддерживают гемостаз.
После эритроцитов тромбоциты являются второй по численности популяцией клеток в крови. Обычное количество тромбоцитов колеблется от 150000 до 450000 тромбоцитов на микролитр. Тромбоцитопения, которая представляет собой снижение количества тромбоцитов, вызванное либо снижением выработки тромбоцитов, либо увеличением разрушения тромбоцитов, связано с повышенным риском кровотечения.
Вирусы могут модулировать выработку тромбоцитов на разных этапах развития. Они способны влиять на профиль цитокинов хозяина, что приводит к изменению продукции ТРО в печени. Примеры этого включают в себя: вирус иммунодефицита обезьян (SIV), который запускает продукцию TPO посредством активизации фактора роста опухоли (TGF); вирус герпеса человека 6, который может препятствовать образованию колоний мегакариоцитов, индуцируемых ТРО; вирус герпеса человека 7, который ухудшает выживание и дифференцировку мегакариоцитов. Некоторые вирусы также напрямую влияют на выработку ТРО, разрушая ткани печени, как показано для вируса гепатита С. Результирующее снижение выработки ТРО приводит к задержке развития мегакариоцитов и снижению выработки тромбоцитов. Другие вирусы инфицируют стромальные клетки костного мозга и гематопоэтические стволовые клетки, что приводит к измененной выработке цитокинов и уменьшению числа клеток-предшественников, нарушая тем самым гематопоэз.
В течение десятилетий считалось, что эти две системы действуют независимо, но в последнее время эта концепция подвергается сомнению. Появляющиеся данные свидетельствуют о том, что границы между коагуляцией и иммунной защитой на самом деле не такие четкие, как первоначально предполагалось. Недавно была предложена новая концепция вовлечения иммунных клеток в гемостаз, называемая иммунотромбозом, которая предполагает функцию врожденных иммунных клеток при тромбозе. С другой стороны, важная роль тромбоцитов в иммунной реакции становится все более и более очевидным.
В 1882 году Биззозеро ( Bizzozero) открыл тромбоциты в качестве третьего морфологического элемента в крови и выяснил функцию этих клеток при гемостазе и тромбозе. Долгое время считалось, что тромбоциты и их содержание в гранулах в основном обеспечивают активацию системы коагуляции и рекрутирование других тромбоцитов для остановки кровопотери при повреждении. Было отмечено, что нежелательная активация тромбоцитов происходит в ответ на внутренние повреждения, например денудацию и эрозию поверхности эндотелия или разрыв атеросклеротической бляшки. Следовательно, предполагалось, что тромбоциты ответственны за стадии сердечно-сосудистых заболеваний, особенно, тогда, когда нестабильные тромбы закупоривают мелкие сосуды, тем самым нарушая снабжение кислородом целевых органов. Тем не менее, тромбоциты участвуют в гораздо большем количестве процессов, и они реагируют и взаимодействуют с гораздо большим количеством триггеров, чем первоначально предполагалось. Помимо своей центральной роли в гемостазе, тромбоциты модулируют воспалительные реакции и иммунные реакции путем прямого взаимодействия с лейкоцитами, а также эндотелиальными клетками и высвобождения растворимых медиаторов воспаления, которые усиливают рекрутирование лейкоцитов и запускают их активацию.
На сегодняшний день роль тромбоцитов в ответ на вторжение патогенов до конца не изучена. Взаимодействия тромбоцитов и микробов, по-видимому, полезны для хозяина из-за усиления иммунных реакций. Однако, предполагается, что взаимодействие тромбоцитов с патогенными микроорганизмами приносит пользу вирусу или бактериям, поскольку тромбоциты обеспечивают защиту от лейкоцитов, противовирусных агентов и антибиотиков. Кроме того, «липкость» тромбоцитов может ослаблять микроб-эндотелиальные взаимодействия и облегчать инфицирование с помощью механизмов, аналогичных тем, которые недавно были описаны для взаимодействий тромбоцитов с циркулирующими опухолевыми клетками.
Тромбоцитопения часто возникает после вирусных инфекций, и вирусы используют различные стратегии для снижения уровня циркулирующих тромбоцитов. Поскольку вирус-опосредованная тромбоцитопения часто является многофакторной и отличается между вирусными инфекциями, механизмы, с помощью которых вирусы запускают тромбоцитопению различны.
Передача сигналов извне через связывание рецептора способствует полимеризации актина и распространению тромбоцитов и, таким образом, может усиливать прикрепление вируса к эндотелиальным клеткам, но также способствует клиренсу тромбоцитов.
Однако тромбоциты активируются не только прямым взаимодействием с вирусами. Механизмы защиты хозяина в ответ на вирусные инфекции также могут приводить к активации тромбоцитов. Например, многие вирусные инфекции приводят к системному воспалению, которое, в свою очередь, запускает активацию тромбоцитов и уменьшает продолжительность жизни тромбоцитов. Среди прочего, инфекция вирусом гриппа, риновирусом и ЦМВ приводит к повышенной регуляции цитокинов, таких как интерлейкин 6 (IL-6), в клетках-мишенях.
Несколько вирусных инфекций активируют каскад коагуляции посредством индукции экспрессии тканевого фактора (TF) в клетках-мишенях. Генерация тромбина активированным каскадом коагуляции вызывает активацию тромбоцитов и последующий клиренс посредством передачи сигналов рецептора, активирующего протеазу (PAR). PAR на тромбоцитах, эндотелиальных клетках и лейкоцитах являются важными модуляторами во время вирусных инфекций, которые модулируют врожденные иммунные ответы и оказывают положительное и отрицательное влияние на TLR-зависимые ответы.
Кроме того, было показано, что выработка B-лимфоцитами антител против некоторых вирусов влияет на выживание тромбоцитов. Эти антитела, которые обычно нацелены на поверхностные гликопротеины вирусов, проявляют перекрестную реактивность с поверхностными интергринами тромбоцитов, такими как GPIIb / IIIa или GPIb-IX-V. Эта так называемая идиопатическая тромбоцитопеническая пурпура (ITP) или тромбоцитопения, вызванная аутоантителами тромбоцитов, была описана для HCV, ВИЧ, CMV, EBV, хантавируса, вируса ветряной оспы, вирусов герпеса и тяжелого острого респираторного синдрома коронавируса. Кроме того, разрушение тромбоцитов в ответ на вирусные инфекции может происходить из-за нарушения давления в воротной вене и повышенной секвестрации тромбоцитов увеличенной селезенкой, как в случае инфекции вирусом.
Тромбоцитопения, вызванная вирусом иммунодефицита человека, обусловлена несколькими механизмами. Вкратце, ВИЧ приводит к нарушению выживания мегакариоцитов костного мозга и их предшественников. ВИЧ также уменьшает количество и активность клеток-предшественников человека и уменьшает созревание и плоидность мегакариоцитов. Поверхностный гликопротеин ВИЧ gp120 приводит к усилению апоптоза мегакариоцитов in vitro из-за увеличения TGFβ и подавления индуцирующего пролиферацию члена 13 суперсемейства лигандов фактора некроза лигандов (TNFSF13). Кроме того, gp120 взаимодействует с CD4, который экспрессируется незрелыми мегакариоцитами, которые также экспрессируют CCR5, и приводит к их инфекции. Кроме того, ВИЧ-инфекция мегакариоцитов может привести к снижению экспрессии рецептора ТРО (c-Mpl).
При инфицировании вирусом денге продуцирование тромбоцитов нарушается подавлением мегакариопоэза через инфицирование кроветворных клеток-предшественников или косвенно через измененные уровни цитокинов в костном мозге из-за нарушения функции стромальных клеток. Тромбоциты от пациентов с инфекцией денге имеют признаки активации, митохондриальной дисфункции и усиленного апоптоза, которые могут способствовать возникновению тромбоцитопении. Кроме того, усиленное разрушение тромбоцитов происходит из-за перекрестной реакции тромбоцитов с антителами против вируса денге. Индуцированный вирусом денге неструктурный белок-1 (NS-1) вызывает опосредованный комплементом лизис тромбоцитов и тем самым еще больше ускоряет тромбоцитопению. NS-1 также может активировать эндотелиальные клетки и приводит к увеличению проницаемости сосудов и дальнейшей активации тромбоцитов. Инфицированные вирусом денге пациенты обнаруживают повышенный уровень E-селектина на поверхности своих эндотелиальных клеток, что способствует адгезии и клиренсу тромбоцитов, а также усиленной активации каскада коагуляции.
Инфекция Arenaviruses вирусом лимфоцитарного хориоменингита (LCMV) или вирусом Junin приводит к тромбоцитопении и снижению индуцированных агонистом реакций тромбоцитов у мышей. Как следствие, истощение тромбоцитов у LMCV-инфицированных мышей приводит к летальной геморрагической анемии. Этот эффект вызван уменьшением реакции тромбоцитов, а не только падением количества тромбоцитов. Было установлено, что лежащий в основе механизм изменения продукции тромбоцитов и снижения их реактивности зависит от индуцированной вирусом продукции интерферона (IFN) α / β.
Вирус Джунина в основном заражает CD34 +клетки не являются мегакариоцитами, но ухудшают образование пропеллетов и высвобождение тромбоцитов посредством передачи сигналов IFNα / β-рецептора. Передача сигналов IFNα / β-рецептора представляет собой важный паракринный репрессор мегакариопоэза, который непосредственно ингибирует передачу сигналов, индуцированную TPO, посредством индукции супрессора передачи сигналов цитокинов 1 (SOCS-1), индукции 2’5′-олигоаденилатсинтетазы (OAS) и снижение экспрессии ядерного фактора эритроида 2 (NF-E2).
Несмотря на его влияние на образование ТРО, прямое взаимодействие нечеловеческого SIV с тромбоцитами приводит к образованию агрегатов тромбоцитов-моноцитов, что способствует дифференцировке моноцитов в более воспалительный фенотип. Кроме того, активация тромбоцитов запускает клиренс тромбоцитов, когда тромбоциты распознаются макрофагами в селезенке, что приводит к быстрому снижению количества тромбоцитов.
В настоящее время неясно, могут ли и в какой степени вирусы или хозяин извлечь пользу из тромбоцитопении. Было высказано предположение, что подавление гематопоэза, например, при вирусной инфекции денге может играть защитную роль для микроокружения, ограничивая повреждение при удалении инфицированных клеток.
Наиболее распространенным тромбоцитарным киноцидином является фактор тромбоцитов 4 (PF-4 / CXCL4). CXCL4 высвобождается в кровоток при повреждении тканей, воспалении, окислительном стрессе или стимуляции патогенов, таких как взаимодействия тромбоцитов и вирусов. CXCL4 был идентифицирован как ингибитор ВИЧ-1 широкого спектра действия и подавляет заражение ВИЧ-1 Т-лимфоцитами посредством стерического ингибирования путем связывания CXCL4, проксимального с сайтом связывания CD4 на gb120.
Наибольшее количество серотонина в крови хранится в плотных гранулах тромбоцитов, которые также выделяются при активации тромбоцитов. Было установлено, что серотонин является важным медиатором регенерации печени, а также обеспечивает раннюю стимуляцию Т-лимфоцитов. Кроме того, дегрануляция тромбоцитов приводит к поверхностной экспрессии P-селектина, который является частью внутренней мембраны α-гранул, которая сливается с наружной мембраной тромбоцитов при экзоцитозе гранул. P-селектин взаимодействует со своим контррецептором P-селектина гликопротеиновым лигандом-1 (PSGL-1), который конститутивно экспрессируется на поверхности лейкоцитов. Взаимодействие тромбоцитов с лейкоцитами опосредует иммунные ответы во время вирусных инфекций. Прямое взаимодействие с тромбоцитами приводит к активации лейкоцитов, что приводит к усилению фагоцитоза и реактивной продукции кислорода нейтрофилами, а также образованию внеклеточной ловушки нейтрофилов. Взаимодействие тромбоцитов с моноцитами приводит к повышенной активации и дифференцировке и повышает поверхностную экспрессию моноцитов TF и образование микрочастиц.
Опосредованная вирусом активация тромбоцитов и последующее выделение цитокинов из тромбоцитов не только защищает хозяина, но также может иметь нежелательные последствия для хозяина. Хотя в нескольких сообщениях указывается, что CXCL4 является широким спектром средств подавления ВИЧ-инфекции, в одном сообщении указывается, что CXCL4 тромбоцитов может также способствовать заражению макрофагов человека ВИЧ-1 и потенцировать репликацию вируса. Кроме того, было показано, что CXCL4 опосредует фиброз печени на экспериментальных моделях мышей, что указывает на то, что этот хемокин может играть роль в опосредованном тромбоцитами ускорении вызванного гепатитом фиброза печени. Полученный из тромбоцитов серотонин приводит к задержке проникновения активированных цитотоксических Т-лимфоцитов в печень, что замедляет вирусный контроль и поддерживает персистенцию вируса в печени. Это приводит к усилению вирусопатологической иммунопатологии. Предполагается, что инфекция мегакариоцитов и последующая модуляция функции тромбоцитов ЦМВ являются причиной недостаточности трансплантата при аллергенной трансплантации костного мозга.
Первичный и вторичный гемостаз работают плотно вместе. Дисбаланс одной из систем приводит к нарушению функции другой. Активация каскада коагуляции наблюдалась при различных вирусных инфекциях, включая ВИЧ, инфекцию денге и вирус Эбола, и может обеспечить механизм защиты хозяина для ограничения распространения патогенных микроорганизмов. Изменения в активации каскада коагуляции и модуляции количества и функции тромбоцитов, которые также наблюдаются при вирусных инфекциях, приводят к повышенному риску диссеминированного сосудистого свертывания (ДВС-синдром), тромбоза глубоких вен (ТГВ) и кровоизлияний у инфицированных пациентов. Тромбоцитопения является распространенным результатом вирусных инфекций и связана с повышенным риском кровотечения. Приблизительно 10% ВИЧ-положительных пациентов и до 60% пациентов с синдромом приобретенного иммунодефицита (СПИД) страдают от тромбоцитопении, которая может привести к тяжелым кровотечениям у этих пациентов. При многих вирусных инфекциях функция тромбоцитов и агрегация в ответ на различные агонисты уменьшаются, вызывая осложнения кровотечения при вирусных геморрагических лихорадках. Вспышки последних приводят к гибели тысяч людей каждый год и вызваны различными РНК-вирусами с оболочкой, которые включают Arenaviridae (например, вирус Lassa), Bunyaviridea (например, hantavirus),Filioviridae (например, вирус Марбург и Эбола) и Flaviviridae (например, вирус денге).
Следует отметить, что недавно было показано, что уменьшение количества тромбоцитов более чем на 85% необходимо для возникновения кровоизлияний, что указывает на то, что очень низкий процент тромбоцитов достаточен для поддержания целостности сосудов. На модели LCMV было продемонстрировано, что даже у тяжелых мышей с тромбоцитопенией развиваются только локальные кровоизлияния в местах воспаления, и что LCMV-зависимые кровотечения являются результатом дисфункции тромбоцитов, вызванной передачей сигналов IFNα / β. У мышей, у которых отсутствует функциональный рецептор IFNα / β, наблюдается менее выраженная анемия и кровоизлияния из-за восстановленной способности к агрегации тромбоцитов во время инфекции LCMV. Это указывает на то, что дисфункция тромбоцитов имеет более выраженные эффекты, чем тромбоцитопения при этих патологиях. Следует отметить, что многие вирусы VHF ингибируют функцию тромбоцитов. Вирус Джунина, вызывающий аргентинскую геморрагическую лихорадку, вызывает зависимое от передачи сигналов IFNα / β снижение продукции и функции тромбоцитов. Вирус Эбола также вызывает увеличение IFNα, что коррелирует с увеличением летальности. Инфекция Эбола также вызывает экспрессию TF, которая связана с геморрагической лихорадкой Эбола. Хантавирус и лассавирус также отменяют реакции тромбоцитов через плазменное ингибирование и / или прямое взаимодействие тромбоцитов.
Хотя тромбоцитопения часто наблюдается у пациентов с инфекциями денге, кровотечения редки. Однако, если кровотечение действительно происходит, это связано с высоким риском смертности. Следует отметить, что у пациентов, инфицированных вирусом денге, количество тромбоцитов не предсказывает риск кровотечения. Однако системная активация тромбоцитов может вносить вклад в прокоагуляционное состояние у этих пациентов, у которых часто развивается ДВС-синдром. Кроме того, повышенная активация тромбоцитов связана с утечкой плазмы. Инфекция гриппа H1N1 усиливает активацию циркулирующих тромбоцитов и приводит к увеличению числа случаев тромбоза.
Существует некоторое расхождение в отношении достоверности данных, касающихся инфекции ВПГ и сердечно-сосудистых заболеваний, и, несмотря на ее провоспалительные реакции, наблюдается отрицательная связь между инфекцией ВПЧ и сердечно-сосудистыми заболеваниями.
Более того, связь между ВИЧ-инфекцией и сердечно-сосудистыми заболеваниями остается противоречивой, и сама антиретровирусная терапия изменяет функцию тромбоцитов и представляет собой независимый фактор риска развития атеросклероза. Необходимы дальнейшие исследования для оценки вклада тромбоцитарных взаимодействий в сердечно-сосудистые заболевания.
Сообщалось, что тромбоциты и их высвобождаемые продукты прямо и косвенно подавляют инфекцию, а также поддерживают устойчивость вируса в ответ на определенные вирусы, делая тромбоциты обоюдоострым мечом при вирусных инфекциях. Тромбоциты участвуют в различных осложнениях в ответ на вирусную инфекцию, но также играют ключевую роль в сохранении адекватных ответов хозяина. Тромбоцитопения является распространенным осложнением при нескольких вирусных инфекциях, и вирусы применяют различные стратегии для опосредования распада тромбоцитов. Вопрос о том, является ли тромбоцитопения вирусной стратегией для уклонения от иммунных ответов или имеет ли она защитные функции для хозяина, по-видимому, зависит от варианта вируса и лежащей в основе патологии. Необходимы дальнейшие исследования, чтобы полностью понять роль тромбоцитов в вирусных инфекциях и получить четкое представление о влиянии анти-тромбоцитарной терапии при вирусных инфекциях. Эти исследования помогут нам предсказать пользу или недостаток тромбоцитов и их ингибирование при вирусных инфекциях.