Сидеробластная анемия что это такое простыми словами
Сидеробластная анемия
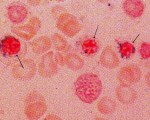
Сидеробластная анемия — это гетерогенная группа наследственных или приобретенных заболеваний, характеризующихся анемиями различной степени тяжести и специфическими клетками-сидеробластами в костном мозге.
По данным ВОЗ, для сидеробластной анемии характерна изолированная дисплазия эритроидных бластов, а также появление в костном мозге овальных сидеробластов.
В медицинской литературе сидеробластами называют эритробласты с не менее чем пятью сидеротическими слоями, общий размер которых составляет, по крайней мере, треть длины окружности ядра эритробласта.
Сидеробластная анемия, как правило, связана с микроцитозом (в периферической крови преобладают микроциты) и гипохромией (кровяной цветовой показатель ниже 0,8). Именно этим она отличается от железодефицитной анемии и талассемии. Хотя железо в необходимых количествах при данном заболевании присутствует, наблюдается митохондриальный дефект, который не дает железу попадать в гемоглобин. Вместо железа в митохондриях накапливаются красные клеточные ядра, образуя «кольца» сидеробластов.
Избыточное накопление красных клеточных ядер происходит за счет снижения синтеза гемоглобина. Это состояние может быть как врожденным, так и приобретенным. Чаще встречается приобретенная форма заболевания. Иногда она является определенным этапом развития миелодиспластического синдрома (МДС). Множество случаев сидеробластной анемии связаны с алкогольной зависимостью, лекарственными препаратами.
Наследственная сидеробластная анемия
Наследственная сидеробластная анемия называется также Х-хромосомной сидеробластной анемией и передается в женской хромосоме.
В 1945 году доктор Томас Кули описал первые случаи Х-хромосомной сидеробластной анемии у двух братьев из многодетной семьи, в которой наследование заболевания наступило через шесть поколений. Первый генетический дефект, ответственный за появление данного заболевания — нарушения в гене ALAS-2, второй — аномалия Xq13 в Х-хромосоме. Также последние исследования в данной области подтверждают связь заболевания с геном фосфоглицераткиназы (ФГК), наблюдаемой при синдроме Менкеса (врожденной аномалии транспортировки меди). Медь имеет большое значение для клеточного усвоения железа из трансферрина. Кроме того, она является кофактором ферментов митохондриальной цепи при переносе электронов. Изменение в хромосомной области Xq13 нарушает клеточный метаболизм меди.
Сидеробластная анемия в этом случае будет вторичным заболеванием, которое сопровождает нарушения обмена веществ. Мутации гена могут быть классифицированы в соответствии с их влиянием на ферменты: низким сродством к пиридоксальфосфату, структурной нестабильностью, аномальными каталитическими свойствами или повышенной восприимчивостью к митохондриальной протеазе. Любая из этих аномалий замедляет биосинтез, следовательно, снижается производство таких составляющих крови, как гемы. В конце концов, появляется низкая производительность гемоглобина, развивается анемия. Наследственная Х-хромосомная сидеробластная анемия обычно чаще встречается у мужчин.
Митохондриальная цитопатия
Группа расстройств, в ходе которых происходит удаление части митохондриального генома (от 30 до 16%), то есть его делеция (утрата хромосомного участка). Независимая митохондриальная репликация в сочетании со случайной сегрегацией дочерних клеток при митозе приводит к тому, что новореплицированные клетки могут иметь большее или меньшее количество дефектных митохондрий. Этот процесс случайный, и предугадать, какое количество дефектных митохондрий будет в клетке, невозможно. Митохондрии передаются ребенку матерью. Следовательно, митохондриальная цитопатия передается по материнской линии, и мать с умеренным проявлением заболевания может иметь одного здорового ребенка и одного тяжелобольного ребенка с митохондриальной гетероплазией (при этом заболевании одна и та же клетка может содержать и здоровые, и дефектные митохондрии).
Вторичная сидеробластная анемия, связанная с заболеваниями и приемом лекарственных препаратов
Большинство сидеробластных анемий связаны с употреблением медикаментов, а также алкоголя и различных химических веществ, тяжелых металлов (например, свинца), гематологическими, неопластическими и воспалительными заболеваниями.
Приобретенная форма заболевания встречается намного чаще наследственной. Состояние иногда сопутствует миелодиспластическому синдрому. Проявляются наследственные формы почти всегда в младенчестве или в детстве. Приобретенные в основном возникают в пожилом возрасте. Миелодиспластический синдром — это группа расстройств, для которой характерна гемопоэтическая дисфункция стволовых клеток. Приводят к ухудшению функции мозга, цитопении периферической крови. Примерно у 15% пациентов с миелодисплазией развивается острый лейкоз.
Лекарственная и токсин-индуцированная сидеробластная анемия появляется под воздействием активного вещества лекарства или токсина. Обычно при устранении главного раздражающего фактора такая анемия исчезает, то есть довольно легко поддается лечению и устранению без дополнительного приема лекарственных препаратов.
Сидеробластная анемия вследствие токсинов — самая распространенная форма приобретенного заболевания этого вида. Основное раздражающее вещество – этанол. Именно поэтому у людей, страдающих алкоголизмом, это заболевание встречается чаще.
Этанол вызывает сидеробластную анемию пиридоксинреагирующую (избыток пиридоксальфосфата) и дефицит пиридоксальфосфата.
Свинцовая интоксикация быстро приводит к сидеробластной анемии из-за быстрой всасываемости в ткани. Если в организме имеется хотя бы небольшой железодефицит, интоксикация свинцом будет проходить намного быстрее. В настоящее время практически во всех странах мира запрещено использование свинцовых красок, а также различных строительных материалов на основе этого компонента.
Многие страны запретили производить бензин с добавлением свинца. К сожалению, запрет действует не во всех странах мира. Многие бедные страны продолжают использовать бензин, содержащий свинец, поскольку он дает большее количество энергии на литр и менее дорогой, чем бензин высокой степени рафинации. Автомобильные выхлопы и промышленная отработка загрязняют свинцом почву и питьевую воду.
Пиридоксинреагирующая анемия
Пиридоксин — это вещество, которое является производной от пиридина – активного соединения, проявляющего свойства витаминов группы В. Вот почему различные виды анемии так часто связаны с питанием, в частности, недоеданием. Ведь витамины группы В организм получает преимущественно из пищи, и дефицит питательных веществ очень быстро сказывается на состоянии здоровья человека.
Первичная недостаточность пиридоксина, как правило, вторична по отношению к недоеданию. В клинической картине больного с дефицитом пиридоксина преобладает периферическая невропатия и дерматит.
Пиридоксальфосфат — это витамин В6. Он принимает активное участие в синтезировании различных белков, в том числе и гемоглобина, глютаминовой кислоты, а также превращает фолиевую кислоту, поступающую с пищей, в форму, пригодную для усвоения и переработки в организме человека. Без этого вещества печень, нервная система, сердце и другие внутренние системы и органы не смогут функционировать нормально.
Пиридоксинреагирующая анемия возникает не только из-за недополучения витамина В6, но и из-за избыточного его количества. Особенно это характерно для больных, проходящих лечение от туберкулеза (они принимают такие препараты, как фтивазид, тубазид, изониазид и другие).
Симптомы и лечение сидеробластных анемий
Основные симптомы сидеробластных анемий и всех их подвидов:
Первым шагом в лечении сидеробластной анемии является исключение внешних раздражающих факторов: алкоголя, токсичных веществ, а также различных лекарственных препаратов (если это возможно, уменьшить дозировку). При пиридоксинреагирующей анемии необходим прием пиридоксина, начиная с дозировки 100-200 мг и до 500 мг. Показан прием фолиевой кислоты, которая компенсирует возможный эритропоэз.
Редко применяемые методы лечения: трансплантация стволовых клеток. Однако этого вида лечения рекомендуется избегать, особенно у пожилых пациентов, так как он связан с высоким риском для жизни. Пациенты с тяжелыми формами наследственной сидеробластной анемии и их семьи должны получить консультацию у генетика.
5 вариантов завтрака, которые помогут избавиться от жира на животе
Неправильные формы микропластика разрушают клетки человека и вызывают аллергию
Бег в районах с плохой экологией так же опасен, как и низкий уровень физической активности
Ученые: Из-за устойчивости к антибиотикам будет ежегодно погибать 10 млн человек
Деятельность, которая может спровоцировать инсульт в течение следующих 60 минут
Исследование: Человек эволюционировал и стал жить долго благодаря постоянной физической нагрузке
Публикации в СМИ
Анемии сидеробластные
Сидеробластная сидероахрестическая анемия (сидероахрестическая анемия) — гипохромная микроцитарная гипорегенераторная анемия вследствие нарушения утилизации внутриклеточного железа для синтеза Hb, несмотря на нормальное или повышенное содержание железа в митохондриях эритробластов. В результате в костном мозге увеличивается количество сидеробластов — нормобластов с характерным кольцевидным расположением гранул железа вокруг ядра (кольцевидные сидеробласты).
Диагностика. Нарушение синтеза Hb вызывает снижение среднего содержания Hb в эритроците; появляется популяция гипохромных микроцитов. У пациентов старше 60 лет (а также при врождённой форме у подростков) анемия может быть относительно тяжёлой • В костном мозге — эритроидная гиперплазия, при окраске мазка на железо видны кольцевидные сидеробласты • В сыворотке крови обнаруживают увеличение количества ферритина и значительное увеличение содержания сывороточного железа с высоким насыщением трансферрина • Содержание ретикулоцитов снижено (гипорегенераторная анемия) • Сочетание гипохромных микроцитарных клеток с нормоцитами или даже макроцитами — диагностический признак сидеробластной анемии.
Лечение • Исключение провоцирующих факторов (ЛС, алкоголь) • Всем пациентам следует пробно назначить пиридоксин в больших дозах (в большинстве случаев, исключая почти все наследственные формы, улучшения состояния нет). Аналогичен и эффект андрогенов • Гемотрансфузии (больные часто трансфузиозависимы).
МКБ-10 • D64 Другие анемии
Код вставки на сайт
Анемии сидеробластные
Сидеробластная сидероахрестическая анемия (сидероахрестическая анемия) — гипохромная микроцитарная гипорегенераторная анемия вследствие нарушения утилизации внутриклеточного железа для синтеза Hb, несмотря на нормальное или повышенное содержание железа в митохондриях эритробластов. В результате в костном мозге увеличивается количество сидеробластов — нормобластов с характерным кольцевидным расположением гранул железа вокруг ядра (кольцевидные сидеробласты).
Диагностика. Нарушение синтеза Hb вызывает снижение среднего содержания Hb в эритроците; появляется популяция гипохромных микроцитов. У пациентов старше 60 лет (а также при врождённой форме у подростков) анемия может быть относительно тяжёлой • В костном мозге — эритроидная гиперплазия, при окраске мазка на железо видны кольцевидные сидеробласты • В сыворотке крови обнаруживают увеличение количества ферритина и значительное увеличение содержания сывороточного железа с высоким насыщением трансферрина • Содержание ретикулоцитов снижено (гипорегенераторная анемия) • Сочетание гипохромных микроцитарных клеток с нормоцитами или даже макроцитами — диагностический признак сидеробластной анемии.
Лечение • Исключение провоцирующих факторов (ЛС, алкоголь) • Всем пациентам следует пробно назначить пиридоксин в больших дозах (в большинстве случаев, исключая почти все наследственные формы, улучшения состояния нет). Аналогичен и эффект андрогенов • Гемотрансфузии (больные часто трансфузиозависимы).
Сидеробластная анемия ( Сидероахрестическая анемия )
Сидеробластная анемия – это приобретенное или наследственное заболевание крови, характеризующееся гипохромией эритроцитов, высоким уровнем сывороточного железа с отложением в тканях органов. Клиническая картина представлена анемическим синдромом (головокружение, утомляемость, бледность кожи), гемосидерозом внутренних органов (гепатомегалия, кардиомегалия, ХПН), изменением картины крови. Диагноз выставляется на основании клинических и биохимических анализов (ОАК, сывороточное Fe, ферритин, трансферрин, витамин В6), генодиагностики, исследования миелограммы. Лечение может включать гемотрансфузии, витамино-, гормонотерапию, хелаторную терапию.
МКБ-10
Общие сведения
Сидеробластные (сидероахрестические) анемии включают несколько гетерогенных синдромов, которые протекают с нарушением синтеза гема, несмотря на повышенное содержание железа в плазме. Популяционная частота сидеробластных анемий (СБА) не выяснена ввиду их клинической неоднородности, однако известно, что приобретенные формы встречаются чаще наследственных. Врожденные анемии обычно манифестируют в детстве, но могут оставаться нераспознанными вплоть до зрелого возраста. Первичная приобретенная сидеробластная анемия диагностируется преимущественно у лиц среднего и пожилого возраста.
Причины
Врожденная сидеробластная анемия
Врожденные СБА связаны с мутациями в генетическом материале. Они различаются по типу наследования и патогенетическому механизму:
Приобретенная сидеробластная анемия
Идиопатические (первичные) СБА ‒ рефрактерные анемии с кольцевыми сидеробластами ‒ рассматриваются как разновидность миелодиспластического синдрома (МДС) и занимают в его структуре 5-15%. Чаще возникают как следствие лучевой или цитостатической терапии, проводимой по поводу коллагенозов, гемобластозов, различных онкопроцессов. Риск развития МДС повышен у курильщиков, лиц, контактирующих с химическими веществами (бензином, растворителями, инсектицидами).
Вторичная сидеробластная анемия может быть этиологически связана со следующими факторами:
Патогенез
Независимо от многообразия причин все они тем или иным путем приводят к нарушению образования гема. Гем является соединением, состоящим из протопорфирина и атома железа (Fe2+). При его связывании с белком глобином образуется гемсодержащий хромопротеин гемоглобин, главная функция которого заключается в транспорте кислорода к тканям, а углекислоты из тканей.
При СБА в результате дефектов ферментных систем, дефицита пиридоксальфосфата, токсического влияния или других факторов нарушается биосинтез протопорфирина, что делает образование гема невозможным, несмотря на достаточный уровень Fe в сыворотке крови. Развивается гипохромная анемия. В условиях, когда железо не используется клетками, оно начинает накапливаться в тканях и внутренних органах с развитием их дисфункции.
Классификация
Сидеробластные анемии делятся на 2 большие группы – наследственные и приобретенные, внутри которых выделяют конкретные клинические формы, связанные с определенными этиофакторами:
1. Наследственные сидеробластные анемии:
2. Приобретенные сидеробластные анемии:
Симптомы сидеробластной анемии
В клинической картине сидероахрестических анемий преобладают две группы симптомов: циркуляторно-гипоксические и недостаточность органов, обусловленная гемосидерозом. Гематологические изменения выявляются при диагностическом исследовании крови и костного мозга.
Гипоксический синдром сопровождается недомоганием и слабостью, тахикардией, снижением АД. Характерны жалобы на головокружение, ноющие боли в сердце, появление «мушек» перед глазами, одышку при движениях. Отмечается сухость и бледность кожи, ломкость ногтей. У детей ухудшается запоминание учебного материала, снижается успеваемость.
Депонирование железа приводит к развитию гепатоспленомегалии, а в поздних стадиях – циррозу печени. Поражение поджелудочной железы сопровождается манифестацией сахарного диабета. Гемосидероз миокарда проявляется кардиомегалией, нарушением ритма, сердечной недостаточностью. Отложение железа в тканях мужских половых желез вызывает вторичный гипогонадизм. При поражении легких возникает дыхательная недостаточность, почек – ХПН.
Осложнения
Перегрузка железом вызывает необратимые органные поражения, приводящие к стойкой функциональной недостаточности сердца, печени, почек, эндокринных органов. Таким пациентам требуется пожизненная заместительная и поддерживающая терапия, у них снижена общая продолжительность жизни. Течение идиопатической формы сидеробластной анемии у 5-10% пациентов осложняется острым лейкозом, рефрактерным к полихимиотерапии.
Диагностика
Основанием для выставления диагноза «сидеробластная анемия» служат клинические и лабораторные данные. Больных консультирует врач-гематолог, при необходимости – генетик, токсиколог, ревматолог, нарколог. Опорными диагностическими критериями выступают:
Лечение сидеробластной анемии
При токсических и лекарственных формах СБА в первую очередь устраняют провоцирующий фактор (отменяют ЛС, проводят дезинтоксикационную терапию и т.д.). Лекарственная терапия сидеробластной анемии включает назначение следующих препаратов:
При выраженном анемическом синдроме возникает необходимость в гемотрансфузиях. В случае значительного увеличения селезенки производится спленэктомия. В литературе имеются отдельные сообщения об эффективности аллогенной трансплантации гемопоэтических стволовых клеток (ТГСК) для терапии наследственной пиридоксин-резистентной сидеробластной анемии.
Прогноз и профилактика
Прогноз при сидеробластной анемии обусловлен ее этиологией. Лучше поддаются коррекции пиридоксин-зависимые и некоторые приобретенные формы (лекарственные, алиментарные). Существенно снижена продолжительность жизни у лиц с СБА, трансфузионно-зависимыми, рефрактерными к лечению, ассоциированными с лейкемией, синдромом Пирсона. Профилактика, прежде всего, касается вторичных сидеробластных анемий: следует полноценно питаться, принимать витаминные комплексы, не допускать интоксикаций (этанолом, свинцом) и контакта с вредными веществами. Для исключения наследственных СБА рекомендуется генетическое консультирование.
Сидеробластные анемии
, MD, PhD, Johns Hopkins University School of Medicine
Сидеробластные анемии могут быть
Врожденная сидеробластная анемия является следствием одной из многочисленных Х-сцепленных или аутосомных мутаций и обычно представляет собой микроцитарную гипохромную анемию.
Сидеробластные анемии это анемии при нарушенной утилизации железа, которые характеризуются недостаточной утилизацией железа в костном мозге со снижением синтеза гема, несмотря на наличие достаточного или повышенного количества железа. Сидеробластные анемии иногда характеризуются наличием полихроматофилии (свидетельствующей об увеличении количества ретикулоцитов) и эритроцитов с базофильной зернистостью (сидероцитов) содержащих железосодержащие гранулы (тельца Паппенгеймера)
Как при приобретенных так и при врожденных сидеробластных анемиях, синтез гема нарушается из-за невозможности включения железа в состав протопорфирина IX, что приводит к образованию кольцевидных сидеробластов.
Приобретенная сидеробластная анемия
Чаще всего приобретенные сидеробластные анемии являются частью
Происходят соматические мутации генов, участвующих в сплайсинге РНК, чаще всего SF3B1. Приобретенная сидеробластная анемия возникает в зрелом возрасте.
Менее распространенные причины включают:
Лекарственные средства (например, хлорамфеникол, циклосерин, изониазид, линезолид, пиразинамид)
Токсины (в том числе этанол и свинец)
Дефицит витамина B6 (пиридоксина) или меди (возможно, вызванный приёмом цинка, который препятствует всасыванию меди в желудочно-кишечном тракте)
При этом наблюдается снижение продукции ретикулоцитов, гибель эритроцитов в костном мозге, эритроидная гиперплазия (или дисплазия) костного мозга. Хотя эритроциты являются гипохромными, некоторые эритроциты могут быть крупными и иметь нормоцитарные или макроцитарные показатели; в таком случае вариабельность размеров эритроцитов (диморфизм) обычно приводит к повышению показателя распределения эритроцитов по объему (RDW).
Врожденная сидеробластная анемия
Многочисленные другие сцепленные с Х-хромосомой, аутосомные и митохондриальные формы были отождествлены с мутациями в генах, участвующих в синтезе гема или других митохондриальных ферментативных путей (1 Справочные материалы Сидеробластные анемии представляют собой разнородную группу анемий, которые характеризуются увеличением сывороточного железа, ферритина и насыщения трансферрина, а также наличием кольцевидных. Прочитайте дополнительные сведения 
Эритроциты, как правило, микроцитарные и гипохромные, но это не всегда так.
Справочные материалы
1. Ducamp S, Fleming MD: The molecular genetics of sideroblastic anemia. Blood 133:59–69, 2019. doi: 10.1182/blood-2018-08-815951
Диагностика сидеробластных анемий
Complete blood count (CBC), reticulocyte count, and peripheral blood smear
Исследование содержания железа (сывороточное железо, сывороточный ферритин и насыщение трансферрина)
Исследование образца костного мозга
Генетическое тестирование подозреваемой наследственной или приобретенной мутации
Сидеробластную анемию необходимо предполагать у пациентов с микроцитарной анемией или повышением показателя RDW, особенно в сочетании с повышением уровня сывороточного железа, сатурации ферритина и трансферрина (см. Железодефицитная анемия Железодефицитная aнемия Дефицит железа является наиболее частой причиной анемии и обычно обусловлен кровопотерей; мальабсорбция, такая, к примеру, как при целиакии, является гораздо менее распространенной причиной. Прочитайте дополнительные сведения 
В мазке периферической крови Мазок периферической крови Анемия возникает при снижении числа эритроцитов (эритроциты измеряются количеством, гематокритом или содержанием гемоглобина в эритроцитах). У мужчин анемия определяется как уровень гемоглобина Прочитайте дополнительные сведения 
Если причина сидеробластной анемии остается неустановленной, сыворотка крови исследуется на содержание свинца.
Лечение сидеробластных анемий
Устранение провоцирующих факторов (при приобретенной форме)
Витаминные или минеральные добавки
Рекомбинантный эритропоэтин (ЭПО)
Элиминация токсина или лекарственного средства (особенно потребления этилового спирта или цинка) или добавление минеральных/витаминных препаратов (медь или пиридоксин) может привести к выздоровлению.
В случаях врожденной патологии пероральное применение пиридоксина в дозе 50 мг 3 раза в день может иметь лечебный эффект, хотя обычно неполный.
Приобретенные случаи часто отвечают на терапию рекомбинантным ЭПО.
Ключевые моменты сидеробластных анемий
Сидеробластная анемия может быть приобретенной или врожденной.
Наличие кольцевых сидеробластов в биоптате костного мозга является патогномоническим признаком.
Анемия обычно является микроцитарной при врожденной сидеробластной анемии и макроцитарной при приобретенной сидеробластной анемии.
Уровни сывороточного железа, ферритина и трансферрина обычно повышены.
Проводят лечение основного заболевания и рассматривают необходимость назначения пиридоксина в случаях врожденной анемии или рекомбинантного эритропоэтина в случаях приобретенной анемии.
Сидеробластная анемия что это такое простыми словами
Наследственные сидеробластные анемии — разнородная по спектру генетических нарушений и выраженности клинических проявлений группа заболеваний.
Варианты наследования и патогенез
Наследственные сидеробластные анемии, сцепленные с Х-хромосомой. У большинства детей с сидеробластной анемией механизм наследования связан с Х-хромосомой. В связи с этим анемия диагностируется преимущественно у мальчиков и их близких родственников мужского пола по материнской линии (родные дяди и двоюродные братья). Редко имеется другой вариант наследования, не связанный с Х-хромосомой. В некоторых семьях заболевание возникает только у девочек, так как у мальчиков-гомозигот патология не совместима с жизнью.
В основе патогенеза лежит дефект синтеза 5-аминолевулинатсинтетазы (АЛК), участвующей в синтезе гема. Для нормальной работы этого фермента необходимо достаточное количество пиридоксина — витамина В6 (этим и объясняется эффективность лечения витамином В6). Активность фермента 5-аминолевулинатсинтетазы (АЛК-синтетазы) кодирует ген ALAS2, расположенный на Х-хромосоме. У больных сидеробластной анемией описано несколько различных мутаций данного гена.
Наследственные сидеробластные анемии с аутосомным типом наследования. Этот тип наследования встречается значительно реже, чем сцепленный с Х-хромосомой. Известны случаи как аутосомно-доминантного, так и аутосомно-рецессивного наследования. Мутации гена ALAS2 не определяются, поэтому терапевтический эффект пиридоксина отсутствует.
Спорадическая врожденная сидеробластная анемия. В мире описано около 20 случаев сидеробластной анемии, выявленной сразу после рождения, без признаков заболевания у других членов семьи. Вероятно, при этом имелись либо аутосомно-рецессивный тип наследования, либо появление новых мутаций гена ALAS2 в родительских половых клетках.
Митохондриальная цитопатия (синдром Пирсона). Синдром Пирсона — врожденное заболевание, которое обусловлено делециями или другими генетическими перестройками митохондриальной ДНК и клинически проявляется множественными органными поражениями. Одним из ранних признаков заболевания является тяжелая анемия, ассоциированная с наличием кольцевых сидеробластов в костном мозге. Продолжительность жизни детей с синдромом Пирсона обычно не превышает 2-3 года.
Синдром DIOMOAD. В основе большинства клинических проявлений заболевания, наследующегося по аутосомно-рецессивному типу, лежат дегенеративные процессы в нервной ткани, обусловленные, вероятно, наследственными дефектами метаболизма тиамина. Гематологическим проявлением синдрома является нормоцитарная сидеробластная анемия средней степени тяжести в сочетании с нейтропенией и выраженной тромбоцитопенией. Отмечен терапевтический эффект применения тиамина.
Классификация сидеробластных анемий
Данные клинических и лабораторных исследований при наследственных сидеробластных анемий
В большинстве случаев клиническая картина сидеробластной анемии, сцепленной с Х-хромосомой, не отличается от таковой при анемии с аутосомным типом наследования или других врожденных форм. Тяжелая анемия, как правило, диагностируется в младенчестве или раннем детстве. При менее выраженных проявлениях анемического синдрома или бессимптомном течении заболевание выявляется обычно у взрослых или даже пожилых больных.
Наряду с анемическим синдромом у всех больных определяются признаки избытка железа в организме, которые получили специальное название: синдром эритропоэтигеского гемохроматоза. Проявления этого синдрома достаточно разнообразны. Чаще всего определяются умеренная гепатомегалия и спленомегалия. Функция печени в большинстве случаев нарушена незначительно или не страдает вообще. При биопсии печеночной ткани определяются депозиты железа в гепатоцитах. У некоторых больных старше 30-40 лет при гистологическом исследовании находят признаки микронодулярного цирроза печени, протекающего, как правило, доброкачественно.
На фоне гемохроматоза поджелудочной железы могут определяться сахарный диабет или нарушения толерантности к глюкозе. Редко при объективном обследовании выявляется пигментация кожных покровов. Наиболее опасными проявлениями синдрома эритро-поэтического гемохроматоза являются тяжелые нарушения сердечного ритма и сердечная недостаточность, которые развиваются, как правило, на поздних этапах заболевания. В тяжелых случаях у детей может наблюдаться задержка роста и развития.
В анализе крови определяется анемия различной степени тяжести. При тяжелой анемии обычно имеются гипохромия, микроцитоз, анизо- и пойкилоцитоз, реже мишеневидные клетки и единичные сидероциты. При менее тяжелых формах анемии в мазке могут выявляться две популяции клеток: гипохромные микроциты и нормальные эритроциты. На гистограмме эритроцитов при этом образуется двухфазная кривая, отражающая различия в размерах эритроцитов. Уровень лейкоцитов и тромбоцитов обычно в норме, но при развитии гиперспленизма может снижаться. Количество ретикулоцитов в большинстве случаев в норме или незначительно повышено.
В миелограмме выявляется гиперплазия эритроидного ростка на фоне нормобластического типа кроветворения и повышенное количество сидеробластов. В редких случаях (при сопутствующем дефиците фолиевой кислоты) может определяться мегалобластический тип кроветворения.
При биохимическом исследовании обычно выявляется незначительная гипербилирубинемия, повышение уровня ферритина и снижение уровня трансферрина, и увеличение его сатурации. При анемии, сцепленной с Х-хромосомой, имеется снижение активности АЛК-синтетазы.
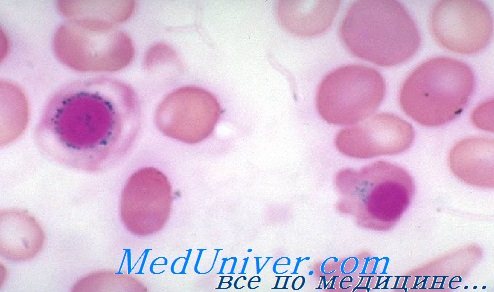
У больных с синдромом Пирсона диагностируется рефрактерная сидеробластная анемия, которая сочетается с признаками экзокринной недостаточности поджелудочной железы, эпизодами молочнокислого ацидоза и прогрессирующей почечной и печеночной недостаточностью. Анемия выявляется, как правило, после рождения и носит нормоцитарныи или макроцитарный характер. Уровень ретикулоцитов чаще всего снижен. В большинстве случаев имеются нейтропения и тромбоцитопения различной степени тяжести. При электрофорезе гемоглобина обычно определяется повышение уровня Hb F. Костный мозг гиперклеточный или нормоклеточный, выявляются кольцевые сидеробласты.
Лечение и прогноз наследственных сидеробластных анемий
Всем больным наследственными сидеробластными анемиями необходимо начинать терапию пиридоксином (витамин В6), которая эффективна в среднем в 1/3 случаев. Доза витамина В6 обычно составляет 50-100 мг в сутки. Выраженность терапевтического эффекта у пациентов, ответивших на лечение, различна. В большинстве случаев появляется ретикулоцитоз и уровень гемоглобина в течение 1-2 месяцев лечения постепенно повышается до нормы или субнормальных значений. Морфологические изменения эритроцитов при этом сохраняются.
При отсутствии оптимального эффекта на фоне терапии пиридоксином уровень гемоглобина стабилизируется, но не достигает нормальных значений. Необходимо проведение поддерживающей терапии витамином В6, при отсутствие которой концентрация гемоглобина через несколько месяцев снижается до исходных величин. При выявлении мегалобластического типа кроветворения показано лечение фолиевой кислотой. Пациентам с тяжелой анемией, у которых отсутствует эффект витамина В6, по показаниям проводятся периодические трансфузии эритроцитарной массы. Это уменьшает выраженность анемии и предотвращает задержку роста и развития у детей.
Для профилактики гемосидероза показана терапия дефероксамином, в которой нуждаются прежде всего больные с тяжелой анемией, получающие гемотрансфузионную терапию. Предпочтительно проведение 12-часовых подкожных инфузий препарата в дозе 40 мг/(кг-день) каждые 5 дней недели (этот режим обладает минимальной токсичностью). Спленэктомия при наследственных формах сидеробластной анемии довольно часто осложняется тромбоэмболией, в ряде случаев с летальным исходом, поэтому оперативное лечение используется редко.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021