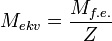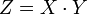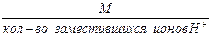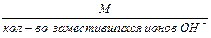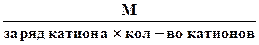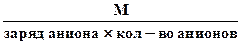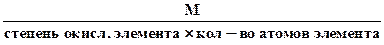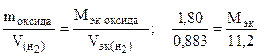Эквивалентная масса что это
ЭКВИВАЛЕНТНАЯ МАССА
Полезное
Смотреть что такое «ЭКВИВАЛЕНТНАЯ МАССА» в других словарях:
эквивалентная масса — 4.1.3 эквивалентная масса: Масса условного ударника, вычисленная путем деления на ускорение свободного падения измеренного значения силы (в ньютонах), направленной вдоль вертикально расположенной оси ударника и необходимой для удержания плеча… … Словарь-справочник терминов нормативно-технической документации
эквивалентная масса — lygiavertė masė statusas T sritis Standartizacija ir metrologija apibrėžtis Daugiadalelės sistemos arba iš kelių dalių sudaryto kūno masė, apskaičiuota pagal tam tikras taisykles arba formules. atitikmenys: angl. equivalent mass vok. äquivalente… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
эквивалентная масса — ekvivalentinė masė statusas T sritis fizika atitikmenys: angl. equivalent mass vok. äquivalente Masse, f rus. эквивалентная масса, f pranc. masse équivalente, f … Fizikos terminų žodynas
ЭКВИВАЛЕНТНАЯ ПЛОТНОСТЬ — масса глаза на единицу площади зрения, спроецированной на оптическую поверхность … Словарь понятий и терминов, сформулированных в нормативных документах российского законодательства
приведенная масса — lygiavertė masė statusas T sritis Standartizacija ir metrologija apibrėžtis Daugiadalelės sistemos arba iš kelių dalių sudaryto kūno masė, apskaičiuota pagal tam tikras taisykles arba formules. atitikmenys: angl. equivalent mass vok. äquivalente… … Penkiakalbis aiškinamasis metrologijos terminų žodynas
Приведённая масса — условная характеристика распределения масс в движущейся механической или смешанной (например, электро механической) системе, зависящая от физических параметров системы (масс, моментов инерции, индуктивности и др.) и от её закона движения[1].… … Википедия
Эквивалент вещества — Эквивалент вещества или Эквивалент это реальная или условная частица, которая может присоединять, высвобождать или другим способом быть эквивалентна катиону водорода в ионообменных реакциях или электрону в окислительно восстановительных… … Википедия
ГОСТ Р 52762-2007: Методы испытаний на стойкость к механическим внешним воздействующим факторам машин, приборов и других технических изделий. Испытания на воздействие ударов по оболочке изделий — Терминология ГОСТ Р 52762 2007: Методы испытаний на стойкость к механическим внешним воздействующим факторам машин, приборов и других технических изделий. Испытания на воздействие ударов по оболочке изделий оригинал документа: 4.1.2 высота… … Словарь-справочник терминов нормативно-технической документации
Фактор эквивалентности — Эквивалент реальная или мнимая частица вещества, которая может присоединять, высвобождать или быть каким либо иным образом эквивалентна (то есть равноценна) одному иону H+ в обменных реакциях или одному электрону в окислительно восстановительных … Википедия
Эквивалент (химия) — Эквивалент реальная или мнимая частица вещества, которая может присоединять, высвобождать или быть каким либо иным образом эквивалентна (то есть равноценна) одному иону H+ в обменных реакциях или одному электрону в окислительно… … Википедия
зМБЧБ 1. пУОПЧОЩЕ ЪБЛПОЩ ИЙНЙЙ

1.1 уФЕИЙПНЕФТЙЮЕУЛЙЕ ЪБЛПОЩ
оБЙВПМЕЕ ЧБЦОПЕ РТБЛФЙЮЕУЛПЕ ЪОБЮЕОЙЕ ЙНЕАФ УМЕДХАЭЙЕ ЪБЛПОЩ ИЙНЙЙ: УФЕИЙПНЕФТЙЮЕУЛЙЕ Й ЗБЪПЧЩЕ.
лБЦДЩК ИЙНЙЮЕУЛЙК ЬМЕНЕОФ ПФМЙЮБЕФУС ПФ ДТХЗЙИ ОЕ ФПМШЛП ИЙНЙЮЕУЛЙН УЙНЧПМПН (ЛБЮЕУФЧЕООБС ИБТБЛФЕТЙУФЙЛБ), ОП ОЕЛПФПТЩНЙ ЛПМЙЮЕУФЧЕООЩНЙ РБТБНЕФТБНЙ. л ОЙН ПФОПУСФУС, РТЕЦДЕ ЧУЕЗП, БФПНОБС НБУУБ ЬМЕНЕОФБ Й ЪБТСД ЕЗП СДТБ (ЙМЙ РПТСДЛПЧЩК ОПНЕТ ЬМЕНЕОФБ). ьФЙ ИБТБЛФЕТЙУФЙЛЙ ДМС ЛБЦДПЗП БФПНБ ЬМЕНЕОФБ РТЙЧЕДЕОБ Ч рЕТЙПДЙЮЕУЛПК УЙУФЕНЕ ЬМЕНЕОФПЧ д. й. нЕОДЕМЕЕЧБ. пДОБЛП УМЕДХЕФ ПФНЕФЙФШ, ЮФП РТЙЧЕДЕООЩЕ НБУУЩ БФПНПЧ СЧМСАФУС ПФОПУЙФЕМШОЩНЙ ЧЕМЙЮЙОБНЙ (ФБЛ ОБЪЩЧБЕНЩНЙ, БФПНОЩНЙ ЕДЙОЙГБНЙ НБУУЩ ЙМЙ Б.Е.Н.). нПМЕЛХМСТОБС НБУУБИЙНЙЮЕУЛПЗП УПЕДЙОЕОЙС ФБЛЦЕ МЕЗЛП ПРТЕДЕМЙНБ, ФБЛ ЛБЛ ПОБ ТБЧОБ УХННЕ БФПНОЩИ НБУУ УПУФБЧМСАЭЙИ ДБООХА НПМЕЛХМХ БФПНПЧ.
фБЛЙН ПВТБЪПН, МАВПЕ ИЙНЙЮЕУЛПЕ УПЕДЙОЕОЙЕ ИБТБЛФЕТЙЪХЕФУС НБУУПК ПДОПЗП НПМС ЙМЙ НПМШОПК (НПМСТОПК) НБУУПК н, ЧЩТБЦБЕНПК Ч З/НПМШ. ъОБЮЙФ, н(H2O) = 18 З/НПМШ, Б н(H2SO4) = 98 З/НПМШ.
уЧСЪШ НЕЦДХ ЛПМЙЮЕУФЧПН n (Ч НПМСИ) Й НБУУПК m (Ч ЗТБННБИ) ЧЕЭЕУФЧБ ЧЩТБЦБЕФУС ЖПТНХМПК:
чПЪОЙЛБЕФ ЪБЛПОПНЕТОЩК ЧПРТПУ П ОЕПВИПДЙНПУФЙ ЧЧЕДЕОЙС ФЕТНЙОБ «НПМШОБС НБУУБ ЧЕЭЕУФЧБ» Й ЕЗП РТЙНЕОЕОЙС, ЧЕДШ ДМС ЙЪНЕТЕОЙС НБУУЩ ЧЕЭЕУФЧБ ХЦЕ ЙНЕАФУС ЧЕМЙЮЙОЩ, ЧИПДСЭЙЕ Ч УЙУФЕНХ уй: ЛЙМПЗТБНН, ЗТБНН, ФПООБ Й Ф.Д. чПРТПУ ПФРБДБЕФ, ЕУМЙ ТБУУНПФТЕФШ РТЙНЕОЕОЙЕ ДБООЩИ ЧЕМЙЮЙО РТЙ БОБМЙЪЕ ИЙНЙЮЕУЛЙИ ХТБЧОЕОЙК.
ч ПВЭЕН УМХЮБЕ ХТБЧОЕОЙЕ ИЙНЙЮЕУЛПК ТЕБЛГЙЙ ЪБРЙУЩЧБАФ Ч ЧЙДЕ

ч ЛБЮЕУФЧЕ РТЙНЕТБ ТБУУНПФТЙН РТПУФПЕ ИЙНЙЮЕУЛПЕ ЧЪБЙНПДЕКУФЧЙЕ:
дБООБС ЪБРЙУШ РПЛБЪЩЧБЕФ, ЮФП РТЙ ЧЪБЙНПДЕКУФЧЙЙ ДЧХИ НПМЕЛХМ ЗБЪППВТБЪОПЗП ЧПДПТПДБ о 2 Й ПДОПК НПМЕЛХМЩ ЗБЪППВТБЪОПЗП ЛЙУМПТПДБ п2 ПВТБЪХЕФУС ДЧЕ НПМЕЛХМЩ ЧПДЩ.
йЪ ДБООПЗП РТЙНЕТБ ЧЙДОП, ЮФП ЛПМЙЮЕУФЧП НПМШ ТЕБЗЙТХАЭЙИ Й ПВТБЪХАЭЙИУС Ч ТЕЪХМШФБФЕ ИЙНЙЮЕУЛПК ТЕБЛГЙЙ ЧЕЭЕУФЧ РТСНПРТПРПТГЙПОБМШОП ЛПЬЖЖЙГЙЕОФБН Ч ХТБЧОЕОЙЙ ИЙНЙЮЕУЛПК ТЕБЛГЙЙ.
ьФП РПЪЧПМСЕФ РТПЧПДЙФШ ЛПМЙЮЕУФЧЕООЩЕ ТБУЮЕФЩ, ЙУРПМШЪХС ХТБЧОЕОЙС ЪБДБООЩИ ИЙНЙЮЕУЛЙИ ТЕБЛГЙК.
рТЙНЕТ: ПРТЕДЕМЙФШ НБУУХПВТБЪХАЭЕКУС ЧПДЩ РТЙ УЦЙЗБОЙЙ 16 ЗТБННПЧ ЧПДПТПДБ Ч ЙЪВЩФЛЕ ЛЙУМПТПДБ.
йУРПМШЪХЕН ХЦЕ ЪОБЛПНПЕ ОБН ХТБЧОЕОЙЕ ТЕБЛГЙЙ Й ТБУУФБЧЙН Ч ОЕН ФТЕВХЕНЩЕ ЧЕМЙЮЙОЩ.
РТЙ УЗПТБОЙЙ 4 ЗТБННПЧ о2 ПВТБЪПЧБМПУШ 36 ЗТБННПЧ о2п
РТЙ УЗПТБОЙЙ 16 ЗТБННПЧ о2 ПВТБЪПЧБМПУШ и ЗТБННПЧ о2п
1.1.2 ьЛЧЙЧБМЕОФОБС НБУУБ (НПМСТОБС НБУУБ ЬЛЧЙЧБМЕОФБ ЧЕЭЕУФЧБ)
mЬЛЧ(ПЛУЙДБ) = нПЛУЙДБ/(ЮЙУМП БФПНПЧ ЛЙУМПТПДБ·2);
mЬЛЧ(ПУОПЧБОЙС) = нПУОПЧБОЙС/ЛЙУМПФОПУФШ ПУОПЧБОЙС;
mЬЛЧ(ЛЙУМПФЩ) = нЛЙУМПФЩ/ПУОПЧОПУФШ ЛЙУМПФЩ;
mЬЛЧ(УПМЙ) = нУПМЙ/(ЮЙУМП БФПНПЧ НЕФБММБ·ЧБМЕОФОПУФШ НЕФБММБ).
нПЦОП ПФНЕФЙФШ, ЮФП Ч ВПМШЫЙОУФЧЕ УМХЮБЕЧ ЛЙУМПФОПУФШ ПУОПЧБОЙС ТБЧОБ ЮЙУМХ ЗЙДТПЛУЙМШОЩИ ЗТХРР Ч ЖПТНХМЕ ПУОПЧБОЙС, Б ПУОПЧОПУФШ ЛЙУМПФЩ ТБЧОБ ЮЙУМХ БФПНПЧ ЧПДПТПДБ Ч ЖПТНХМЕ ЛЙУМПФЩ.
ьЛЧЙЧБМЕОФОЩЕ НБУУЩ ЧЕЭЕУФЧ ЙУРПМШЪХАФ ДМС ЛПМЙЮЕУФЧЕООЩИ ТБУЮЕФПЧ РТЙ ИЙНЙЮЕУЛЙИ ЧЪБЙНПДЕКУФЧЙСИ НЕЦДХ ЧЕЭЕУФЧБНЙ. пЗТПНОЩН РТЕЙНХЭЕУФЧПН РТЙ ЬФПН СЧМСЕФУС ФП, ЮФП ДМС ЬФПЗП ОЕ ОХЦОП ЙУРПМШЪПЧБФШ ХТБЧОЕОЙЕ ИЙНЙЮЕУЛПК ТЕБЛГЙЙ (ЛПФПТПЕ ЧП НОПЗЙИ УМХЮБСИ ОБРЙУБФШ ЪБФТХДОЙФЕМШОП), ОХЦОП ФПМШЛП ЪОБФШ, ЮФП ДБООЩЕ ИЙНЙЮЕУЛЙЕ ЧЕЭЕУФЧБ ЧЪБЙНПДЕКУФЧХАФ НЕЦДХ УПВПК ЙМЙ ЧЕЭЕУФЧП СЧМСЕФУС РТПДХЛФПН ИЙНЙЮЕУЛПК ТЕБЛГЙЙ.
дМС ЛПМЙЮЕУФЧЕООЩИ ТБУЮЕФПЧ ЙУРПМШЪХЕФУС ЪБЛПО ЬЛЧЙЧБМЕОФПЧ: НБУУЩ ТЕБЗЙТХАЭЙИ Й ПВТБЪХАЭЙИУС ЧЕЭЕУФЧ ПФОПУСФУС ДТХЗ Л ДТХЗХ, ЛБЛ ЙИ ЬЛЧЙЧБМЕОФОЩЕ НБУУЩ.
нБФЕНБФЙЮЕУЛПЕ ЧЩТБЦЕОЙЕ ЪБЛПОБ ЬЛЧЙЧБМЕОФПЧ ЙНЕЕФ УМЕДХАЭЙК ЧЙД:
| m1/m2 = mЬЛЧ(1)/mЬЛЧ(2) | (1.2) |
рТЙНЕТ: ПРТЕДЕМЙФШ НБУУХ УПДЩ (ЛБТВПОБФБ ОБФТЙС) Na2CO3, ОЕПВИПДЙНХА ДМС РПМОПК ОЕКФТБМЙЪБГЙЙ 1,96 ЛЗ УЕТОПК ЛЙУМПФЩ H2SO4.
чПУРПМШЪХЕНУС ЪБЛПОПН ЬЛЧЙЧБМЕОФПЧ
пРТЕДЕМСЕН ЬЛЧЙЧБМЕОФОЩЕ НБУУЩ ЧЕЭЕУФЧ, ЙУИПДС ЙЪ ЙИ ИЙНЙЮЕУЛЙИ ЖПТНХМ:
Эквивалент (химия)
Эквивалент (химия)
Эквивалент — реальная или мнимая частица вещества, которая может присоединять, высвобождать или быть каким-либо иным образом эквивалентна (то есть равноценна) одному иону H + в обменных реакциях или одному электрону в окислительно-восстановительных реакциях.
Например, в реакции:
NaOH + HCl = NaCl + H2O
эквивалентом будет реальная частица — ион Na+, в реакции
эквивалентом будет являться мнимая частица ½Zn(OH)2.
Содержание
Фактор эквивалентности
Эквивалентом является частица ½Zn(OH)2. Число ½ получило название фактора эквивалентности и может обозначаться, как «fэкв«. или «z».
Фактор эквивалентности помогает сформулировать закон эквивалентности.
Эквивалентная масса
Эквивалентная масса — это масса одного эквивалента данного вещества.
Молярная масса эквивалента вещества — масса одного моля эквивалентов, равная произведению фактора эквивалентности на молярную массу этого вещества.
Эквивалент — условная частица вещества, в целое число раз Z меньшее формульной единицы (Z — число эквивалентов; показывает, во сколько раз эквивалент меньше формульной единицы).
| вещество | реакция | |||
|---|---|---|---|---|
| простое ˆ | сложное | ОВР (Окислительно-восстановительная реакция) | обменная | |
| X | число атомов в формульной единице | число катионов (анионов) | число атомов элемента, поменявших степень окисления | число замещенных частиц в формульной единице |
| Y | характерная валентность элемента | фиктивный заряд на катионе (анионе) | число принятых (отданных) элементом электронов | фиктивный заряд на частице |
ˆ — для инертных газов Z = 1
Закон эквивалентов
В результате работ И. В. Рихтера (1792—1800) был открыт закон эквивалентов: все вещества реагируют в эквивалентных отношениях. Эквивалентом называют реальную или условную частицу вещества, которая может замещать, присоединять, высвобождать или быть каким-либо другим способом эквивалентна одному иону водорода в кисло-основных или ионообменных реакциях или одному электрону в окислительно-восстановительных реакциях.
Ссылки
Полезное
Смотреть что такое «Эквивалент (химия)» в других словарях:
Эквивалент(химия) — Эквивалент вещества его масса (выраженная в углеродных единицах), которая присоединяет или замещает атомную массу водорода (1,008 г) или половину атомной массы кислорода (15,9994/2 г.) Эквивалент кислоты равен ее молярной массе, деленной на… … Википедия
Эквивалент — – равнозначащий, равносильный продукт. Эквивалентность особенно важна при сравнении товаров и их обмене друг на друга. С этой целью применяются товарные эквиваленты, то есть товары, равноценные другим,… … Энциклопедия терминов, определений и пояснений строительных материалов
ЭКВИВАЛЕНТ ХИМИЧЕСКИЙ — условная частица, в целое число раз меньшая (или равная) соответствующей ей формульной единицы атома, молекулы, иона, радикала и др. В одной формульной единице в ва В может содержаться z(B) Э. х. этого в ва. Число z(B) (эквивалентное число)… … Химическая энциклопедия
ХИМИЯ. РАСТВОРЫ И РАСТВОРИМОСТЬ — Благодаря неравномерному распределению электрического заряда в молекулах, т.е. наличию у них отрицательных и положительных полюсов (если говорить более строго дипольного момента), даже нейтральные в целом молекулы притягиваются друг к другу. Сила … Энциклопедия Кольера
Электрохимический эквивалент — масса вещества, которое должно выделиться на электроде, согласно закону Фарадея, при прохождении через электролит единицы количества электричества: где постоянная Фарадея … Википедия
химический эквивалент — – реальная или условная частица вещества x, которая эквивалентна одному иону водорода в данной кислотно основной реакции или одному электрону в данной окислительно восстановительной реакции. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
Углеродный эквивалент — – условная величина содержания углерода, получаемая из набора основных химических элементов арматурной стали. [Терминологический словарь по бетону и железобетону. ФГУП «НИЦ «Строительство» НИИЖБ им. А. А. Гвоздева, Москва, 2007 г. 110 стр.] … Энциклопедия терминов, определений и пояснений строительных материалов
Периодическая законность химических элементов — После открытий Лавуазье (см.) понятие о химических элементах и простых телах так укрепилось, что их изучение положено в основу всех химических представлений, а вследствие того взошло и во все естествознание. Пришлось признать, что все вещества,… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
ЭКВИВАЛЕНТНАЯ МАССА — (химический эквивалент). Эквивалентная масса элемента это масса 1 эквивалента элемента; эквивалентом элемента называют такое его количество, которое реагирует с 1 моль атомов водорода или замещает то же количество атомов водорода в химических… … Энциклопедия Кольера
Эквиваленты и эквивалентные массы



Количественный подход к изучению химических явлений и установление закона постоянства состава показали, что вещества вступают во взаимодействие в определенных соотношениях масс, что привело к введению такого важного понятия, как «эквивалент», и установлению закона эквивалентов: массы взаимодействующих без остатка веществ соотносятся как их эквивалентные массы.
Математическое выражение закона эквивалентов:
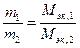
Из этого определения видно, что понятие «эквивалент» относится к конкретной химической реакции; если его относят к атому в химическом соединении, то имеют в виду реакцию образования этого соединения из соответствующего простого вещества и называют эквивалентом элемента в соединении.
Относительная масса эквивалента называется эквивалентной массой, а масса одного моля эквивалентов, выраженная в граммах, называется молярной эквивалентной массой; она обозначается Мэк, единица измерения – моль эк/г, она численно равна относительной молекулярной массе эквивалента.
Пример 5. Определить эквивалент, эквивалентную массу и молярную массу эквивалента кислорода в молекуле воды.
Решение. Такая формулировка вопроса предполагает реакцию образования воды из кислорода и водорода H2 + ½O2 = Н2О, в которой с 1 атомом водорода соединяется ½ атомов кислорода. Следовательно, Z(О) = 2. Атомная масса кислорода равна 16. Эквивалентом кислорода является ½ его атома, эквивалентная масса равна 8, а молярная масса эквивалента равна 8 г/ моль.
Эквивалентное число серы в этих оксидах равно 4 и 6, т.е. оно равно степени окисления (стехиометрической валентности) серы в этих соединениях. Таким образом, относительная эквивалентная масса и численно равная ей молярная масса элемента в соединении вычисляется по формуле:
Мэк (элемента) = 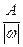
Например, Z(Mn) в соединении KMnO4 составляет 7(w = +7), а Мэк (Mn)=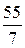
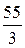
Эквивалентная масса вещества имеет различные значения в зависимости от того, в какой химической реакции участвует это вещество. При расчете эквивалентных масс можно пользоваться следующими правилами и формулами.
1. Эквивалентная масса кислоты в реакциях замещения ионов водорода равна:
Мэк кислоты =
2. Эквивалентная масса основания в реакции замещения гидроксид-ионов равна:
Мэк основания =
Пример 6. Определить эквивалентную массу H2SO4 в реакциях:
Решение. В реакции 1 замещён один ион водорода, следовательно, эквивалентное число серной кислоты Z(H2SO4) = 1, Мэк(H2SO4) = 98 г/моль эк. В реакции 2 заместились оба иона водорода, следовательно, эквивалентное число Z(H2SO4) = 2, а Mэк(H2SO4) = 49 г/моль эк.
Пример 7. Определить эквивалентную массу гидроксида висмута в реакциях:
3. Эквивалентная масса соли в реакциях полного замещения катиона или аниона равна:
Мэк. соли =
или Мэк соли =
4. Эквивалентная масса оксида в реакциях полного замещения равна
Мэк оксида =
Например, Z(Fe2O3) = 3 × 2 = 6, Мэк = М(Fe2O3) = 160 : 6 = 26,6 г/моль эк. Но в реакции
Z(Fe2O3) = 4, Мэк(Fe2O3) = 160 : 4 = 40 г/моль эк, т.к. одна формульная единица Fe2O3 взаимодействует с четырьмя эквивалентами HCl.
При решении задач, связанных с газообразными веществами, целесообразно пользоваться значением эквивалентного объема. Это объем, занимаемый одним молем эквивалентов газообразного вещества. Для водорода при н.у. этот объем равен 11,2 л/моль эк (так как Мэк(Н) = 1 г/моль эк), а для кислорода – 5,6 л/моль эк (так как Мэк(О) = 8 г/моль эк).
Пример 8. На восстановление 1,80 г оксида металла израсходовано 883 мл водорода (н.у.). Вычислить эквивалентные массы оксида и металла.
Решение. Согласно закону эквивалентов, массы (объемы) реагирующих веществ пропорциональны их эквивалентным массам (объемам):
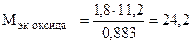
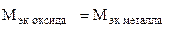
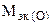
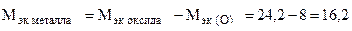
Пример 9. Вычислить эквивалентную массу цинка, если 1,168 г этого металла вытеснили из кислоты 438 мл Н2 (Т = 17 °С и Р = 750 мм рт. ст.).
Решение. 1) По уравнению Клапейрона–Менделеева вычисляем массу водорода:
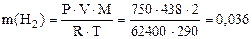
Согласно закону эквивалентов
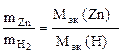
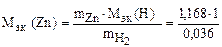
ЭКВИВАЛЕНТНАЯ МАССА
Методы определения.
Первые опыты по определению эквивалентных масс провели Дж.Дальтон, Й.Берцелиус, Ж.Дюма, Ж.Стас и другие ученые, но основная заслуга принадлежит здесь Т.Ричардсу, который впервые выполнил тщательные измерения эквивалентных масс с высочайшей точностью. Нагревая чистый перхлорат калия KClO3, превращали его в хлорид калия (KCl), при этом из 100 масс. ч. KClO3 образовывалось 60,835 масс. ч. KCl и 39,165 масс. ч. кислорода. Поскольку одна молекула KClO3 содержит на 3 атома кислорода, т.е. на 47,998 масс. ч., больше, чем KCl, то эквивалентная масса хлорида равна 47,998 Ч (60,835:39,165) = 74,555. Далее, известное количество чистого серебра превращали в нитрат серебра, который использовали для осаждения хлорида серебра из раствора при взаимодействии с чистым хлоридом калия. Было установлено, что для полного превращения 74,555 масс. ч., т.е. массового эквивалента хлорида калия KCl, в хлорид серебра, который содержит 35,453 масс. ч. хлора, требуется 107,87 масс. ч. серебра. Эквивалентная масса калия при этом равна 74,555 – 35,453 = 39,102. Аналогично, зная эквивалентную массу серебра и изучая реакции образования им соответствующих галогенидов, например бромида AgBr, можно рассчитать эквивалентную массу галогена (в частности, брома). С использованием эквивалентных масс хлора и брома были определены эквивалентные массы многих металлов. Для нахождения эквивалентной массы какого-либо металла (М) синтезируют его чистый хлорид или бромид MBrx и осаждают галоген в виде галогенида серебра. Зная массы использованного MBrx и полученного AgBr, эквивалентные массы серебра (107,87) и брома (79,999), несложно определить эквивалентную массу металла М, который соединяется с 79,999 масс. ч. брома.
Описанный метод используется для точных расчетов, а для приближенных оценок можно применять другие способы, основанные на измерении объема и расчете массы водорода, выделившегося при растворении металла в кислоте, на определении массы одного металла, вытесняемого известным количеством другого из раствора, на определении состава гидридов или оксидов непосредственно по реакции соединения или аналитическими методами. Эквивалентные массы позволяют не только устанавливать соотношения, в которых элементы соединяются или замещают друг друга, но и точно определять атомные массы.
Кратные эквивалентные массы.
Иногда два элемента соединяются друг с другом в разных соотношениях, образуя два (или более) разных соединения. Например, известны два оксида меди. В одном из них, оксиде меди(II), 31,8 ч. меди соединены с эквивалентной массой, т.е. с 7,9997 масс. ч., кислорода, тогда как в оксиде меди(I) эта же эквивалентная масса кислорода соединена с 63,6 масс. ч. меди. Соответственно эквивалентные массы меди равны 31,8 и 63,6, при этом последняя величина ровно в два раза больше первой, а значит, эквивалентные массы являются кратными величинами. Этот вывод согласуется с ранее высказанным утверждением, что элементы соединяются пропорционально их эквивалентным массам или величинам, кратным этим массам.
Электрохимический эквивалент.
При прохождении через электролит количества электричества 1 F (фарадей) = 96 500 Кл (1 Кл = 1 А Ч с) выделяется один химический эквивалент (т.е. эквивалентная масса) любого вещества. Следовательно, масса, выделяемая при прохождении 1 Кл (кулон), равна 1 экв., деленному на 96 500. Эта величина, называемая электрохимическим эквивалентом данного элемента, лежит в основе еще одного метода экспериментального определения эквивалентных масс.
Эквивалентные массы соединений.
Понятие эквивалентной массы было распространено и на соединения; в этом случае эквивалентная масса определяется как масса вещества, кратная эквивалентной массе элемента, являющегося ключевым для данного соединения. Например, для кислот ключевым элементом является водород, образующий в растворе ионы водорода; таким образом, эквивалентная масса кислоты есть масса кислоты, кратная 1,00797 массовым частям водорода, способного образовывать ионы водорода, т.е. водорода, который может быть замещен. Другими словами, эквивалентная масса кислоты равна ее молярной массе, деленной на основность кислоты. Эквивалентная масса основания есть масса основания, которая реагирует с эквивалентной массой любой кислоты и, следовательно, является химическим эквивалентом этой массы. Иначе можно сказать, что эквивалентная масса основания равна его молярной массе, деленной на валентность металла, образующего основание. Для солей эквивалентная масса обычно кратна эквивалентной массе металла, образовавшего эту соль; она равна молярной массе соли, деленной на произведение валентности металла и числа его атомов в молекуле соли. Для эквивалентной массы окислителей и восстановителей можно дать несколько определений. С практической точки зрения наиболее удобно определение, согласно которому эквивалентная масса есть количество вещества, кратное 7,9997 ч. кислорода (или реагирующее с ними) либо его эквиваленту. Другое определение основано на том, что при восстановлении этого количества кислорода происходит перенос одного электрона. В этом случае эквивалентная масса окислителя или восстановителя есть масса, соответствующая массе вещества, принимающего или отдающего один электрон в окислительно-восстановительной реакции.
Глинка Н.Л. Общая химия. Л., 1985
Степин Б.Д. Применение Международной системы физических единиц в химии. М., 1990
Степин Б.Д., Цветков А.А. Неорганическая химия. М., 1994