Эскалационная доза что это
Эскалационная доза что это
V. Антибактериальная терапия хирургических инфекций
Основные различия между антибиотикопрофилактикой и антимикробной терапией в хирургии
Важно различать ситуации, в которых показано назначение антибиотиков с профилактической целью, от ситуаций, при которых необходимо проведение курсов антибактериальной терапии. Эти ситуации требуют использования различных препаратов и различной длительности назначения антибиотиков. Профилактическое назначение антибиотиков в хирургии показано только для проведения периоперационной профилактики. Антибиотикопрофилактика, начинаясь непосредственно перед хирургическим вмешательством, не должна проводиться более 24 ч после операции, так как она не имеет целью предотвращение развития ИОХВ, связанной с контаминацией тканей в послеоперационном периоде. Необоснованно продолжительное использование антибиотиков с целью профилактики приводит к развитию антибиотикорезистентности и может стирать клиническую картину развившейся хирургической инфекции, затрудняя установление диагноза.
В противоположность антибиотикопрофилактике, антимикробная терапия первичной хирургической инфекции, начинаясь, как правило, еще в предоперационном периоде, продолжается более 24 ч после операции и направлена на лечение подтвержденной хирургической инфекции.
Показания для антибактериальной терапии у хирургических пациентов
Антимикробная терапия показана отдельным категориям пациентов с ИОХВ, а также пациентам с подтвержденной первичной хирургической инфекцией.
Решение о необходимости назначения антибиотиков с целью лечения ИОХВ принимается на основании класса ИОХВ (по традиционной классификации) и клинической картины инфекции. На практике, в большинстве случаев развития поверхностной ИОХВ разреза без признаков системного воспалительного ответа антибактериальная терапия не требуется. Наоборот, при глубоких ИОХВ разреза и ИОХВ органа/полости, а также при любых ИОХВ с системными симптомами инфекции необходимо назначение антибиотиков.
Необходимо подчеркнуть, что первичным мероприятием при развитии ИОХВ должно быть взятие клинического материала для культурального исследования. Более того, единственным адекватным методом лечения ИОХВ является дренирование раны и/или санация очага инфекции. Антибактериальная терапия показана в качестве дополнения к адекватному хирургическому вмешательству и только при наличии системных признаков инфекции.
В каких ситуациях показано проведение антибактериальной терапии, а не профилактики?
Назначение антибиотиков практически при всех «контаминированных» и «грязных» операциях по сути является терапией, а не профилактикой. В этих случаях антибактериальная терапия обычно начинается еще в предоперационном периоде и продолжается в течение нескольких дней после операции, то есть более 24 ч.
В отношении первичной хирургической инфекции, пациенты, у которых имеет место распространение инфекции за пределы первичного очага, должны получать антибиотики с целью терапии, то есть в течение более 24 часов. И, наоборот, у пациентов с очагом воспаления или инфекции, который может быть радикально удален во время операции (ограниченная локальная инфекция), достаточным считается проведение только периоперационной антибиотикопрофилактики, то есть назначение антибиотиков в течение не более 24 часов. Наличие распространенной инфекции, подтвержденной интраоперационно (например, обнаружение во время операции гнойной или инфицированной перитонеальной жидкости), является абсолютным показанием для назначения антибактериальной терапии, так как эти пациенты рассматриваются как пациенты с доказанной хирургической инфекцией.
Несмотря на принципиальные различия между терапевтическим и профилактическим назначением антибиотиков в хирургии, имеются ситуации, в которых назначение антибиотиков попадает в т.н. «переходную зону». Например, считается адекватным назначение антибиотиков в течение не более 24 ч у многих пациентов с травматическими и ятрогенными перфорациями кишечника (перфорация толстой кишки во время эндоскопического исследования или случайное вскрытие просвета тонкой кишки во время операции), а также у пациентов с гастродуоденальными перфорациями, оперированных в экстренном и неотложном порядке. Тем не менее, существует единое мнение экспертов, что пациенты с перфорациями тонкого или толстого кишечника и гастродуоденальными перфорациями, оперированные более чем через 12 и 24 ч с момента перфорации соответственно, рассматриваются как пациенты с первичной интраабдоминальной инфекцией, по поводу которой они должны получать антибактериальную терапию.
Учитывая вышесказанное, одной из основных задач локальных комитетов по политике применения антибиотиков является разработка четких рекомендаций, в которых для каждой области хирургии были бы определены показания для проведения антибиотикопрофилактики/антимикробной терапии на основании доказательных научных данных, полученных в контролируемых клинических исследованиях.
Основные принципы антибактериальной терапии хирургических инфекций
При назначении антибактериальной терапии каждый хирург должен строго соблюдать следующие рекомендации, позволяющие эффективно лечить пациентов и сдерживать развитие антибиотикорезистентности:
Эмпирическая и направленная антибактериальная терапия
Необходимо проводить различия между направленной и эмпирической терапией.
В тех случаях, когда возбудитель инфекции неизвестен, назначается эмпирическая антимикробная терапия, выбор которой проводится на основании локализации и вида инфекции, а также предполагаемого спектра наиболее вероятных возбудителей. При этом следует назначать антибиотики (в виде монотерапии или в комбинации), которые
При получении данных о выделенном возбудителе и его чувствительности к антибиотикам появляется возможность проведения коррекции терапии и смены антибиотика на препарат с более узким спектром активности, то есть проводить направленную терапию. Это позволяет снизить риск развития нежелательных реакций, уменьшить селективное давление антибиотиков на микроорганизмы и сэкономить материальные средства.
Пути введения антибиотиков
Единственно адекватными способами применения антимикробных препаратов в хирургии являются парентеральный (внутримышечный и внутривенный) и пероральный пути введения.
Основным преимуществом внутривенного пути введения антибиотиков является возможность быстрого достижения высоких сывороточных и тканевых концентраций. В связи с этим при тяжелых и жизнеугрожающих хирургических инфекциях требуется внутривенное введение антибактериальных препаратов.
Как только позволяет клиническое состояние пациента, следует стремиться к переходу с внутривенного на пероральный путь введения антибиотика. В то же время прием препаратов внутрь не рекомендуется у пациентов с нарушением сознания, рвотой, дисфагией или нарушениями функции ЖКТ, которые могут повлиять на биодоступность препарата.
Другие пути введения антибиотиков являются неадекватными, в связи с чем не должны применяться на практике.
Введение антибиотиков непосредственно в брюшную полость во время операции не позволяет достичь адекватных тканевых концентраций в месте локализации инфекции. Увеличение количества вводимого антибиотика приводит к развитию нежелательных системных реакций.
Местное применение антибиотиков в хирургии
Использование местных антибиотиков часто оказывается эффективным при лечении инфицированных ран. Тем не менее, комбинация местного и системного применения антибактериальных препаратов не обладает большей эффективностью, чем использование только системных или только местных антибиотиков. Более того, изолированное местное применение антибиотиков значительно уступает по эффективности системному применению. При местном использовании антибиотиков следует соблюдать следующие принципы: (1) не применять местно в ране или брюшной полости антибиотики, которые в данной ситуации не были бы показаны и для системного применения; (2) не использовать большее число антибиотиков, чем это было бы необходимо при их системном применении в данной ситуации. При расчете общей дозы следует суммировать количества препарата, введенного парентерально, и использованного местно в ране. Препараты для местного применения, используемые у пациентов с ожоговыми ранами, могут применяться и у отдельных категорий пациентов с обширными открытыми ранами.
За исключением ожоговых ран, местное применение системных антимикробных препаратов (обкалывание раны, введение в дренажные трубки, орошение полостей во время операции) с целью профилактики или лечения ИОХВ является порочной хирургической практикой и не может сравниваться по эффективности с парентеральным назначением антибиотиков. В исследованиях показано, что большинство антимикробных препаратов разрушается в результате взаимодействия с продуктами распада тканей, бактериальными токсинами и ферментами. Местное применение системных антибиотиков не позволяет создать оптимальные бактерицидные концентрации препарата в очаге инфекции и окружающих тканях, что приводит к формированию антибиотикорезистентности у микроорганизмов.
Де-эскалационная терапия
Таким образом, адекватная стартовая терапия представляет собой важный фактор, определяющий исход заболевания у этих пациентов. Адекватной терапией считается назначение с того момента, когда взят материал для культурального исследования, как минимум одного антибиотика, к которому in vitro чувствительны все предполагаемые возбудители. Де-эскалационная терапия представляет собой подход, который «балансирует необходимость назначения адекватной стартовой антибактериальной терапии пациентам высокого риска и необходимость избежать необоснованного использования антибиотиков, которое способствует развитию антибиотикорезистентности».
Де-эскалационная терапия проводится в 2 этапа. Первый этап предполагает назначение антибиотиков широкого спектра действия. Основная концепция состоит в том, что при первом подозрении на инфекцию следует назначить антибиотик широкого спектра, активный в отношении как грам(-), так и грам(+) микроорганизмов. Это позволяет снизить летальность, предотвратить развитие органной недостаточности и уменьшить длительность пребывания пациента в стационаре. Естественно, что для каждого стационара крайне важно иметь локальные микробиологические данные о наиболее вероятных возбудителях инфекций и их чувствительности к антибиотикам.
Второй этап заключается в собственно де-эскалации антибактериальной терапии, направленной на максимальное уменьшение вероятности появления резистентных штаммов микроорганизмов и осуществление более эффективного с экономической точки зрения лечения. После получения предварительных данных (через 24-72 ч) о выделенном возбудителе инфекции и его чувствительности к антибиотикам появляется возможность перейти на применение антибиотиков с узким спектром активности или, при необходимости, завершить курс антибактериальной терапии. Все это позволяет избежать лишних экономических затрат, необоснованно длительного назначения антибиотиков, селективного давления, которое приводит к развитию антибиотикорезистентности, высокой заболеваемости и летальности, связанных с неадекватной антибактериальной терапией.
Основные принципы де-эскалации:
Ступенчатая терапия в хирургии
Большинство госпитализированных пациентов с инфекциями должны получать антимикробные препараты перорально. Исключение составляют такие ситуации, как крайне тяжелое состояние пациента, неспособность приема препаратов per os, отсутствие сходного по эффективности перорального антибиотика. Показано, что если пациент может принимать антибиотики внутрь, и у него нет нарушений функции ЖКТ, то различий в исходах заболевания при использовании эквивалентных препаратов независимо от способа применения (внутривенное введение или пероральный прием) не наблюдается. При принятии решения о проведении ступенчатой терапии более важно учитывать не путь введения, а спектр активности антибиотика, его биодоступность и степень проникновения в ткани. При проведении ступенчатой терапии выбранный пероральный антибиотик должен создавать в сыворотке крови и тканях концентрации, эквивалентные применявшемуся внутривенному препарату.
При переходе с внутривенного на пероральный режим терапии необходимо, чтобы общая длительность курса антибиотиков не превышала таковую при проведении только парентеральной антибиотикотерапии в данной ситуации. Более того, у многих пациентов при отчетливом клиническом улучшении состояния, нормализации температуры и количества лейкоцитов в крови антибиотики можно отменить, не переходя на пероральный режим терапии. Продолжение антибактериальной терапии в данной ситуации является необоснованным.
Несмотря на очевидные преимущества ступенчатой терапии, этот подход крайне медленно внедряется в клиническую практику, особенно в хирургии. До 75% госпитализированных пациентов с различными инфекциями теоретически могли бы получать ступенчатую терапию. В контролируемых клинических исследованиях подтверждена эффективность ступенчатой терапии у пациентов с инфекциями мочевыводящих путей, инфекциями кожи и мягких тканей, остеомиелитом. Также в рандомизированных проспективных клинических исследованиях доказана целесообразность использования ступенчатой терапии у пациентов с интраабдоминальными инфекциями. Так, например, в некоторых исследованиях ступенчатая терапия интраабдоминальных инфекций комбинацией ципрофлоксацин + метронидазол (внутривенное введение с последующим переходом на пероральный прием) оказалась такой же эффективной, как и стандартный внутривенный режим терапии этими антибиотиками.
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
В основе концепции деэскалационной терапии лежит принцип, который направлен на повышение эффективности лечения наиболее сложных и тяжелых, с точки зрения антимикробной терапии, нозокомиальных инфекций – нозокомиальной пневмонии и ангиогенных инфекций. Необходимость повышения эффективности лечения именно этих инфекций заключается в том, что из всех нозокомиальных инфекций – именно пневмония и ангиогенные инфекции имеют высокую вероятность неблагоприятного исхода непосредственно связанного с течением инфекции. Понятие деэскалационной терапии тесно связано с понятиями адекватной и неадекватной антимикробной терапии. Адекватной антимикробной терапией считается такая, при которой хотя бы один из используемых антибиотиков оказывается активным в отношении, выделенного при бактериологическом исследовании, возбудителя данной инфекции. Следовательно, неадекватной терапией считается та, ни один компонент которой не активен в отношении выделенного возбудителя инфекции. Несмотря на то, что пациенты с тяжелыми нозокомиальными инфекциями требуют комплексного лечения, именно неадекватная антимикробная терапия инфекции является неблагоприятным прогностическим фактором и достоверно увеличивает вероятность неблагоприятного исхода инфекции. Концепция деэскалационной терапии содержит доказательства необходимости применения у пациентов с тяжелыми нозокомиальными инфекциями наиболее эффективных антимикробных препаратов в режиме стартовой терапии и объясняет причины недостаточной эффективности эксалационного принципа лечения, который предполагает применение в режиме стартовой терапии препаратов, которые обычно обладают высокой эффективностью в отношении внебольничных инфекций. Основным различием возбудителей вне– и внутрибольничных инфекций является их резистентность к антимикробным препаратам и, следовательно, выбор антимикробных препаратов является ключевым моментом, способным оказывать влияния на исход лечение больных тяжелыми нозокомиальными инфекциями.
В основе концепции деэскалационной терапии лежит принцип, который направлен на повышение эффективности лечения наиболее сложных и тяжелых, с точки зрения антимикробной терапии, нозокомиальных инфекций – нозокомиальной пневмонии и ангиогенных инфекций. Необходимость повышения эффективности лечения именно этих инфекций заключается в том, что из всех нозокомиальных инфекций – именно непосредственно связанного с течением инфекции. Понятие деэскалационной терапии тесно связано с понятиями адекватной и неадекватной антимикробной терапии. Адекватной антимикробной терапией считается такая, при которой хотя бы один из используемых антибиотиков оказывается активным в отношении, выделенного при бактериологическом исследовании, возбудителя данной инфекции. Следовательно, неадекватной терапией считается та, ни один компонент которой не активен в отношении выделенного возбудителя инфекции. Несмотря на то, что пациенты с тяжелыми нозокомиальными инфекциями требуют комплексного лечения, именно неадекватная антимикробная терапия инфекции является неблагоприятным прогностическим фактором и достоверно увеличивает вероятность неблагоприятного исхода инфекции. Концепция деэскалационной терапии содержит доказательства необходимости применения у пациентов с тяжелыми нозокомиальными инфекциями наиболее эффективных антимикробных препаратов в режиме стартовой терапии и объясняет причины недостаточной эффективности эксалационного принципа лечения, который предполагает применение в режиме стартовой терапии препаратов, которые обычно обладают высокой эффективностью в отношении внебольничных инфекций. Основным различием возбудителей вне– и внутрибольничных инфекций является их резистентность к антимикробным препаратам и, следовательно, выбор антимикробных препаратов является ключевым моментом, способным оказывать влияния на исход лечение больных тяжелыми нозокомиальными инфекциями.
Проблемы диагностики нозокомиальных инфекций и выбора режима антибактериальной терапии
Обычно развитие нозокомиальных инфекций сопровождается ухудшением состояния пациентов, связанным с появлением местных признаков инфекции, признаков генерализованного воспаления и интоксикации, органной дисфункции. Однако у тяжелых больных с наличием признаков генерализованнного воспаления и полиорганной недостаточности, развитие нозокомиальной инфекции может не иметь яркой клинической симптоматики. Имеются литературные данные, указывающие, что только у одной трети пациентов в тяжелом состоянии имеется яркая клиническая симптоматика, указывающая на появление нозокомиальной инфекции. Поэтому обычно для подтверждения нозокомиальной инфекции применяются микробиологические методы, возволяющие установить источник инфекции и возбудителя. Необходимо отметить, что микробиологическое исследование, как минимум, продолжается 24–72 часа. Задержка с назначением антимикробной терапии – основного компонента лечения инфекций не может быть объяснена ожиданием данных микробиологического исследования. Поэтому после диагностики инфекции на основании клинических, функциональных и лабораторных исследований, необходимо выбрать режим стартовой антибактериальной терапии.
Проблема выбора антибактериальной терапии нозокомиальной инфекции всегда несет в себе высокую вероятность выбора неадекватного стартового режима. Для того чтобы максимально снизить вероятность выбора неадекватной антимикробной терапии, существуют определенные подходы или правила. Эти правила заключаются в следующем.
1. Эмпирическая терапия должна проводиться в режиме монотерапии препаратом, обладающим широким спектром антибактериального действия или комбинацией препаратов, позволяющей максимально расширить антимикробный спектр.
2. Для выбора адекватной терапии необходимо использовать данные локального микробиологического мониторинга и чувствительности флоры.
3. Выбор антибактериальных препаратов должен быть основан на определенных данных о пациенте:
a. локализации инфекции (указание на определенный спектр возбудителей);
b. тяжести инфекции (количество возбудителей);
c. возможности хирургической санации очага инфекции;
d. прогнозе развития и исхода инфекции;
e. характере предшествующей антибактериальной терапии (резистентность флоры).
Опасность неадекватного выбора стартовой антибактериальной терапии
Неадекватный выбор антимикробной терапии может быть связан со следующими причинами: возбудитель инфекции имеет природную или приобретенную резистентность к выбранному режиму антимикробной терапии, препарат применяется в неправильной дозе или не выдерживается правильно промежутки между введением антибактериального препарата, не применяется комбинированная терапия, если она показана [1,2]. Две последние причины неадекватной антимикробной терапии имеют субъективный характер и могут быть легко исправлены с помощью информации, которая, как правило, содержится в инструкции к применению препарата, прикладываемой изготовителем. Сведения о природной резистентности предполагаемого возбудителя имеется в большинстве общедоступных справочников по антимикробной терапии и должны учитываться при эмпирическом назначении препарата. Существенно сложнее дело обстоит с характеристикой приобретенной резистентности возбудителя, которая может быть получена только в результате микробиологического исследования или обобщения данных мониторинга флоры, циркулирующей в данном отделении.
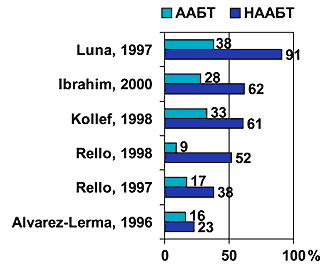
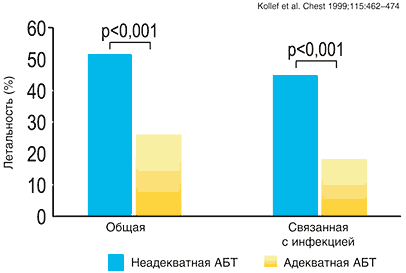
Сложность выбора адекватной эмпирической терапии подтверждена данными различных исследователей [3–6]. Так неадекватный выбор стартовой антибактериальной терапии нозокомиальных инфекций согласно этим исследованиям широко варьировал от 24% до 73%. В условиях отсутствия адекватной антибактериальной терапии, т.е. невозможности контроля очага инфекции, существенно ухудшаются результаты лечения. Согласно представленным сводным клиническим данным (рис. 1), эффективность эмпирической антимикробной терапии оказывает существенное влияние на исход заболевания. Так, пациенты отделения реанимации и интенсивной терапии, получавшие адекватную антимикробную терапию имели примерно в два раза меньшую летальность по сравнению с пациентами, получившими неадекватную антимикробную терапию. У пациентов с летальным исходом в результате инфекции (рис. 2) эффект влияния адекватности антибактериальной терапии выражен еще более существенно. Таким образом, неадекватная стартовая антимикробная терапия является независимым фактором риска неблагоприятного исхода тяжелых нозокомиальных инфекций.
Рис. 1. Сравнение летальности больных тяжелыми нозокомиальными инфекциями при адекватной (ААБТ) и неадекватной (НААБТ) стартовой антимикробной терапии [2,4-7]
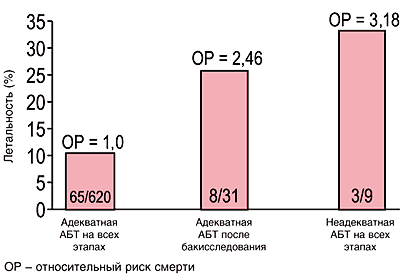
Еще одним важным фактором, влияющим на исход больных тяжелыми нозокомиальными инфекциями, является своевременность назначения адекватной стартовой терапии. На рисунке 3 представлены результаты сравнения влияния на результаты лечения больных нозокомиальным ангиогенным сепсисом [8]. В группе больных, получивших адекватную стартовую антимикробную терапию, летальность составила 11%, в группе получивших адекватную антибактериальную терапию после получения микробиологических данных, т.е. позже на несколько суток, летальность увеличилась до 26%. При этом относительный риск летального исхода увеличился в 2,5 раза. В группе, которая по разным причинам вовсе не получала адекватной антибактериальной терапии, летальность составила 34%, а относительный риск летального исхода по сравнению с первой группой вырос в 3,2 раза. Таким образом, у больных, которым антибактериальная терапия назначалась с задержкой или не назначалась вовсе, вероятность летального исхода оказалась близкой. То есть, не само по себе назначение антибактериальной терапии, а только назначение адекватной (эффективной) антибактериальной терапии оказывает существенное влияние на исходы тяжелых нозокомиальных инфекций.
Рис. 3. Снижение летальности больных ангиогенными инфекциями при применении адекватной АБТ
Оптимизация антимикробной терапии нозокомиальных инфекций
Учитывая тот факт, что неадекватный и несвоевременный выбор адекватной терапии являются факторами риска неблагоприятного исхода лечения инфекции, необходимо предпринимать меры, направленные на коррекцию этих недостатков. Оптимизация антибактериальной терапии может быть проведена за счет:
Расширение спектра антимикробных препаратов
Необходимо отметить, что понятие «широкого спектра антимикробной активности» препарата претерпевает определенные изменения в процессе его использования в клинической практике. Например, препараты тетрациклинового ряда, первоначально считавшиеся препаратами широкого спектра действия, к настоящему времени в значительной мере утратили это значение. Это происходит из–за изменения актуальности возбудителей инфекций, роста резистентности связанного с широким применением препарата в клинической практике и других причин. В зависимости от особенностей препарата, все эти факторы могут вообще привести к существенному ограничению его применения. Не все препараты широкого спектра одинаково активны в отношении различной флоры. Например, цефалоспорины 3 генерации, которые по сравнению с цефалоспоринами 1 и 2 генераций обладают более широким спектром активности в отношении грамотрицательной флоры, однако уступают им в активности в отношении стафилококков. По–видимому, в настоящее время наиболее широким спектром антимикробной активности обладают карбапенемы, цефалоспорины 4 генерации и фторхинолоны. Однако в отношении фторхинолонов происходит быстрый рост резистентности нозокомиальной флоры, что приводит к существенному ограничению их применения у пациентов с нозокомиальными инфекциями.
Исторически ограничение спектра активности антимикробного препарата компенсировали одновременным применением препарата, обладающего активностью в отношении других возбудителей. Это подход называется комбинированной терапией. Так, например, для расширения спектра природных пенициллинов и цефалоспоринов 1–2 генерации, обладающих высокой активностью преимущественно в отношении грамположительной флоры, применяются комбинации с препаратами других групп – аминогликозидами или фторхинолонами, обладающих преимущественной активностью в отношении грамотрицательной флоры. Комбинированная терапия может состоять из 2, 3 и более препаратов, однако имеются клинические данные, указывающие на отсутствие дополнительной клинической выгоды от применения 3 и более препаратов, одновременно с этим увеличивается вероятность возникновения токсических эффектов, обусловленных препаратами, входящими в комбинацию. Тем не менее до настоящего времени применение комбинированной терапии считается оправданным для эмпирической терапии полимикробных инфекций (абдоминальные инфекции) или лечения инфекций, вызванных резистентной флорой (Ps. aeruginosa).
Расширение спектра антимикробной активности может быть получено за счет внедрения новых препаратов. Так, внедрение в клиническую практику в середине 80–х годов ХХ века имипенема/циластатина (Тиенам), препарата, относящегося в то время к новому классу антимикробных препаратов – карбапенемов, имело очень важные последствия. Результаты многочисленных микробиологических исследований этиологической структуры различных, в том числе нозокомиальных инфекций, указывают на высокую активность этого класса препаратов. Важным отличием этого класса препаратов является ультраширокий спектр антимикробной активности, включающий возбудителей, относящихся к грамположительной, грамотрицательной и анаэробной флоре. Примерно за 20 лет клинического использования карбапенемов клинически значимое нарастание резистентности отмечено в последние годы только в отношении Ps. aeruginosa.
Клинические исследования последних лет указывают на необходимость лечения тяжелых инфекций, особенно нозокомиальных, антимикробными препаратами, обладающими широким спектром антимикробной активности, или комбинациями антимикробных препаратов. Применение препаратов широкого спектра в режиме эмпирической терапии позволяет увеличить вероятность клинической эффективности режима антимикробной терапии. Однако рост резистентности флоры, например, грамположительной (метициллинрезистентные стафилококки, резистентные энтерококки) приводит к необходимости в режиме эмпирической терапии, даже в случае применения карбапенемов, применять их в комбинации с препаратами, активными в отношении этой резистентной флоры (ванкомицин, линезолид). Но после получения результатов микробиологического исследования может оказаться, что резистентных грамположительных возбудителей не будет выявлено и необходимость в применении комбинированной терапии отпадет. Переход с комбинированной терапии на монотерпию нужно рассматривать, как применение принципа деэскалационной терапии.
Очень важным является вопрос о возможности деэскалационной терапии при применении в режиме эмпирической терапии монотерапии карбапенемами. Этот вопрос является не таким простым, как кажется на первый взгляд. Если карбапенемы, назначенные в режиме эпирической терапии абдоминального сепсиса, были заменены стандартными для лечения перитонита препаратами после стабилизации состояния больного и получения микробиологических данных о наличии внегоспитальной флоры, то изменение тактики антибактериальной терапии рассматривается, как деэскалационная терапия.
При применении карбапенемов в режиме монотерапии для лечения тяжелых госпитальных инфекций (нозокомиальная пневмония, связанная с проведением искусственной вентиляции легких), вопрос о возможности проведения деэскалационной терапии остается до настоящего не совсем ясным. С одной стороны, если нозокомиальная инфекция является основной причиной тяжести состояния пациента, корректно произведен посев из бронхов, выявлен возбудитель пневмонии и определена его чувствительность, то возможен переход на препараты более узкого спектра, т.е. проведение деэскалационной терапии. Однако при отсутствии микробиологических данных переход на деэскалационную терапию затруднителен. Также затруднителен переход на деэскалационную терапию при наличии нескольких локусов инфекции, не связанных между собой патогенетически (например, при инфицированном панкреонекрозе и наличии нозокомиальной пневмонии). Таким образом, деэскалационный принцип применения антимикробной терапии является гибким инструментом, направленным на контроль очага инфекции, позволяющим повысить эффективность антимикробной терапии и вместе с тем избегать избыточного применения антимикробных препаратов – важного фактора развития резистентности нозокомиальной флоры. Этапы реализации принципа деэскалационной терапии представлены на рисунке 5.
Рис. 5. Принцип применения деэскалационной антимикробной терапии
Выбор пациентов для проведения деэскалационной терапии и оценка эффективности
Принцип деэскалационной терапии должен применяться при лечении больных в критическом состоянии, тяжесть которых связана с течением инфекции и высокой вероятности летального исхода в случае неэффективности антибактериальной терапии. Теоретически нуждающимися в проведении этого принципа лечения являются группами пациентов с:
К настоящему времени, к сожалению, исследований, напрямую указывающих на высокую эффективность деэскалационной антибактериальной терапии при всех вышеуказанных нозологических формах, нет. Тем не менее имеются отдельные исследования, указывающие на высокую потенциальную возможность этого подхода.
При применении метода деэскалационной терапии у тяжелых больных с нозокомиальной пневмонией, связанной с искусственной вентиляцией легких и наличием факторов риска резистентной нозокомиальной флоры (продолжительность ИВЛ более 7 суток и наличие предшествующей антибактериальной терапии) проведена оценка применения карбапенемных антибиотиков в сочетании с ванкомицином по сравнению со стандартной антибактериальной терапией [9].
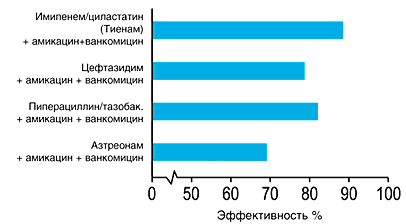
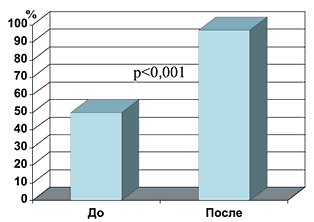
На рисунке 6 показано достоверное повышение адекватности антибактериальной терапии в связи с применением комбинации препаратов, которая оказывается активной в отношении около 90% возбудителей нозокомиальной пневмонии по сравнению с 50% – при применении стандартной антимикробной терапии.
Рис. 6. Увеличение адекватности стартовой терапии после внедрения принципа деэскалационной терапии
Вторым преимуществом (рис. 7) применения указанной комбинации является достоверное укорочение продолжительности антибактериальной терапии примерно в два раза, что может существенно компенсировать затраты, связанные с применением в режиме деэскалационной терапии более дорогостоящих препаратов.
Рис. 7. Укорочение продолжительности антимикробной терапии при внедрении принципа деэскалационной терапии
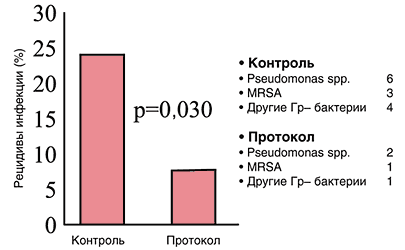
Третьим, не менее важным результатом данного исследования (рис. 8) явилось то, что у пациентов, которым применялась комбинация карбапенема и ванкомицина, достоверно снизилось количество рецидивов инфекции. Необходимо отметить существенное снижение количества резистентной флоры при развитии рецидива инфекции, что отражает способность выбранного режима терапии снижать риск появления и персистенции резистентной флоры. Так, количество выделенных штаммов резистентной флоры снизилось примерно в три раза.
Рис. 8. Снижение частоты рецидивов инфекции и повторного выделения резистентной флоры
Нозокомиальные инфекции представляют собой серьезную проблему современной клинической медицины. Рост резистентности нозокомиальной флоры опережает разработку новых препаратов для эффективного лечения инфекций, вызванных резистентной флорой. В этих условиях меры по повышению эффективности применения антибактериальных препаратов и ограничению роста резистентности нозокомиальной флоры необходимо гармонично сочетать. Многими экспертами в области антибактериальной терапии поддерживается концепция деэскалационной терапии и необходимости применения адекватной антимикробной терапии для стартовой терапии тяжелых инфекций [1,2]. Учитывая то, что концепция деэскалационной терапии выдвинута сравнительно недавно, крупных систематических исследований по оценке ее клинической эффективности недостаточно. Однако аргументы и логика применения этого подхода, имеющиеся клинические данные вписываются в объективную необходимость совершенствования глобальной стратегии антибактериальной терапии и заслуживают самого внимательного изучения и применения в клинической практике.
Нозокомиальные инфекции представляют собой серьезную проблему современной клинической медицины. Рост резистентности нозокомиальной флоры опережает разработку новых препаратов для эффективного лечения инфекций, вызванных резистентной флорой. В этих условиях меры по повышению эффективности применения антибактериальных препаратов и ограничению роста резистентности нозокомиальной флоры необходимо гармонично сочетать. Многими экспертами в области антибактериальной терапии поддерживается концепция деэскалационной терапии и необходимости применения адекватной антимикробной терапии для стартовой терапии тяжелых инфекций [1,2]. Учитывая то, что концепция деэскалационной терапии выдвинута сравнительно недавно, крупных систематических исследований по оценке ее клинической эффективности недостаточно. Однако аргументы и логика применения этого подхода, имеющиеся клинические данные вписываются в объективную необходимость совершенствования глобальной стратегии антибактериальной терапии и заслуживают самого внимательного изучения и применения в клинической практике.
1. Kollef MH et al. Chest 1999;115:462–474.
2. Ibrahim EH et al. Chest 2000;118:146–155.
3. Alvarez–Lerma F et al. Intensive Care Med 1996;22:387–394.
4. Kollef MH et al. Chest 1998;113:412–420.
5. Luna CM et al. Chest 1997;111:676–685.
6. Rello J et al. Am J Resp Crit Care Med 1997;156:196–200.
7. Trouillet et al. Am J Respir Crit Care Med 1998;157:531–539
8. Weinstein A et al. Clin Infect Dis 1997; 24: 584–602.
9. Ibrahim et al. Crit Care Med 2001;29:1109–1115