Кто такие трипаносомы какие болезни они вызывают
Кто такие трипаносомы какие болезни они вызывают
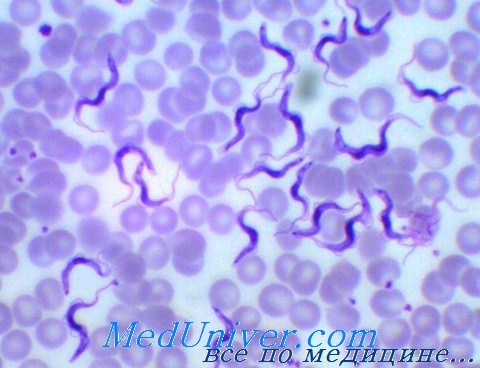
Африканский трипаносомоз. Возбудители африканского трипаносомоза — Trypanosoma brucei gambiense и Trypanosoma brucei rhodesiense; переносчик — муха цеце. Хозяином для Т. brucei gambiense может быть только человек. Т. brucei rhodesiense паразитируют в организме антилоп и крупного рогатого скота. В крови жизнедеятельность паразита подавляет иммунная система хозяина, но со временем структура поверхностных антигенов возбудителя изменяется, и он снова начинает размножаться, при этом развивается общая лимфаденопатия и отёчность кожи.
У пациента возникает гипергаммаглобулинемия, что делает организм восприимчивым к вторичным бактериальным инфекциям. При проникновении паразита в головной мозг развивается хронический прогрессирующий энцефалит, пациент впадает в кому и умирает часто от вторичной бактериальной пневмонии.
Диагностика и лечение африканского трипаносомоза. Возбудителя обнаруживают в крови, спинномозговой жидкости и лимфатических узлах больного. Для диагностики также используют серологические тесты. Проведение спинномозговой пункции возможно только после уничтожения паразитов в циркулирующей крови (сурамин) во избежание повторного заражения. При развитии церебральных осложнений лечение следует проводить меларсопролом (обладает высокой токсичностью). При лечении болезни в Западной Африке эффективен эфлорпитин.
Болезнь Шагаса (южноамериканский трипаносомоз), возбудителем которой является Trypanosoma cruzi, передаётся при укусе триатомового клопа. Выделяют три основные стадии течения болезни: острая инфекция (отёк кожи, неправильная лихорадка, шок, наблюдается высокая смертность среди детей), латентная форма и поздние проявления (ахалазия, мегаколон, аритмии, кардиомиопатия и нейропатия).
Диагностика южноамериканского трипаносомоза. Возбудителей обнаруживают при микроскопии или с помощью ксенодиагностики (заражение лабораторных животных). Кроме того, применяют серологические методы исследований.
Лечение южноамериканского трипаносомоза. В острой стадии заболевания применяют нифуртимокс и бензнидазол. Лечение осложнений в основном паллиативное (искусственные водители ритма при сердечной блокаде вследствие кардиомиопатии, хирургическое вмешательство при мегаколоне).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Трипаносома
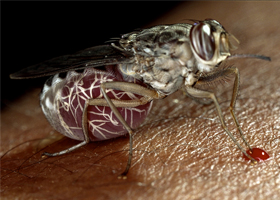
Знакомьтесь: трипаносома
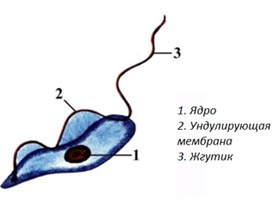
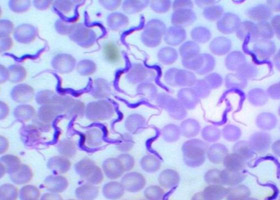
Передвигается трипаносома за счет жгутика, тянущегося вдоль всего тела, который приводится в движение за счет сокращений волнообразной (ундулирующей) мембраны. Размножается продольным делением, питается за счет всасывания нужных ей веществ поверхностью оболочки. Поскольку относится к классу анаэробных организмов, в кислороде не нуждается.
В организм человека трипаносома попадает при укусах насекомых, являющихся промежуточными носителями. В зависимости от вида микроорганизма, это могут быть триатомовый клоп или муха Цеце. По данным статистики, на сегодняшний день насчитывается около 5 миллионов зараженных той или иной разновидностью трипаносомоза, но отмечается и тенденция к снижению количества заболеваний.
Жизненный цикл трипаносомы
В течение своего жизненного цикла строение трипаносомы претерпевает значительные изменения.
Различают следующие стадии:
Трипаносома обладает уникальным механизмом защиты: чтобы «обмануть» иммунную систему носителя, она активизирует специальный ген, который способен полностью перестраивать структуру ее оболочки. В результате, иммунные клетки оказываются не в состоянии распознать «врага», процесс его идентификации затягивается, а за это время трипаносома успевает дать многочисленное потомство.
Разновидности трипаносомы
В зависимости от переносчика и вида заболевания, различают трипаносому.
Бруцеи трипаносома
Переносчиком является муха цеце, вызывает африканский трипаносомоз у человека и животных.
Попадая в кишечник своего промежуточного носителя (мухи цеце), микроорганизм переходит в стадию эпимастиготы и, локализуется в хоботке. При укусе мухи трипаносома попадает в организм окончательного хозяина (человека или животного).
Переносчиком этого вида трипаносомы является триатомовый клоп, укус которого вызывает болезнь Шагаса, или американский трипаносомоз. Название связано с тем, что данный вид распространен, в основном, в Южной Америке.
В данном случае возбудитель от зараженного животного проникает в кишечник клопа, где переходит в стадию эпимастиготы, а затем вместе с испражнениями попадает на кожу человека.
Далее, проникает в организм (при расчесывании места укуса, во время еды и т.д.), здесь приобретает форму амастиготы и начинает размножаться.
Укусы насекомых являются основным, но не единственным путем заражения. Реже, но встречаются случаи инфицирования при переливании крови или трансплацентарным способом: то есть, внутриутробно.
Самые опасные виды трипаносомоза
При укусе насекомого – носителя трипаносомы возможны аллергические реакции, поражения кроветворных и иммунных внутренних органов. К тому же, этот микроорганизм способен навредить и домашним животным, существенно сократив их поголовье. Но наиболее опасными признаны две разновидности трипаносомоза, на которых мы остановимся подробнее.
Сонная болезнь
При этом заболевании (второе название – африканский трипаносомоз) поражаются лимфатическая и нервная система человека, заразиться ею можно при укусе мухи цеце. Различают два вида сонной болезни: гамбийскую и родезийскую, которую вызывают соответствующие разновидности трипаносомы бруцеи.
Гамбийская форма вызывает хроническое заболевание, когда состояние больного ухудшается медленно, в течение нескольких месяцев, а иногда и лет.
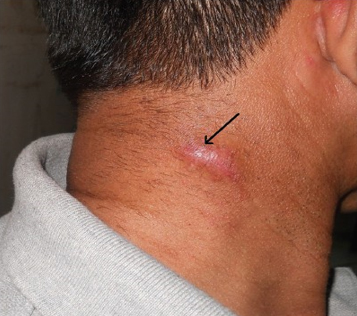
Типичными симптомами хронической сонной болезни являются появление в месте укуса трипаносомного шанкра (на ранних стадиях) – болезненного образования, напоминающего фурункул, который через некоторое время заживает, оставляя после себя рубец.
На более поздних стадиях у больных отмечается увеличение лимфатических узлов в области шеи, нарастающая сонливость, тремор, невнятность речи, возможны судороги и коматозные состояния. Без лечения вероятность смертельного исхода приближена к 100%.
Родезийская форма вызывает более тяжелую и скоротечную болезнь. Состояние больного быстро ухудшается, ярче выражены все симптомы, часто поражается сердце. Если вовремя не оказать медицинскую помощь, человек может умереть уже через несколько месяцев, причина смерти – развившиеся на фоне сонной болезни малярия, пневмония, дизентерия и т.д.
При подозрении на сонную болезнь предварительный диагноз ставится при осмотре шейных лимфоузлов, а лабораторные исследования, в результате которых выявлено наличие трипаносомы в организме, дают основание для постановки диагноза окончательного. Лечение наиболее эффективно на ранних стадиях.
Болезнь Шагаса
Это заболевание, имеющее второе название – американский трипаносомоз, вызывает укус триатомового клопа.
В организм человека возбудитель болезни Шигаса – трипаносома крузи может попасть как непосредственно при укусе клопа-носителя, так и в результате расчесывания ранок. Инкубационный период длится до 3-х недель, после чего может развиться отек века, имеющий багровый оттенок (синдром Роменьи, считающийся одним из симптомов болезни Шегаса).
При острой форме ярко выраженные симптомы практически отсутствуют, больных может беспокоить головная боль, отеки конечностей. Но особенно опасна хроническая форма заболевания, поскольку она довольно долго вообще не дает о себе знать и проявляется лишь после того, как во внутренних органах произойдут необратимые изменения, которые при отсутствии медицинской помощи могут привести к смерти больного.
При подозрении на болезнь Шегаса выполняется тщательный сбор анамнеза. Диагноз ставится на основании лабораторных и серологических исследований.
На сегодняшний день эффективного лекарства, способного дать 100% гарантию выздоровления, нет, современные препараты способны лишь уменьшить количество смертных случаев. Больным прописываются средства, поддерживающие работу внутренних органов. В некоторых случаях, при тяжелых поражениях ЖКТ, показано оперативное вмешательство.
Профилактика трипаносомоза
В рамках борьбы с возможностью заражения выполняется регулярная обработка инсектицидами мест скопления насекомых-переносчиков. Среди населения районов «зоны риска» проводится разъяснительные беседы, цель которых – объяснить, что такое трипаносомоз и насколько он опасен. Донорская кровь обязательно исследуется на наличие трипаносомы.
И в заключение
«Как хорошо, что у нас этого нет!» – с облегчением скажет читатель. Действительно, климат средней полосы не подходит ни самой трипаносоме, ни ее носителям. Но ежегодно тысячи туристов отправляются в жаркие страны, чтобы насладиться теплом, солнцем и экзотикой. Если вы тоже собираетесь в дорогу – проявите осторожность: от этого зависит ваша жизнь и здоровье!
Африканский трипаносомоз человека (сонная болезнь)
Основные факты
Африканский трипаносомоз человека, также известный как сонная болезнь, относится к трансмиссивным паразитарным заболеваниям. Его возбудителям являются паразитирующие простейшие, принадлежащие к роду Trypanosoma. Они передаются человеку при укусе мухи цеце (род Glossina), инфицированной от людей или животных, выступающих в роли хозяев этих патогенных для человека паразитов.
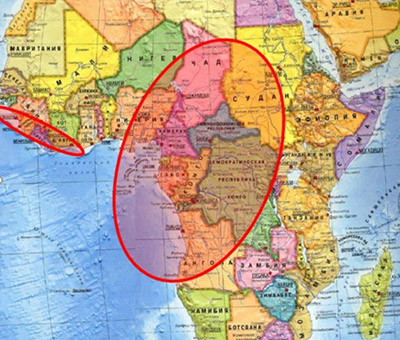
Муха цеце обитает только в Африке к югу от Сахары, и передавать болезнь могут лишь некоторые ее виды. По неизвестным на сегодняшний день причинам во многих районах ареала обитания мухи цеце случаи сонной болезни не отмечаются. Наиболее подвержены укусам мухи цеце и, следовательно, данной болезни жители эндемичных сельских районов, занимающиеся сельским хозяйством, рыболовством, животноводством и охотой. Случаи болезни могут отмечаться как на территории отдельных деревень, так и в целом регионе. В пределах отдельно взятого инфицированного района интенсивность распространения болезни может сильно варьироваться от одного сельского поселения к другому.
Формы африканского трипаносомоза человека
Африканский трипаносомоз человека имеет две формы в зависимости от вида возбудителя:
Существует еще одна форма трипаносомоза, которая встречается преимущественно в Латинской Америке. Она известна как американский трипаносомоз или болезнь Шагаса. Возбудитель болезни Шагаса относится к другому подроду Trypanosoma, передается другими переносчиками и вызывает заболевание, клинические проявления которого отличаются от африканского трипаносомоза человека.
Трипаносомоз животных
Другие виды и подвиды паразитов рода Trypanosoma являются патогенными для животных и вызывают трипаносомоз у некоторых видов диких и домашних животных. Трипаносомоз крупного рогатого скота называют нагана. Трипаносомоз домашних животных, особенно крупного рогатого скота, серьезно подрывает экономическое развитие инфицированных сельских районов.
Животные могут быть носителями патогенных для человека паразитов, особенно T.b. rhodesiense, причем домашние и дикие животные являются важным резервуаром последнего. Животные могут быть также инфицированы T.b. gambiense и, вероятно, могут также выступать в качестве его резервуара, хотя и в меньшей степени. Тем не менее реальная роль животного резервуара в эпидемиологии гамбийской формы болезни до сих пор недостаточно изучена.
Крупные эпидемии
За последнее столетие в Африке произошло несколько эпидемий:
В 1920 г. борьба с эпидемией велась силами передвижных бригад, которые выполняли скрининг миллионов людей, проживающих в районах высокого риска. К середине 1960-х гг. распространение болезни было взято под контроль, и на всем континенте регистрировалось менее 5 000 случаев заболевания. После такого успеха эпиднадзор был ослаблен, в связи с чем болезнь вернулась, и к 1970 г. в нескольких регионах ее вспышки разрослись до эпидемии. В 1990-е гг. и в начале XXI века благодаря усилиям ВОЗ, осуществлению национальных программ по борьбе с болезнью, двустороннему сотрудничеству и деятельности неправительственных организаций (НПО) тенденция к росту заболеваемости была остановлена.
Поскольку число новых случаев заболевания африканским трипаносомозом человека за период с 2000 по 2012 г. значительно сократилось в результате международных координированных усилий, в Дорожной карте ВОЗ по борьбе с забытыми тропическими болезнями была поставлена цель по его элиминации как проблемы общественного здравоохранения к 2020 г. и ликвидации передачи инфекции (сведение числа случаев к нулю) к 2030 г.
Бремя болезни
Сонная болезнь угрожает здоровью миллионов людей в 36 странах Африки к югу от Сахары. Многие из них проживают в отдаленных районах с ограниченным доступом к необходимой медицинской помощи, что затрудняет эпиднадзор и, следовательно, диагностику и лечение больных. Кроме того, важными факторами, способствующими передаче инфекции, являются перемещение населения, вооруженные конфликты и нищета.
Текущий ареал распространения заболевания
Показатели распространенности болезни варьируются между странами, а также между районами на территории отдельно взятой страны.
Механизм передачи и симптомы
Болезнь передается, главным образом, при укусе инфицированной мухи цеце, однако известны и другие механизмы передачи инфекции:
На первой стадии инфекции трипаносомы размножаются в подкожных тканях, крови и лимфе. Эта стадия известна как гемолимфатическая фаза болезни, для которой характерны приступы лихорадки, головная боль, увеличение лимфоузлов, боль в суставах и зуд.
На второй стадии паразиты проходят гематоэнцефалический барьер и инфицируют центральную нервную систему. Эта стадия известна как неврологическая, или менингоэнцефалитическая. В целом на этой стадии появляются наиболее очевидные признаки и симптомы болезни: изменение поведения, спутанность сознания, сенсорные расстройства и нарушение координации движений. Важным клиническим признаком на этой стадии является нарушение цикла сна, которое и дало название этой болезни. Без лечения сонная болезнь считается смертельной, хотя известны случаи здорового носительства инфекции.
Ведение болезни: постановка диагноза
Ведение болезни осуществляется в три этапа:
Во избежание необходимости применения сложных и тяжелых методов лечения диагностика должна выполняться как можно раньше до развития неврологической стадии заболевания.
Ввиду длительного и бессимптомного течения первой стадии сонной болезни, вызванной T. b. gambiense, рекомендуется организация тщательного и активного скрининга групп риска с целью выявления пациентов на ранней стадии заболевания и ограничения дальнейшего распространения инфекции посредством их лечения, после которого они перестают выступать в качестве резервуара. Всесторонний скрининг населения требует серьезных финансовых вложений в кадровые и материальные ресурсы. В Африке, особенно в отдаленных районах с наибольшей распространенностью заболевания, этих ресурсов часто не хватает. В результате часть инфицированных умирает еще до постановки диагноза и получения лечения.
Лечение
Тип лечения зависит от формы и стадии заболевания. Раннее выявление болезни повышает шансы на успешное излечение. Ввиду того, что паразит может сохранять жизнеспособность в течение длительного времени и вызывать рецидивы через много месяцев после окончания терапии, для оценки результатов лечения пациенты должны оставаться под наблюдением в течение периода продолжительностью до 24 месяцев, в рамках которого следует проводить клиническое обследование пациентов и выполнять лабораторные исследования физиологических жидкостей, в том числе, в некоторых случаях, спинномозговой жидкости, полученной путем люмбальной пункции.
Для успешного лечения болезни на второй стадии необходимо применение лекарственных препаратов, способных преодолевать гематоэнцефалический барьер и нейтрализовывать паразита в центральной нервной системе.
В 2019 г. ВОЗ опубликовала новое руководство по лечению гамбийской формы африканского трипаносомоза человека. Зарегистрировано в общей сложности шесть препаратов для лечения сонной болезни. Эти препараты предоставляются ВОЗ производителями безвозмездно и на бесплатной основе поставляются в эндемичные страны.
Препараты для лечения болезни на первой стадии:
Препараты для лечения болезни на второй стадии:
Препараты для лечения заболевания на обеих стадиях:
Фексинидазол – пероральный препарат для лечения гамбийской формы африканского трипаносомоза человека. В 2019 г. препарат был включен в Перечень основных лекарственных средств ВОЗ и рекомендован в руководстве ВОЗ по лечению африканского трипаномомоза человека. Препарат показан в качестве терапии первой линии на первой и нетяжелой второй стадии заболевания. Лечение должно проводиться под наблюдением квалифицированного медицинского персонала; препарат принимается через 30 минут после приема твердой пищи. В настоящее время проводятся клинические испытания этого препарата для лечения родезийской формы трепаносомоза.
Частно-государственные партнерства
В 2000 и 2001 гг. ВОЗ учредила частно-государственное партнерство с компаниями Aventis Pharma (в настоящее время Sanofi) и Bayer HealthCare, в результате чего была создана программа по эпиднадзору и борьбе с данным заболеванием под руководством ВОЗ, в рамках которой эндемичным странам предоставляется поддержка в осуществлении противоэпидемических мероприятий и бесплатно поставляются лекарственные препараты.
Партнерство неоднократно продлевалось в 2006, 2011, 2016 и 2021 г. Успехи в сокращении числа случаев сонной болезни и появление реальной перспективы ее элиминации побудили ряд других партнеров из частного сектора поддержать инициативу ВОЗ по элиминации болезни как проблемы общественного здравоохранения и обеспечению ликвидации передачи инфекции к 2030 г.
Деятельность ВОЗ
ВОЗ оказывает содействие и техническую поддержку национальным программам по борьбе с сонной болезнью.
Организация на безвозмездной основе поставляет эндемичным странам противотрипаносомные лекарственные средства в рамках частно-государственных партнерств с компаниями Sanofi (пентамидин, меларсопрол, эфлорнитин и фексинидазол) и Bayer HealthCare (сурамин и нифуртимокс). Отгрузка и транспортировка лекарственных препаратов осуществляется совместно с логистическим отделением организации «Врачи без границ» MSF-Logistics.
Для содействия разработке новых и недорогостоящих средств диагностики ВОЗ в 2009 г. создала банк образцов биоматериалов, которыми могут пользоваться исследователи. В банке, размещенном в Институте Пастера в Париже, хранятся образцы крови, сыворотки, спинномозговой жидкости, слюны и мочи, взятые у пациентов, инфицированных обеими формами болезни, а также образцы, взятые у неинфицированных людей из эндемичных районов.
В 2008 г. ВОЗ выступила с инициативой по созданию атласа африканского трипаносомоза человека с данными обо всех зарегистрированных случаях заболевания на уровне сельских поселений. Инициатива осуществляется совместно с ФАО в рамках Программы борьбы с африканским трипаносомозом (ПБАТ). Атлас представляет собой динамическую базу данных, которая содержит географические и эпидемиологические данные, собранные ВОЗ на основе информации, представляемой национальными программами по борьбе с сонной болезнью, НПО и научно-исследовательскими институтами.
В 2014 г. в целях активизации и поддержки усилий по элиминации болезни по инициативе ВОЗ была создана координационная сеть по африканскому трипаносомозу человека. В число партнеров этой сети вошли национальные программы по борьбе с сонной болезнью, организации, занимающиеся созданием новых лекарственных и диагностических средств, международные и неправительственные организации, а также организации-доноры.
Программа ВОЗ призвана решать следующие задачи:
Сонная болезнь (трипаносомоз, болезнь Шагаса)
Общие сведения
Трипаносомоз представляет собой тропическое трансмиссивное заболевание, вызываемые простейшими микроорганизмами класса жгутиковых — трипаносомами. Различают африканский трипаносомоз (синонимы — sleeping sickness, африканская сонная болезнь) и американский трипаносомоз (синонимы — болезнь Шагаса, morbus Shagasy, в разговорной речи неправильно произносимые болезнь Чагаса и синдром Чагаса). Каждый их этих видов имеет свое географическое распространение, который определяется ареалом обитания переносчиков заболевания.
Африканская сонная болезнь — ареалом обитания мух цеце вида Glossina palpalis (около 36 стран тропической Африки — русло реки Конго, Гамбия, Уганда, Нигерия, Руанда, Буркина-Фасо, Камерун, Габон, Кения, Мозамбик, Замбия, Экваториальная Гвинея, Зимбабве, Гана и другие), на территории которых проживает около 50-60 миллионов человек, подверженных высокому риску заражения трипаносомозами. Ареал обитания («мушиный пояс») составляет около 4 млн кв. км.
Американский трипаносомоз — распространен преимущественно в эндемичных районах 23 стран Латинской Америки, в ареале обитания при поцелуйных (конусоносных/триатомовых) клопов, названия которых различаются в зависимости от географической области. В настоящее время по информации ВОЗ от болезни Шагаса погибает ежегодно около 10 000 человек, инфицировано около 7-8 миллионов человек и около 25 миллионов человек проживают в группе высокого риска. При этом, это заболевание в последние годы все чаще встречается и странах западной части Тихого океана, США, Канаде и даже европейских странах, что обусловлено все возрастающими в различных направлениях миграционными процессами. Если лечение болезни Шагаса начато сразу после инфицирования, то можно добиться полного выздоровления. При запущенной болезни у 30% инфицированных лиц развиваются изменения со стороны сердечной системы, а у 10% лиц – изменения в нервной/пищеварительной системе или смешанного характера, требующие специального лечения.
Патогенез
Африканская сонная болезнь
Трипаносомы в своих метациклических формах проникают в человеческий организм после укуса инфицированной мухой цеце и начинают активно размножаться в подкожной клетчатке. При родезийском трипаносомозе в месте укуса часто образуется трипаносомный шанкр (местный воспалительный очаг). По мере размножения на протяжении нескольких суток трипаносомы проникают в лимфатические/кровеносные сосуды, способствуя тем самым диссеминации возбудителя и генерализации патологического процесса. Этот процесс обусловлен преимущественным поражением лимфатической системы, ЦНС и сердца (панкардит). В начальных стадиях процесса происходит увеличение лимфоузлов и селезенки, в дальнейшем — могут развиться фиброзные изменения в тканях этих органов, периваскулит и эндартериит с выраженной пролиферацией эндотелия мелких кровеносных сосудов.
После проникновения трипаносом в цереброспинальную жидкость и головной мозг развивается менингоэнцефалит/менингомиелит с выраженной нейроглиальной пролиферацией и периваскулярной инфильтрацией в мягкой мозговой оболочке спинного/головного мозга с развитием отека, кровоизлияния и тромбозов в структуры головного мозга, c образованием гранулем. При дальнейшем развитии патологического процесса развиваются периваскулиты сосудов мозга, пролиферация астроцитов и микроглии с развитием — облитерация сосудов мозга с выраженными множественными геморрагиями.
Характерной особенностью сонной болезни является чередование периодов обострения и ремиссий, что сопровождается колебаниями уровня паразитемии, повышением уровня сывороточных IgM и изменением антигенных вариантов трипаносом. Доказано, что часть размножившейся субпопуляции трипаносом после попадания в кровь элиминируется, что обусловлено защитным действием гуморального/клеточного механизмов иммунитета человека.
Выживаемость возбудителя осуществляется за счет изменения последовательности аминокислот гликопротеина, покрывающего оболочку паразита сплошным слоем. При этом, антигенная изменчивость структуры молекулы гликопротеина может происходить неоднократно и во множестве вариантов. Соответственно в патогенезе трипаносомоза такие иммунопатологические процессы способствуют образованию иммунных комплексов, циркулирующих в крови с отложением во внутренних органах. Кроме того, трипаносомы в организме человека оказывают иммуносупрессивное действие, что способствует ослаблению резистентности организма и развитию вторичных инфекционных осложнений на поздних стадиях заболевания. По сути, патогенез можно свести к механическому разрушению клеток/тканей пораженных органов и токсико-аллергическому воздействию на организм человека.
Американский трипаносомоз
Паразиты после укуса клопа внедряются в гистиоциты окружающей ткани, там же размножаются и разносятся с кровью по организму. Далее происходит трансформация трипомастигот в амастиготы, которые интенсивно размножаются и формируются псевдоцисты, представляющие собой погибшие клетки, которые заполнены амастиготами.
Далее, развитие инфекционного процесса может происходить по-разному. В острой стадии происходит интенсивное размножение и гематогенная диссеминация трипаносом. Псевдоцисты, окружённые плазматическими клетками и лимфоцитами обнаруживаются в клетках самых различных тканей, но преобладает их локализация в миокарде и гладких мышцах кишечника. В дальнейшем по мере развития болезни инфильтрация иммунокомпетентными клетками нарастает, но паразиты остаются живыми на протяжении всей жизни человека. В основе патогенеза острой стадии лежат как процессы деструкции клеток тканей, так и токсико-аллергические реакции.
Трипаносома cruzi относится к паразитам с выраженными иммуногенными свойствами и вызванный иммунный ответ носит не только защитный характер, но и вызывает повреждения тканей человека (отложение иммунных комплексов), приводящих к изменениям в стенках кровеносных сосудов. Также, уже в острой стадии наблюдается наряду с поражением мышечных клеток и повреждение ганглиев парасимпатической нервной системы.
При хронизации болезни Шагаса патологический процесс ограничен преимущественным поражением тканей сердца и кишечника. В основе лежат патологические изменения в эндокарде и изменения в проводниковой системе. Как следствие воспалительного процесса отмечается избирательное поражение проводящих путей. В миокарде – развиваются очаговые/диффузные инфильтраты и множественные кровоизлияния. При прогрессировании миокардита в большинстве случаев развивается сердечная недостаточность. Структурные изменения в эндокарде и формирование аневризм приводят к возникновению пристеночных тромбов, что является причиной тромбоэмболии в системе большого/малого кругов кровообращения.
В патогенезе хронической фаз, существенное значение отводится дегенерация автономных интрамуральных ганглиев гладких мышц кишечника, что обусловливает расширение пищевода и толстого кишечника и нарушение их функции, реже — желчного/мочевого пузыря и желудка. У подавляющего большинства лиц, которые инвазированны Т. cruzi, клинические проявления сразу не развиваются и такое состояние рассматривается как промежуточная стадия между острой стадией/инфицированием и хронической. А хроническая клинически выраженная стадия развивается лишь по истечению 10-20 лет.
Классификация
Американский трипаносомоз
Форма — острая, хроническая.
Причины
Африканский трипаносомоз
Этиология. Сонную болезнь вызывают два подвида трипаносом: Trypanosoma brucei gambiense, вызывающая гамбийскую и Trypanosoma brucei rhodesiense, вызывающая родезийскую клинико-эпидемиологическую форму заболевания. Оба вида паразитов, которые вызывают африканскую сонную болезнь по морфологическим признакам идентичны, однако при развитии инвазии антигенная структура возбудителя меняется.
Морфологическая структура трипаносомы
Трипаносома — одноклеточный микроорганизм класса жгутиковых простейших с размерами тела 15-40 х 1,4-2 мкм, морфологическая структура которого содержит оболочку и цитоплазму, в которую погружены клеточное ядро, митохондрии.
Морфологически возбудитель может различаться в зависимости от его носителя: у промежуточных хозяев — преимущественно жгутиковые инвазивные формы, обеспечивающих им возможность активно передвигаться, а у конечных хозяев — безжгутиковые формы.
Способны существовать исключительно в качестве паразитирующей формы жизни. Могут активно размножаться посредством продольного митоза в теле и промежуточного и постоянного хозяина. Жизненный цикл трипаносомы включает 2 стадии: стадию эпимастиготы — в организме переносчика и стадию трипомастиготы — в организме человека. Процесс развития включает смену двух хозяев — позвоночных животных и беспозвоночных.
Эпидемиология
Для гамбийской трипаносомы основным хозяином является человек. Переносчик сонной болезни и промежуточный хозяин — муха цеце семейства Glossina (вид G. Tachinoides), основными местами обитания которых являются заросли по берегам водоемов (рек и озер). Относится к антропонозам (инфекциям, которые передаются от человека к человеку). Пик заболеваемости приходится на сухой сезон года и может проявляться как спорадической заболеваемостью, так и принимать характер эпидемических вспышек. Встречается (картf ниже) преимущественно в странах Центрального/Западного африканского континента (Уганда, Нигерия, Заир, Гамбия, Камерун, Ангола), регистрируют преимущественно в жилых пунктах, расположенных недалеко от водоемов.
Больные лица составляют всего 2-3% всей от реально инфицированных лиц. Хроническое течение заболевания способствует длительному нахождению инфицированных лиц среди популяции здоровых, что увеличивает риск переноса возбудителя мухами.
Основным природным резервуаром родезийской трипаносомы являются лесная антилопа, в качестве дополнительного резервуара выступают крупный рогатый скот, различные дикие животные и человек. Родезийская (синоним восточноафриканская) форма африканского трипаносомоза является природно-очаговой зоонозной инвазией. Переносчик — муха цеце вида Glossinamorsitans и Glossinapallidipes. Заражение людей происходит преимущественно в период нахождения в природных очагах. Встречается (карта ниже) на территории стран Южной/Восточной Африки (Танзания, Зимбабве, Эфиопия, Ботсвана, Уганда, Кения).
Механизм передачи возбудителя, пути заражения
Основной механизм передачи: облигатно-трансмиссивный, при котором возбудитель передается через укус (инокуляцию) переносчиком. Значительно реже встречается гемотрансфузионный путь передачи (при переливании инфицированной крови, использовании нестерильного мед. инструментария).
Трипаносомы в форме трипомастиготы при всасывании мухой крови инфицированного человека попадают в желудок насекомого, где размножаются, превращаются в эпимастиготы и мигрируют в слюнные железы. Цикл развития трипаносом в теле мухи занимает от 15 до 35 суток. Зараженность дикой популяции мух цеце составляет 1-1,5% и лишь у 10-12% мух возбудитель завершает свой цикл развития.
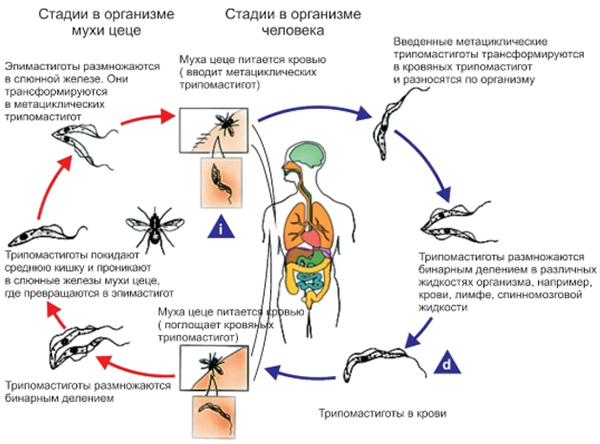
При укусе здорового человека паразиты вводятся в организм со слюной мухи, где трипаносомы сначала размножаются в подкожной клетчатке в месте укуса, а затем возбудитель попадает в лимфатические сосуды/кровь и распространяясь по организму, проникает в сердце, печень, спинномозговую жидкость, головной мозг, почки, селезенку, костный мозг. Схематически стадии развития трипаносом в организме мухи и человека представлены на рисунке.
Больной человек становится заразным ориентировочно с 10-12 дня после укуса насекомого и остается таковым на протяжении всего периода болезни.
Стадии развития трипаносом в организме мухи цеце/человека
Американский трипаносомоз
Этиология. Болезнь Шагаса, названная так в честь ее первооткрывателя K. Шагаса, вызывает trypanosoma cruzi, которая морфологически не отличается от возбудителей африканской сонной болезни. Однако, трипаносома крузи имеет другой цикл развития, включающем несколько, последовательно меняющихся морфологических стадий паразита: трипомастигота, эпимастигота, промастигота и амастигота. По сути, Т. cruzi совершает два цикла развития: один из них в кишечнике триатомового клопа, а второй — в организме позвоночных животных. Процесс размножение этого вида происходит только на стадии амастиготы (безжгутовые округлые образования) первично в месте проникновения в клетках кожи/под слизистыми оболочками, далее — в макрофагах прилегающих к месту укуса лимфатических узлов, а на более поздних стадиях — в клетках гистиофагоцитарной системы селезенки, кишечника, лимфатических узлов, скелетной мускулатуре, в мышце сердца, нейроглии. Трипомастиготы находятся в крови человека/животных и могут передаваться переносчикам-клопам при их нападении на инфицированного/больного человека.
Эпидемиология. Болезнь Шигаса относится к антропозоонозам (группе болезней с природной/синантропной очаговостью). Источником инфекции в природных очагах являются различного рода дикие животные: обезьяны, броненосцы, летучие мыши сумчатые грызуны и другие. В синантропных очагах — домашние животные (свиньи, собаки, кошки) и человек. Переносчик синдрома Шагаса — различные виды триатомовых клопов, в частности, семейства Reduviidae и Dimidiata (Википедия, рис.4.).
Триатомовые клопы (а, б)
Возбудитель американского трипаносомоза передается в основном, через укусы/фекалии клопов, которые обитают как в гнездах птиц/норах животных, так в поселениях человека, преимущественно в неблагоустроенных строениях из соломы, глины. Нападение клопов на людей происходит ночью, а места укуса располагаются в основном около губ/глаз, отсюда и их название «поцелуйные клопы».
Укус инфицированного клопа с повреждением кожных покровов и последующее частое попадание экскрементов клопа в ранку от укуса при ее расчесывании обеспечивает проникновение достаточной инфекционной дозы (метациклический формы трипаносомы) для развития заболевания. Значительно реже заражение происходит при напрямую от больного человека к здоровому при гемотрансфузиях внутриутробно, при трансплантации органов, с молоком материи или алиментарным путем, через пищу, загрязненную испражнениями клопа.
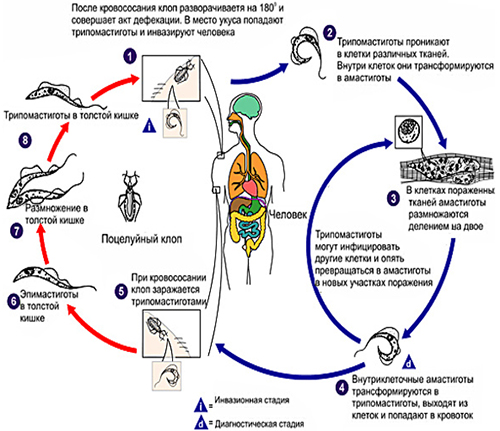
Метациклические формы трипаносомы, являющиеся инвазионной стадией для организма человека, попав в макрофаги кожи/подкожно-жировой клетчатки трансформируются в лейшманиальные (амастиготные формы), которые интенсивно размножаются. Затем, трипаносомы после разрушения клеток сначала трансформируются в критидиальные (эпимастиготные), а далее в трипаносомные (трипомастиготные) формы, циркулирующие, но не размножающиеся в крови. Трипаносомы с током крови попадают и поражают ткани различных органов, где безжгутиковые формы проходят интенсивное размножение.
Цикл развития трипаносомы Cruzi в организме клопа и человека
Географическое распространение — болезнь встречается преимущественно на территории стран южно-центральной Америки (Мексика, Аргентина, Бразилия, Парагвай, Гватемала, Венесуэла, Коста-Рика, Уругвай, Гондурас, Боливии, и Панама).
Перенесённой трипаносомоз стойкого иммунитета после себя не оставляет. Основной причиной препятствующей развитию специфического иммунитета является антигенная изменчивость трипаносом. Образующиеся антитела, являясь специфичными по отношению к определенному антигенному варианту трипаносомы, подавляют его численность, однако, на новый вариант не действуют.
Симптомы
Симптомы сонной болезни
Инкубационный период гамбийской сонной болезни составляет 2-3 недели, родезийской — 1-2 недели. Клинические проявления африканской сонной болезни характеризуются разнообразием симптомов и их неспецифичностью, поскольку в разных эндемичных очагах они существенно варьируют по частоте встречаемости и выраженности их проявлений.
Для родезийского трипаносомоза характерно более острое течение с отсутствием чётко выраженных различий между острой и хронической стадией. Сопровождается лихорадкой, ранним поражением ЦНС (через 3-4 недели от начала заболевания), выраженным поражением сердца, и достаточно быстро наступающим летальным исходом (в течение нескольких недель).
Для гамбийского трипаносомоза характерно более позднее поражение ЦНС (через 2-4 месяца после заражения), длительное хроническое прогрессирующее течение, выраженное поражение лимфоузлов.
На протяжении 7-15 дней на коже (в месте укуса мухи цеце) преимущественно у не коренных жителей Африки, которые инфицированы T.b. rhodesiense может развиться трипаносомный шанкр: темно-красная папула эластичная, болезненная, диаметром от 2 до 5 см, которая исчезает спонтанно через 2-3 недели.
Выделяют 2 стадии болезни:
Ранняя (гемолимфатическая) стадия
Проявляется лихорадкой, продолжительность которой варьирует от 2 до 7 суток. Острое начало более характерно при инфицировании T.b. rhodesiense для некоренных африканцев. Для лиц, проживающих в Западной Африке характерно обычно постепенное начало болезни, и может пойти несколько лет до появления первой клинический симптоматики. На ранней стадии приступы лихорадки часто чередуются с периодами ремиссии, продолжительностью от 2-3 недель до нескольких месяцев, на протяжении которых больные себя чувствуют удовлетворительно. На этой стадии появляются нейропсихические изменения — бессонница, головная боль, возбудимость, реже сонливость.
В ряде случаев на коже появляется эритематозная сыпь, имеющая овальную форму диаметром 7-10 см с преимущественной локализацией в области плеч и бедер, туловища. У некоренных жителей может наблюдаться гиперестезия (симптом Керанделла) — болезненность кожи при сжатии. При прогрессировании болезни появляется увеличение лимфоузлов преимущественно в заднем шейном отделе/над ключицей). При этом, лимфоузлы эластичные, подвижные, безболезненные. В ранней стадии могут отмечаться кожный зуд, потеря веса, слабость, отеки/боли в суставах конечностей, тахикардия, гепатоспленомегалия, периорбитальные отеки.
Хроническая (менингоэнцефалитическая) стадия
Клиническая симптоматика обусловлена развитием диффузного менингоэнцефалита с поражением преимущественно структур основания мозга. Характерно нарастание неврологических симптомов — нарушение мышечного тонуса, сна, моторной функции, рефлексов орального автоматизма. Незаметно появляются и прогрессивно нарастают нейропсихические изменения, проявляющиеся развитием депрессивных/маниакальных состояний.
Первоначально отмечаются изменения личности и поведения — усталость, равнодушие и безразличие к окружению, сонливость днем и ночная бессонница. У ряда лиц выявляются экстрапирамидные расстройства (тремор языка/пальцев, ригидность затылочных мышц, фибриллярные подергивания мышц). Речь невнятная, появляются симптомы мозжечковой атаксии, приводящие к нарушению походки. При отеке мозга — отек диска зрительного нерва, сильная головная боль. По мере прогрессирования заболевания появляются эйфория, эпилептиформные судороги, маниакальное состояние, выраженная сонливость. При вовлечении в патологический процесс гипоталамо-гипофизарной зоны нарушается чувство голода, жажды, либидо, появляются эндокринные нарушения (импотенция, аменорея , ожирение).
В терминальной стадии пациенты лежат неподвижно в постели, от пищи отказываются. Причинами смерти чаще бывают развитие церебральной комы, кахексия, присоединении вторичной инфекции (пневмония, малярия, дизентерия). При африканском трипаносомозе симптомы сонной болезни сопровождаются гемолитической анемией, тромбоцитопенией, а также, нарушением свертываемости крови.
Родезийская сонная болезнь имеет более скоротечное и тяжелое течение. Интоксикация/лихорадка выражены сильнее, истощение наступает быстрее, чаще отмечается поражение сердца. Летальный исход может наступить еще до перехода заболевания в менингоэнцефалитическую стадию уже на первом году болезни.
Американский трипаносомоз
Выделяют несколько форм клинического течения.
Острая форма — регистрируется в эндемических очагах преимущественно у детей в возрасте до 10 лет. Длительность острой стадии варьирует в пределах 1-1,5 месяцев, при этом, симптомы острой стадии могут быть слабо выражены и даже остаться незамеченными. Инкубационный период при острой клинически манифестной форме длится 10-12 суток. Начало острое с ознобом и повышением температуры тела. Характерны боль в глазах, анорексия, недомогание, головная и мышечная боль, диспепсические расстройства.
В месте внедрения трипаносомы Cruzi через кожу в большинстве случаев развивается первичный аффект — шагома (локальная воспалительная реакция), представляющая собой инфильтрацию на коже красно-фиолетового цвета, напоминающую умеренно болезненный фурункул. Шагома часто сопровождается регионарным лимфангиитом/лимфаденитом. При заражении через конъюнктиву глаз первичный аффект представлен резким периорбитальным отеком, конъюнктивитом со стороны поражения со скудными выделениями, увеличением регионарных лимфоузлов (симптомокомплекс Романьи).
Болезнь сопровождается лихорадкой ремитирующего характера, с подъемами температуры в вечернее время до 39-40°С, но при доброкачественном течении лихорадочная реакция незначительная. У больных в остром периоде болезни увеличиваются лимфоузлы практически всех групп — подмышечные, шейные, паховые, отмечается гепатоспленомегалия. Выражены изменения со стороны сердца — границы расширены влево, систолический шум, тахикардия, глухость тонов.
При тяжелом течении сердечная недостаточность быстро прогрессирует и является одной из основных причин летальных исходов. Также, тяжелое течение заболевания часто осложняется менингоэнцефалитом, протекающего с выраженной клиникой неврологических нарушений.
Неопределенная форма — какие-либо клинически выраженные признаки болезни отсутствуют, за исключением наличия положительных серологических реакций. Длительность этой фазы инфекционного процесса может продолжаться много лет, а ориентировочно у 2/3 инфицированных лиц и до конца жизни. У оставшейся 1/3 лиц через 10-20 лет развивается клиническая симптоматика хронической формы трипаносомоза, обусловленная поражением сердца, органов ЖКТ, периферической нервной системы.
Хроническая форма — ведущим признаком является миокардиопатия, отмечаются дилатация желудочков сердца, кардиомегалия. По мере прогрессирования заболевания развивается недостаточность кровообращения, нарушения ритма сердца, тромбоэмболии, в частности и легочных артерий. Характерно и нарушение функции эндокринной, центральной/вегетативной НС.
На ЭКГ — нарушения проводимости и возбудимости (блокады и экстрасистолии). Наряду с миокардиопатией к важным клиническим синдромам относится «мегаколон», представляющий собой дилатацию (расширение) внутренних органов, преимущественно пищевода и сегментов толстого кишечника (сигмовидной кишки), что приводит к запорам, нарушению глотания и развитию кишечной непроходимости. При резком прогрессировании болезни развивается кахексия.
Анализы и диагностика
Диагноз устанавливается на основании данных эпидемиологические анамнеза, клинической симптоматики и лабораторных исследований, включающих:
Микробиологическое исследование ликвора/крови
Лечение
Лечение и выбор препарата определяется типом возбудителя (T. brucei gambiense/T. brucei rhodesiense), стадией заболевания (гемолимфатическая/менингоэнцефалитическая) и побочными действиями препаратов.
На гемолимфатической стадии заболевания традиционно для лечения сонной болезни гамбийской формы сонной болезни используют Сурамин или Эфлорнитин. К препаратам резерва относится Пентамидин. При поражении ЦНС на менингоэнцефалитической стадии назначают Эфлорнитин или Меларсопрол.
При родезийской форме сонной болезни назначают Сурамин или Пентамидин. Однако, следует учитывать, что эти препараты плохо преодолевают гематоэнцефалический барьер, а Эфлорнитин слабо активен в отношении в отношении T. brucei rhodesiense, поэтому на менингоэнцефалитической стадии используется Меларсопрол. Все препараты могут оказывать тяжелые побочные действия, поэтому они должны вводиться под непосредственным контролем врача. Часто развивается тошнота, рвота, артралгия, сыпь, светобоязнь, зуд, появляется артериальная гипотония и даже могут наблюдаться эпилептические припадки. Из тяжелых осложнений — нефротоксическое действие.
Для лечения американского трипаносомоза используют перорально Бензнидазол или Нифуртимокс, которые эффективно подавляют паразитемию и назначаются в ранней (острой) стадии болезни. Препараты токсичны и их прием сопровождается высоким риском развития побочных эффектов. В хронической стадии назначается симптоматическая терапия (сердечные гликозиды, диуретики, ингибиторы АПФ, антикоагулянты, антиаритмические средства и другие).