Селективная нейротомия что это такое
Селективная нейротомия что это такое
Лидирующим заболеванием, приводящим к формированию синдрома спастичности, является детский церебральный паралич (ДЦП), затем следуют нейродегенеративные и сосудистые нарушения головного мозга, а также опухоли и травмы головного мозга [1]. Спастичность (от др.-греч. σπασμóς, от σπáω — «вытягивать») — состояние скелетной мышечной ткани при парезах, проявляющееся расширенной активностью сухожильных рефлексов, гипертонусом мышц и нарушением произвольных движений.
Детский церебральный паралич – это тяжелое заболевание центральной нервной системы, при котором органическое поражение головного мозга плода или новорожденного проявляется чаще всего двигательными нарушениями, вызванными изменением мышечного тонуса, реципрокных взаимоотношений мышц, задержкой редукции примитивных тонических рефлексов и формирования установочных рефлексов [2, 3]. Синдром «спастической руки» наблюдается у 30–40% всех пациентов с ДЦП [3].
Дисфункция верхней конечности резко нарушает возможность самообслуживания, затрудняет обучение письму, лимитирует выбор сферы трудовой деятельности, а также ограничивает способность к передвижению с использованием дополнительных средств опоры [3, 4]. В условиях адаптированной среды современного мира ребенок даже с выраженными нарушениями в сфере движения может получить образование, социализироваться и реализоваться в профессиональной сфере при условии сохранения функциональных возможностей верхних конечностей.
Несмотря на то что сгибательная контрактура локтевого сустава в рамках синдрома «спастической руки» встречается реже прочих, функциональная значимость его разгибания очень велика.
Локтевой сустав является промежуточным суставом верхней конечности, реализующим функциональную связь между плечом и предплечьем. Он позволяет предплечью, которое может занимать любое положение в пространстве в результате движения в плечевом поясе, придавать наиболее функционально выгодное положение кисти [5].
За счет разгибания локтевого сустава и пронации предплечья человек может взять пищу с поверхности стола, а с помощью сгибания верхней конечности в локтевом суставе эта пища подносится ко рту. Таким образом, становится понято, что сгибательная контрактура локтевого сустава может существенно ограничить пациента в такой важной жизненной функции, как самостоятельное питание.
Не менее важной задачей активного разгибания в локтевом суставе для самообслуживания пациента с выраженным снижением опороспособности нижних конечностей является опора на верхнюю конечность при использовании средств опоры [3]. Человек с выраженным ограничением активного разгибания в локтевом суставе не сможет самостоятельно встать из лежачего положения или из инвалидного кресла, передвигаться со средствами опоры. Сгибательная контрактура локтевого сустава может сильно затруднить процесс надевания одежды и обуви [3, 4, 5].
Тоническая контрактура локтевого сустава нередко отмечается в синдроме «спастической руки» и может не проявлять себя в покое, но становится заметной при ходьбе или в момент концентрации пациента на каком-либо другом занятии [6, 7, 8]. Однако в большинстве случаев тоническая контрактура подобной степени выраженности не лимитирует общие функциональные возможности ребенка.
Формирование сгибательной контрактуры обусловлено повышенным мышечным тонусом m.biceps brachii, m.brachialis, m.brachio-radialis, что постепенно приводит к укорочению вышеперечисленных мышц и ретракции капсулы локтевого сустава [9, 10, 11]. Длительно существующие контрактуры могут способствовать развитию суставных и костных деформаций [7, 12, 13].
Для формирования эффективного плана лечения необходимо дифференцировать тоническую контрактуру от фиксированной. С этой целью применяются временные блокады моторных нервов верхней конечности (мышечно-кожного и срединного) или ботулинотерапия [8, 14, 15].
Цель исследования – оценка эффективности селективной невротомии nervus musculo-cutaneus как метода коррекции сгибательной контрактуры локтевого сустава.
Для достижения цели были сформированы следующие задачи:
Материалы и методы исследования
Исследование базируется на оценке результатов обследования и хирургического лечения 17 пациентов с ДЦП, находившихся на лечении в ФГБУ «НМИЦ им Г.И. Турнера» Минздрава России с 2012 по 2020 гг. Разделение по полу пациентов было следующим: мужской пол – 9 детей (53%), женский пол – 8 детей (47%). Возраст пациентов варьировал от 7 до 18 лет, а средний возраст составил 14,5±3,36 года. Из них 10 пациентов были со спастической диплегией, а у оставшихся 7 наблюдался гемипарез с преимущественным поражением верхней конечности. По шкале Ashworth у пациентов, отобранных для исследования, спастичность была III балла и выше.
Эффективность хирургического лечения оценивали на основании: ангулометрических данных (возможность пассивного и активного разгибания в суставах верхней конечности), оценки мышечного тонуса по шкале Ashworth, а также с помощью функциональных показателей верхней конечности.
Мы считали, что именно повышение функциональных возможностей «спастической руки» должно являться основной целью лечения, потому акцент научной работы делали на изменении в показателях функции конечности и в амплитуде активных движений в локтевом суставе. Функциональные возможности верхней конечности в целом мы оценивали по системе MACS (Manual Ability Classification System for Children with Cerebral Palsy 4–18 years) 2002 г. и с помощью следующих функциональных тестов.
Показаниями к проведению нейрохирургического лечения сгибательной контрактуры локтевого сустава с преимущественно тонической составляющей мы считали:
а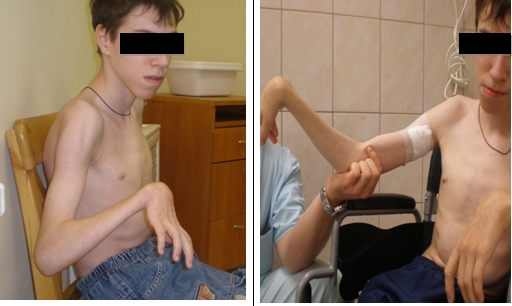
Рис. 1. Пациент А., 13 лет с диагнозом: ДЦП. Спастическая диплегия. Иллюстрация влияния диагностической блокады nervus musculo-cutaneus. Демонстрация предельно возможного активного разгибания локтевого сустава: а – состояние до диагностической блокады,
б – состояние во время действия диагностической блокады
Критериями исключения из исследования мы считали: невозможность произвольных движений в локтевом суставе, отсутствие перспектив хирургического лечения за счет низкого уровня мотивации и невозможности послеоперационной реабилитации, выраженную умственную отсталость.
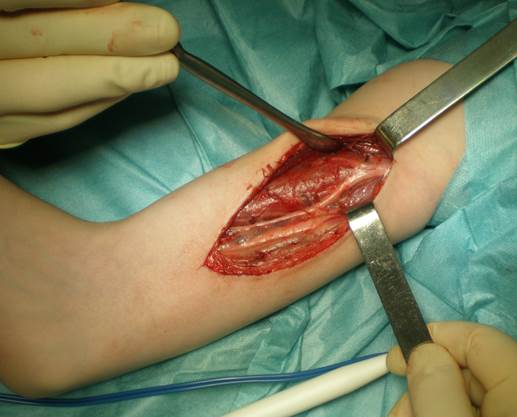
Технически применяемая нами методика нейрохирургического лечения сгибательной контрактуры локтевого сустава была следующей: мы применяли классический доступ к мышечно-кожному нерву по внутренней поверхности плеча в верхней и средней его трети (рис. 2).
Рис. 2. Хирургический доступ к nervus musculo-cutaneus для проведения селективной невротомии
Необходимо тщательно верифицировать положение ствола мышечно-кожного нерва перед его вхождением в клювовидно-плечевую мышцу, иначе существует вероятность упустить дополнительно отходящие от него ветви.
После обнаружения мы мобилизовали все отходящие от ствола nervus musculo-cutaneus ветви в пределах хирургического доступа. Для дифференциации моторной ветви от чувствительной, а также с целью уточнения иннервируемой ею мышцы мы применяли метод электростимуляции (стимуляция двигательного нерва провоцирует мышечное сокращение, а стимуляция чувствительного нерва не дает видимого эффекта). Отобранные для проведения селективной невротомии моторные ветви мы разделяли на пучки и после повторного электростимуляционного тестирования выполняли невротомию гиперактивных пучков в запланированном объеме. Объем невротомии мы определяли, ориентируясь на сочетание таких факторов, как выраженность спастичности мышц-сгибателей локтевого сустава у пациента и степень моторного ответа на электростимуляцию. В среднем мы пересекали 70% от объема двигательного нерва, добиваясь снижения электровозбудимости мышц-мишеней в 8–10 раз при электростимуляционном тестировании.
В послеоперационном периоде верхнюю конечность фиксировали с помощью гипсовой повязки (лонгеты) в положении максимального разгибания в локтевом суставе. Двигательную реабилитацию после оперативного лечения мы начинали после исчезновения болевого синдрома (обычно это происходило на 3–4-е сутки).
Осложнений хирургического лечения в рамках проведенного исследования выявлено не было.
Статистический анализ проводили с применением программ Microsoft Excel 2019 (Microsoft, USA) и SPSS Statistic v.23 (IBM, USA). Для оценки уровеня значимости различий, измеренных в двух разных условиях на одной и той же выборке пациентов, мы применяли непараметрический T-критерий Вилкоксона.
Результаты исследования и их обсуждение
Первичная оценка результатов производилась через 3 месяца после оперативного лечения, но окончательные результаты мы анализировали только спустя 1 год.
Хороший результат лечения мы отметили у 88% пациентов (15 детей), неудовлетворительные результаты были у 12% (2 пациентов). Неудовлетворительным результат был по причине полного рецидива спастичности и тонической контрактуры. Первично результат лечения подходил под критерии хорошего, но со временем наметился постепенный рецидив патологического мышечного тонуса двуглавой мышцы плеча. Начался этот процесс через 3 месяца после невротомии, а полный рецидив произошел в срок 6 месяцев. Удовлетворительных результатов нами получено не было.
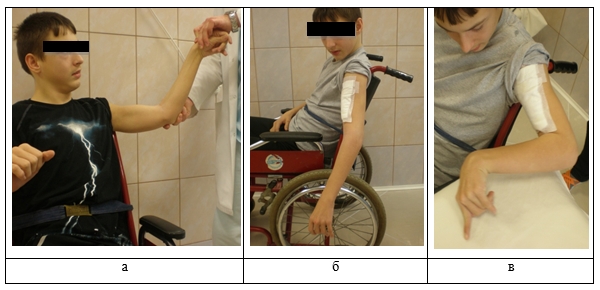
На рисунке 3 представлены фотографии, демонстрирующие хорошие результаты невротомии мышечно-кожного нерва.
Рис. 3. Больной Ш. 16 лет. Диагноз: детский церебральный паралич. Спастическая диплегия. Результат селективной невротомии nervus musculo-cutaneus (a – сгибательная контрактура локтевого сустава до оперативного лечения; б, в – появившаяся активная амплитуда движений локтевого сустава в результате нейрохирургического лечения)
Для оценки результата нейрохирургического лечения мы анализировали влияние операции на тонус мышц-сгибателей локтевого сустава. Его снижение было значительным: на III–IV балла по шкале Ashworth он понизился у 15 пациентов (88%) и на II балла – у 2 детей (12%).
Результаты влияния невротомии на амплитуду движения в локтевом суставе представлены в таблице.
Динамика средних показателей амплитуды активного движения в суставах верхней конечности до и после нейрохирургического лечения
Оцениваемое движение в суставе
Амплитуда движений в суставе
Динамика показателей в результате проведенного лечения
Микрохирургическая нейротомия полового члена при преждевременной эякуляции.
Пациент после данной небольшой операции может свободно контролировать эякуляцию. За время, проходящее до того, как чувствительность кожи головки полового члена полностью восстановится, мужчина привыкает самостоятельно регулировать продолжительность полового акта, и сохраняет эту способность и в последующем. На эректильную функцию данная операция никак не влияет.
Показания и противопоказания к нейротомии полового члена.
Противопоказания в микрохирургической нейротомии:
1. сердечно-сосудистые заболевания, сахарный диабет в стадии декомпенсации;
2. острые воспалительные процессы в органах мочеполовой системы.
Методика микрохирургической нейротомии полового члена при преждевременной эякуляции.
Подготовка к микрохирургической нейротомии полового члена.
При наличии положительного эффекта от пробы со спреем лидокаина или с мазью с анестезином в виде увеличения продолжительности полового акта, проводится стандартная подготовка к хирургическому лечению. Волосы на лобке и на половых органах сбриваются вечером, накануне операции.
Обратная связь с доктором, ответы на вопросы по нейротомии полового члена.
Появились вопросы по нейротомии полового члена?
Вы можете задать их мне:
Или позвоните по телефону 8 (499) 397-84-98, и запишитесь на прием к доктору Миленину!
Буду рад Вам помочь! Всегда ваш, доктор Кузьма Миленин.
Задайте вопрос доктору Кузьме Миленину:
* Поле «Сайт» заполнять не нужно. Свой вопрос напишите, пожалуйста, в поле «Комментарий».
Нейротомия
Микрохирургическая нейротомия — хирургическое вмешательство, заключающееся в пересечении (денервации), мобилизации и по показаниям ренервации нервов, обеспечивающих чувствительность кожи головки и внутреннего листка крайней плоти полового члена. При этом, в зависимости от индивидуальных особенностей пациента, результатов осмотра и диагностики, выбранной и проведённой методики нейротомии происходит временное (на срок от 4-6-ти месяцев до 2-3 лет) и/или постоянное снижение чувствительности кожи головки полового члена, что сопровождается выраженным увеличением продолжительности полового акта.
Пациент после операции может свободно контролировать наступление эякуляции. За время, проходящее до того, как чувствительность кожи головки полового члена восстановится (полностью или частично – зависит от выбранной методики проводимой операции), мужчина привыкает самостоятельно регулировать продолжительность полового акта, формируется новый нейрофизиологический механизм полового акта, и сохраняет эту способность и в последующем. На эректильную функцию операция никак не влияет.
Показания к нейротомии полового члена.
Противопоказания в микрохирургической нейротомии:
Методика микрохирургической нейротомии полового члена при преждевременной эякуляции.
Операция, как правило, проводится под местной анестезией. На верхней поверхности ствола полового члена, ближе к основанию производится разрез кожи длиной 15 — 20 мм. Рядом с дорзальным сосудистым пучком выделяется и пересекается дорзальный нерв полового члена. Кожная рана ушивается. Швы снимаются на 7-10-е сутки. Половая жизнь возобновляется через 2-3 недели после операции, т.е. сразу после заживления послеоперационной раны.
Подготовка к микрохирургической нейротомии полового члена.
При наличии положительного эффекта от пробы со спреем лидокаина или с мазью с анестезином в виде увеличения продолжительности полового акта, проводится стандартная подготовка к хирургическому лечению. Волосы на лобке и на половых органах сбриваются вечером, накануне операции.
В клинике «ВироМед» ежедневно принимают пациентов лучшие специалисты города. В нашей клинике нейротомия полового члена пройдет без боли, потери времени и будет стоит приемлемых денег!
Селективная нейротомия что это такое
Спастические синдромы встречаются при ряде неврологических заболеваний. К ним относятся последствия позвоночно-спинномозговых травм, острых нарушений церебрального и спинального кровообращения, детские церебральные параличи, рассеянный склероз и ряд других нейродегенеративных заболеваний. Повышенный мышечный тонус приводит к ограничению объема активных и пассивных движений, ограничивает реабилитационные возможности больных и при длительном существовании может приводить к развитию фиксированных контрактур и деформаций опорно-двигательного аппарата. В ряде случаев спастичность приводит к развитию болевого синдрома.
Лечение спастических синдромов включает консервативную терапию, физиотерапию и ортезирование, ботулинотерапию и нейрохирургические вмешательства. Консервативное и физиотерапевтическое лечение обычно бывает эффективно при легких и умеренных спастических синдромах. При выраженном повышении мышечного тонуса (3 балла и более по шкале Ashworth) приходится прибегать к более радикальным методикам лечения. При генерализованных формах спастического синдрома, охватывающего многие мышечные группы, оптимальным методом лечения является нейрохирургическое вмешательство: задняя селективная ризотомия, DREZ-томия (деструкция зоны входа задних корешков в спинной мозг), хроническая электростимуляция спинного мозга, хроническая интратекальная терапия с использованием имплантируемых помп [1, 2, 6, 14]. При локальных спастических синдромах во многих случаях эффективно применяется ботулинотерапия [3]. Однако в тех случаях, когда эффект ботулинотерапии незначителен либо отсутствует, возникают показания для применения селективной невротомии.
Селективная невротомия основана на парциальном пересечении двигательных фасцикулярных пучков периферических нервов. Впервые эту операцию осуществил F. Lorenz в 1887 г. у больного с нижним спастическим парапарезом [8]. В 1912 г. A. Stoffel впервые выполнил невротомию срединного нерва путем пересечения моторных фасцикул внутри нервного ствола [14]. Широкого распространения тогда эта операция не получила ввиду большого количества осложнений: мышечной слабости, сенсорных расстройств, болевого синдрома. Однако в 1976 г. Гросс (цит. по [9]) ввел селективную невротомию в широкую клиническую практику благодаря применению микрохирургической техники и нейрофизиологического картирования. На сегодняшний день селективная невротомия широко применяется для лечения ботулинорезистентных спастических синдромов верхних и нижних конечностей.
Материал и методы
Исследованием охвачены 18 больных [(15 (83%) мужчин и 3 (17%) женщины, в возрасте 3—42 года (в среднем 10,8 года)] (см. таблицу).

Все больные до операции получали консервативную лекарственную терапию миорелаксантами центрального действия (баклофен, сирдалуд). Во всех случаях лекарственное лечение оказалось неэффективным. Всем больным до операции проводилось от 2 до 4 курсов ботулинотерапии препаратом Диспорт. В 12 случаях ботулинотерапия не имела эффекта. В 6 случаях в начале терапии отмечался хороший клинический эффект, однако повторные блокады оказались неэффективны. В 7 случаях больным предварительно проводилось нейрохирургическое лечение: в 3 — выполнялась задняя селективная ризотомия на поясничном уровне, в 4 — имплантация хронических электродов на поясничное утолщение спинного мозга и нейростимулятора (система Itrel3). Эффект нейрохирургического лечения оказался неполным, у больных сохранилась спастичность в отдельных мышечных группах.
В исследование были включены все пациенты (2010—2012). Срок катамнестического наблюдения составил от 1,5 до 2 лет. К критериям включения в исследование относились: высокий уровень спастичности — от 3 баллов и выше; резистентность к консервативной лекарственной терапии и физиотерапии; резистентность к ботулинотерапии.
К исключающим критериям относились: грубые деформации опорно-двигательного аппарата; общие противопоказания хирургическому лечению и общей анестезии.
До операции пациенты проходили комплексное обследование с участием нейрохирурга, невролога, физиотерапевта и ортопеда. Уровень мышечного тонуса оценивался в каждой мышечной группе по шкале Ashworth от 1 до 5 баллов. Также оценивался объем пассивных и активных движений с видеорегистрацией стандартных двигательных тестов и ходьбы. Локомоторный статус оценивался по стандартизированной шкале GMFM-88. Такое же обследование проводилось через 3, 6, 12 и 24 мес после операции. Предоперационные и послеоперационные значения уровня мышечного тонуса и локомоторного статуса подвергались статистической обработке по критерию Вилкоксона. Значение p 
Пациенты находились в стационаре в течение 7 сут после операции до снятия швов. Сразу же после выписки начиналось активное реабилитационное лечение.
Результаты
После операции в большинстве случаев отмечалось значительное снижение спастичности по шкале Ashworth: от 4,02±0,52 до операции до 1,86±0,63 балла после операции (p 
Из 11 больных, которым выполнялась невротомия запирательного нерва, полный регресс перекреста отмечался у 6 (54%) (рис. 3).

Из 5 больных, которым выполнялась невротомия большеберцового нерва, полный регресс эквинусной деформации стопы был достигнут у 4 (75%) (рис. 4).

У больного, которому выполнялась невротомия лучевого нерва по поводу спастичности в трехглавой мышце плеча, было отмечено полное восстановление объема движений в локтевом суставе.
Послеоперационных осложнений в нашей серии наблюдений не отмечалось. Ни в одном случае не было рецидива спастического синдрома в катамнезе. Оценка динамики локомоторных функций проводилась нами в катамнезе через 3, 6, 12 и 24 мес после операции. У 11 (61%) больных через 6 мес после операции отмечена положительная динамика локомоторного статуса, оцененного по шкале GMFM-88: от 50,7±12,92 до операции до 54,9±13,6% после операции (p
Хирургическое лечение преждевременной эякуляции
Преждевременная эякуляция (ранняя эякуляция) — устойчивое наступление оргазма и эякуляции у мужчины до наступления оргазма у женщины, которое происходит более чем в 50 % случаев и приносит одному или обоим супругам чувство психологического и сексуального неудовлетворения. Это достаточно частая половая дисфункция, которым по разным данным страдает от 25 до 50% мужчин молодого возраста и около 20% мужчин среднего возраста.
Различают три степени преждевременной эякуляции:
Факторы, влияющими на время до наступления эякуляции у мужчины, могут быть как физиологические — тип половой конституции, время после последнего полового контакта, усталость, чувствительность половых органов и поза при половом контакте, так и патологические — воспалительные заболевания мужских половых органов, инфекции, передающиеся половым путем, злоупотребление алкоголем, некоторыми лекарствами препаратами, психические и неврологические заболевания.
Преждевременную эякуляцию разделяют на первичную, возникшую с самого начала половой жизни, и вторичную, возникшую после половых отношений, нормальных по длительности.
Причиной преждевременной эякуляции в 90% случаев является простатит или простатовезикулит, а также психологические проблемы
Причиной первичной преждевременной эякуляции наиболее часто является гиперчувствительность головки полового члена или слишком быстрое прохождение импульсов в головном мозге.
Существуют несколько методов лечения ранней эякуляции:
Селективная нейротомия при лечении преждевременной эякуляции
На сегодняшний день, согласно проведенным исследованиям, более чем 1000 мужчин с преждевременной эякуляцией, именно селективная нейротомия — микрохирургическая денервация головки полового члена, является самым эффективным методом лечения преждевременной эякуляции (до 98,9 %).
Перед операцией пациенту проводят биотезиометрию или обсуждают данные «лидокаинового» теста. Если проблема в повышенной чувствительности головки полового члена и применение лидокаина удлиняет половой контакт более чем на 50%, то именно селективная нейротомия поможет пациенту при лечении ранней эякуляции.
Операцию проводят под комбинированной анестезией, местно делается укол лидокаина, а внутривенно вводят препараты, которые снимают тревожной состояние. Такой вид анестезии полностью обезболивает пациента, не вредит сердцу и головному мозгу, давая возможность хирургу работать с нервами под микроскопом.
Селективную нейротомию начинают с циркумцизио — удаления крайней плоти, для профилактики ее отека в послеоперационном периоде. Иногда пациенты желают сохранить крайнюю плоть, что потенциально возможно, но наш опыт говорит о лучших послеоперационных результатах при удалении крайней плоти. После чего с помощью операционного микроскопа с 10-ти кратным увеличением рассекают подкожную фасцию и обнажают фасцию Бакха. Именно в ней проходят сосуды и нервы дорсального комплекса. Очень аккуратно, микрохирургическим инструментом находят и пересекают часть нервов. Если нерв пересечь полностью, не трогая парафасциальное пространство, через 6 мес. произойдет частичное реинервация, то есть чувствительность в этой зоне уменьшится до 20-40%, однако частично восстановится. При пересечении части нерва с сохранением его оболочки чувствительность в зоне нерва восстанавливается на 60-80% за 2 мес. При пережигании нерва электрокоагулятором на месте ожога образуется рубец, и восстановление чувствительности в этой зоне не происходит.
Мы выполняем два вида микрохирургической денервации: мозаичную и дорсальную.
Пациент после операции проводит в клинике несколько часов или сутки у иногородних пациентов. При операции накладываются саморассасывающие швы, их не нужно снимать. Через 3 недели пациент может возобновлять половую жизнь и наслаждаться длительным половым контактом.
Истории пациентов
Пациент К., 29 лет, с 17 лет страдал преждевременной эякуляцией, поэтому, с трудом сохранял устойчивые половые отношения. В 2005 году в г. Днепропетровске для лечения преждевременной эякуляции пациенту выполнена операция циркумцизио, которая не помогла удлинить половой акт.
Через 24 дня после операции пациент смог возобновить активную половую жизнь с длительность полового акта в 15-20 мин., чувством удовлетворения и обоюдным оргазмом у половых партнеров. Кроме того, пациенту удалось восстановить отношения с бывшей женой.